
物质的量浓度相同的下列溶液中,符合按pH由小到大顺序排列的是
A.Na2CO3 NaHCO3 NaCl NH4Cl
B.Na2CO3 NaHCO3 NH4Cl NaCl
C.(NH4)2SO4 NH4Cl NaNO3 Na2S
D.NH4Cl (NH4)2SO4 Na2S NaNO3
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源:2015-2016学年河南省高二上学期期中考试化学试卷(解析版) 题型:选择题
下列物质中,属于强电解质的是( )
A.H2O B.NaCl C.NH3·H2O D.CH3COOH
查看答案和解析>>
科目:高中化学 来源:2016届河南省开封市高三上学期第一次模拟理综化学试卷(解析版) 题型:填空题
[化学—选修2化学与技术]《科学》曾评出10大科技突破,其中“火星上‘找’到水的影子”名列第一。水是一种重要的自然资源,是人类赖以生存不可缺少的物质。水质优劣直接影响人体健康。海洋是化学资源宝库,海洋资源的综合利用具有广阔的前景。人类把海水淡化,就可以得到大量的饮用水,常规蒸馏法,技术和工艺比较完备,但也存在较大缺陷,大量推广离子交换法和电渗析法。
(1)天然水在净化处理过程中加入明矾做混凝剂,其净水作用的原理是_________(用离子方程式表示)
(2)家庭用水可以用肥皂水检验其硬度,因为 。家用净水器中装有活性炭和阳离子交换树脂(NaR),用过的阳离子交换树脂放入 中可再生。
(3)电渗析法淡化海水的示意图如图所示,其中阴(阳)离子交换膜仅允许阴(阳)离子通过。

阳极的主要电极反应式是________。在阴极附近加入无色酚酞,看到的现象是___________________________。淡水的出口为________(填“a”“b”或“c”)。
(4)利用海水制得的食盐,制取纯碱的简要过程如下:向饱和食盐水中先通入气体A,后通入气体B,充分反应后过滤得到晶体C和滤液D,将晶体C灼烧即可制得纯碱。
①滤出晶体C后,从滤液D中提取氯化铵有两种方法:
方法一、通入氨,冷却、加食盐,过滤;
方法二、不通氨,冷却、加食盐,过滤。
对两种方法的评价正确的是(选填编号)_____________。
a.方法一析出的氯化铵纯度更高 b.方法二析出的氯化铵纯度更高
c.方法一的滤液可直接循环使用 d.方法二的滤液可直接循环使用
②提取的NH4Cl中含有少量Fe2+、SO42―。将产品溶解,加入H2O2,加热至沸,再加入BaCl2溶液,过滤,蒸发结晶,得到工业氯化铵。加热至沸的目的是___________。滤渣的主要成分是_______________、____________________。
查看答案和解析>>
科目:高中化学 来源:2016届河南省三门峡市高三上学期第二次月考化学试卷(解析版) 题型:选择题
下列关于物质或离子检验的叙述正确的是( )
A.在溶液中加KSCN,溶液显红色,证明原溶液中有Fe3+,无Fe2+
B.气体通过无水硫酸铜,粉末变蓝,证明原气体中含有水蒸气
C.灼烧白色粉末,火焰成黄色,证明原粉末中有Na+,无K+
D.将气体通入澄清石灰水,溶液变浑浊,证明原气体是CO2
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省高二上第二次段考化学试卷(解析版) 题型:填空题
碳及其化合物有广泛的用途。
(1)反应C(s)+ H2O(g) CO(g)+H2(g) ΔH= +131.3 kJ•mol-1,达到平衡后,体积不变时,以下有利于提高H2产率的措施是 。
CO(g)+H2(g) ΔH= +131.3 kJ•mol-1,达到平衡后,体积不变时,以下有利于提高H2产率的措施是 。
A.增加碳的用量 B.升高温度 C.用CO吸收剂除去CO D.加入催化剂
(2)已知,C(s)+CO2(g) 2CO(g)△H= +172.5 kJ•mol-1
2CO(g)△H= +172.5 kJ•mol-1
则反应CO(g)+H2O(g) CO2(g)+H2(g) △H= ____________________。
CO2(g)+H2(g) △H= ____________________。
(3)CO与H2一定条件下反应生成甲醇(CH3OH),可利用甲醇设计一个燃料电池,用KOH溶液作电解质溶液,多孔石墨做电极,该电池负极反应式为______________________________。
(4)在一定温度下,将CO(g)和H2O(g)各0.16 mol分别通入到体积为2.0 L的恒容密闭容器中,发生以下反应:CO(g)+H2O(g)  CO2(g)+H2(g),得到如下数据:
CO2(g)+H2(g),得到如下数据:
t / min | 2 | 4 | 7 | 9 |
n(H2O)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
其它条件不变,降低温度,达到新平衡前 v(逆) _____ v(正) (填“>”、“<”或“=”) 。
该温度下,此反应的平衡常数K=____________________________;
其它条件不变,再充入0.1mol CO和0.1mol H2O(g),平衡时CO的体积分数______(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省高二上第二次段考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.某盐的水溶液呈酸性,该盐一定是强酸弱碱盐
B.弱电解质溶液稀释后,溶液中各种离子浓度一定都减小
C.水的离子积常数KW随着温度的升高而增大,说明水的电离是吸热反应
D.中和相同体积、相同pH的盐酸和醋酸溶液所需NaOH的物质的量相同
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省高二上第三次月考化学试卷(解析版) 题型:选择题
下列反应的离子方程式书写正确的是
A.氯气与氢氧化钠溶液反应:Cl2 + 2OH-=Cl-+ ClO-+ H2O
B.碳酸钙与稀醋酸反应:CO32-+ 2CH3COOH =2CH3COO-+ H2O+ CO2↑
C.铁粉与稀盐酸反应:2Fe + 6H+=2Fe3+ + 3H2↑
D.铜片与氯化铁溶液反应 Cu + Fe3+ =Cu2+ + Fe2+
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高二上第二次段考化学试卷(解析版) 题型:选择题
NM?3和D?58是正处于临床试验阶段的小分子抗癌药物,结构如下:关于NM?3和D?58的叙述,错误的是
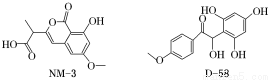
A.都能与溴水反应,原因不完全相同
B.遇FeCl3溶液都显色,原因相同
C.都不能发生消去反应,原因相同
D.都能与NaOH溶液反应,原因不完全相同
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省高三上第三次模拟考试化学试卷(解析版) 题型:选择题
太阳能的开发和利用是21世纪一个重要课题。利用储能介质储存太阳能的原理是:白天在太阳照射下某种盐熔化,吸收热量,晚间熔盐固化释放出相应的能量,已知数据:
盐 | 熔点(℃) | 熔化吸热(kJ·mol-1) | 参考价格(元·t-1) |
CaCl2·6H2O | 29.9 | 37.3 | 780~850 |
Na2SO4·10H2O | 32.4 | 77.0 | 800~900 |
Na2HPO4·12H2O | 35.1 | 100.1 | 1 600~2 000 |
Na2S2O3·5H2O | 45.0 | 49.7 | 1 400~1 800 |
其中最适宜选用作为储能介质的是
A.CaCl2·6H2O B.Na2SO4·10H2O
C.Na2HPO4·12H2O D.Na2S2O3·5H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com