
在25℃时,某稀溶液中由水电离产生的c(OH-)=10-10mol/L。下列有关该溶液的叙述正确的是( )
A.该溶液一定呈酸性
B.该溶液中的c(H+)可能等于10-5
C.该溶液的pH可能为4,可能为10
D.该溶液有可能呈中性
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015-2016学年贵州省高二上学期期中理化学试卷(解析版) 题型:选择题
已知:△H为焓变,△S熵变,下列叙述中正确的是( )
A.△S大于零的反应肯定能自发进行
B.△H小于零且△S大于零的反应一定能自发进行
C.△H小于零的反应肯定能自发进行
D.△H大于 零且△S大于零的反应一定能自发进行
零且△S大于零的反应一定能自发进行
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省龙岩四校高二上学期期中联考化学试卷(解析版) 题型:实验题
电解原理和原电池原理是电化学的两个重要内容。某兴趣小组做如下探究实验:

(1)如上图1为某实验小组依据氧化还原反应设计的原电池装置,若盐桥中装有饱和的KNO3溶液和琼胶制成的胶冻,则NO3-移向_____________装置(填写“甲或乙”)。其他条件不变,若将CuCl2溶液换为NH4Cl溶液,发现生成无色无味的单质气体,则石墨上电极反应式______________________。
(2)如上图2,其他条件不变,若将盐桥换成弯铜导线与石墨相连成n型,则甲装置是____________(填“原电池或电解池”),乙装置中石墨(2)为 极,乙装置中与铁线相连的石墨(1)电极上发生的反应式为 。
(3)在图2乙装置中改为加入CuSO4溶液,一段时间后,若某一电极质量增重 1.28 g,则另一电极生成______________mL(标况下)气体。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省龙岩四校高二上学期期中联考化学试卷(解析版) 题型:选择题
加强能源资源节约和生态环境保护,增强可持续发展能力。下列做法与之不相符的是( )
A.防止废旧电池重金属盐对土壤水资源造成污染,大力开发废旧电池综合利用技术,
B.为减少北方雾霾,作物秸秆禁止直接野外燃烧,研究开发通过化学反应转化为乙醇用作
汽车燃料
C.为节约垃圾处理的费用,大量采用垃圾的填埋
D.为减少温室气体排放,应减少燃煤。大力发展新能源,如核能、风能、太阳能,
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省宣城市等四校高二上期中化学卷(解析版) 题型:选择题
如图是向100mL的盐酸中逐渐加入NaOH溶液时,溶液的pH变化图像。根据图像所得结论正确的是( )
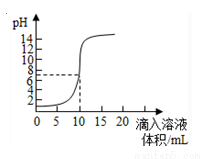
A.原来盐酸的物质的量浓度为0.1mol·L-1
B.可以选择红色石蕊作为指示剂
C.氢氧化钠的物质的量浓度为0.1mol·L-1
D.pH为7时加入的氢氧化钠的物质的量为0.1mol
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省宣城市等四校高二上期中化学卷(解析版) 题型:选择题
下列说法正确的是( )
A.在化学反应中,化学能只可以转化为热能
B.化学键的断裂和形成是化学反应中能量变化的主要原因
C.已知2H2(g)+O2(g)=2H2O(l) △H<0,当反应达平衡后升高温度,反应逆向移动,逆反应速率增大,正反应速率减小
D.合成氨反应N2+3H2  2NH3,当N2、H2、NH3浓度相等时该反应达到了最大限度
2NH3,当N2、H2、NH3浓度相等时该反应达到了最大限度
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省、永年二中高一上期中化学卷(解析版) 题型:实验题


(1)写出下列仪器的名称:
①____________;②____________;④ ;
(2)仪器①~④中,使用时必须检查是否漏水的有 ;图I实验过程中使用冷凝管时应从 处进水(均填序号)。
(3)若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器有 ;将仪器补充完整后进行的实验操作的名称为: 。现需配制500 ml 0.2 mol/L NaCl溶液,装置II是某同学转移溶液的示意图,图中的错误是 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省宁德市高一上期中化学试卷(解析版) 题型:实验题
某同学通过实验研究钠及其化合物的有关性质,请回答相关问题。
(1)实验室中少量的钠通常保存在__________中,在实验室中取用钠的仪器是_______________。
(2)若将钠在空气中加热,钠会燃烧发出黄色火焰,同时生成________________色的固体,写出该产物与H2O反应的化学方程式:___________________。
(3)将金属钠投入水中,发生反应的离子方程式为______________________。
(4)该同学在实验室欲配制500 ml.0.1 mol/L NaOH溶液。
①配制溶液时肯定不需要如图所示仪器中的______________(填字母),配制上述溶液还需要用到的玻璃仪器是_______________(填仪器名称)。

②根据计算,该同学应用托盘天平称取NaOH的质量为________。
③该同学将所配制的NaOH溶液进行测定,发现浓度大于0.1 mol/L。下列操作会引起所配浓度偏大的是___________。
A.烧杯未进行洗涤
B.配制前,容量瓶中有少量蒸馏水
C.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中,并进行定容
D.往容量瓶转移时,有少量液体溅出
E.在容量瓶中定容时俯视容量瓶刻度线
F.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com