
【题目】对如图所示有机物分子的叙述错误的是( )

A. 碱性条件下能发生水解,1 mol该有机物完全反应消耗8 mol NaOH
B. 常温下,能与Na2CO3溶液反应放出CO2
C. 与稀硫酸共热,能生成两种有机物
D. 该有机物遇FeCl3溶液显色
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源: 题型:
【题目】用 NA 表示阿伏加德罗常数,下列说法正确的是
A.用氢氧燃料电池电解饱和食盐水得到 0.4mol NaOH,在燃料电池的负极上消耗氧气分子数为 0.1 NA
B.2 mol H3O+中含有的电子数为 20 NA
C.密闭容器中 1 mol N2(g)与 3 mol H2 (g)反应制备氨气,形成 6 NA 个 N-H 键
D.32 g N2H4中含有的共用电子对数为6 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3是一种重要的化工原料,利用NH3催化氧化并释放出电能(氧化产物为无污染性气体),其工作原理示意图如下。下列说法正确的是
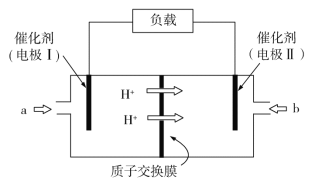
A.电极Ⅰ为正极,电极上发生的是氧化反应
B.电极Ⅰ的电极反应式为2NH36e![]() N2+6H+
N2+6H+
C.电子通过外电路由电极Ⅱ流向电极Ⅰ
D.当外接电路中转移4 mol e时,消耗的O2为22.4 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸合铜(Ⅱ)酸钾[KaCub(C2O4)c·xH2O]是一种重要的化工原料。
(1)二草酸合铜(Ⅱ)酸钾晶体可以用CuSO4晶体和K2C2O4溶液反应得到。从硫酸铜溶液中获得硫酸铜晶体的实验步骤为:加入适量乙醇、蒸发浓缩、冷却结晶、过滤、洗涤、干燥。在蒸发浓缩的初始阶段还采用了蒸馏操作,其目的是_____________________。
(2)某同学为测定草酸合铜(Ⅱ)酸钾的组成,进行如下实验:
步骤Ⅰ测定Cu2+:准确称取0.7080 g样品,用20.00 mL NH4ClNH3·H2O缓冲溶液溶解,加入指示剂,用0.1000 mol·L1的EDTA(Na2H2Y)标准溶液滴定至终点(离子方程式为Cu2++H2Y2![]() CuY2+2H+),消耗EDTA标准溶液20.00 mL;
CuY2+2H+),消耗EDTA标准溶液20.00 mL;
步骤Ⅱ测定C2O42-:准确称取0.7080 g样品,用6.00 mL浓氨水溶解,加入30.00 mL 4.0 mol·L1的硫酸,稀释至100 mL,水浴加热至70~80℃,趁热用0.1000 mol·L1 KMnO4标准液滴定至终点,消耗KMnO4溶液16.00 mL。
①已知酸性条件下MnO4-被还原为Mn2+,步骤Ⅱ发生反应的离子方程式为___________。
②步骤Ⅱ滴定终点的现象是______________________。
③通过计算确定草酸合铜(Ⅱ)酸钾的化学式(写出计算过程)。____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室以海绵铜(主要成分为Cu和CuO)为原料制取CuCl的主要流程如图所示。

已知:①CuCl微溶于水,不溶于乙醇,可溶于氯离子浓度较大的溶液中。
②CuCl露置于潮湿的空气中易被氧化。
回答下列问题。
(1)“氧化”时温度应控制在60~70℃,原因是____________________。
(2)写出“转化”过程中的离子方程式____________________。
(3)“过滤Ⅱ”所得滤液经__________、__________、过滤等操作获得(NH4)2SO4晶体,可用作化学肥料。“过滤Ⅱ”所得滤渣主要成分为CuCl,用乙醇洗涤的优点是________________。
(4)氯化铵用量[![]() ]与Cu2+沉淀率的关系如图所示。随着氯化铵用量的增多Cu2+沉淀率增加,但当氯化铵用量增加到一定程度后Cu2+的沉淀率减小,其原因是__________。
]与Cu2+沉淀率的关系如图所示。随着氯化铵用量的增多Cu2+沉淀率增加,但当氯化铵用量增加到一定程度后Cu2+的沉淀率减小,其原因是__________。

(5)若CuCl产品中混有少量CaSO4,设计提纯CuCl的实验方案:__________。(实验中可选试剂:0.1 mol·L1盐酸、10 mol·L1盐酸、蒸馏水、无水乙醇)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化合物X的叙述正确的是

A. X分子只存在2个手性碳原子
B. X分子能发生氧化、取代、消去反应
C. X分子中所有碳原子可能在同一平面上
D. 1 mol X与足量NaOH溶液反应,最多消耗3 mol NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用CO和H2生产燃料甲醇(CH3OH)。一定条件下密闭容器中发生反应,测得数据曲线如图所示(反应混合物均呈气态)。下列说法错误的是

A.反应的化学方程式:CO+2H2CH3OH
B.反应进行至3分钟时,正、逆反应速率相等
C.反应至10分钟,(CO)=0.075mol/(L·min1)
D.反应至3分钟,用甲醇来表示反应的平均速率为![]() mol/(L·min1)
mol/(L·min1)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍镉(Ni—Cd)可充电电池在现代生活中有广泛应用,它的充、放电反应按下式进行:Cd(OH)2+2Ni(OH)2![]() Cd+2NiOOH+2H2O,有关这个电池的说法正确的是( )
Cd+2NiOOH+2H2O,有关这个电池的说法正确的是( )
A.放电时负极附近的溶液的碱性不变
B.放电时电解质溶液中的OH-向正极移动
C.原电池时的正极反应是:Cd(OH)2+2e-=Cd+OH-
D.原电池时的负极反应是:Cd-2e-+2OH-=Cd(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物M的结构简式如图,有关M的下列叙述中正确的是

A. 可与H2反应,1 molM最多消耗1 molH2
B. 可与浓溴水反应,1molM最多消耗4 molBr2
C. 可与NaOH溶液反应,1 mol M最多消耗3 molNaOH
D. 常温下,M在水中的溶解度小于苯酚在水中的溶解度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com