
【题目】在密闭容器中,一定条件下进行如下反应2NO(g)+2CO(g)![]() N2(g)+2CO2(g),△H=-373.2kJ·mol-1,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
N2(g)+2CO2(g),△H=-373.2kJ·mol-1,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是( )
A.加催化剂同时升高温度B.加催化剂同时增大压强
C.升高温度同时充入N2D.降低温度同时增大压强
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:
【题目】H+、Na+、Al3+、Ba2+、OH、![]() 、Cl七种离子形成了甲、乙、丙、丁四种化合物,它们之间可以发生如图所示转化关系(产物H2O未标出),下列说法不正确的是
、Cl七种离子形成了甲、乙、丙、丁四种化合物,它们之间可以发生如图所示转化关系(产物H2O未标出),下列说法不正确的是

A.白色沉淀A可能能溶解在溶液D中
B.在甲中滴加丁可能发生反应:![]() +Ba2++OHBaCO3↓+H2O
+Ba2++OHBaCO3↓+H2O
C.溶液丙与I、![]() 、
、![]() 可以大量共存
可以大量共存
D.溶液甲中一定满足:c(H2CO3)+c(H+)=c(OH)+c(![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据原子结构,元素周期表填空
(1)某元素的原子序数为33,该元素原子的价电子排布式为____________________________该元素原子核外______个能级,_______个原子轨道。
(2)铜原子核外电子排布式为_________________________,属于第_____周期,______族。
(3)位于第四周期ⅥB族元素核外电子排布式___________________________,价电子的排布图 ____________________。
(4)某元素原子的价电子构型为3d54s2,它属于____区元素,最高正化合价为____,元素符号是_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为1L的密闭容器中,加入5molA物质,在一定条件下同时发生下列两个反应:(1)2A(g)![]() 2B(g)+C(g);(2)A(g)
2B(g)+C(g);(2)A(g)![]() C(g)+D(g)。当达到平衡时,测得c(A)=2.5mol·L-1,c(C)=2.0mol·L-1。则下列说法中正确的是( )
C(g)+D(g)。当达到平衡时,测得c(A)=2.5mol·L-1,c(C)=2.0mol·L-1。则下列说法中正确的是( )
A.达到平衡时c(B)为1.0mol·L-1
B.达到平衡时c(B)=2c(D)
C.达到平衡时c(D)为2.0mol·L-1
D.达到平衡时A的总转化率为40%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在3个容积均为1.0L的恒容密闭容器中发生反应:PCl5(g)![]() PCl3(g)+Cl2(g)。下列说法正确的是
PCl3(g)+Cl2(g)。下列说法正确的是
容器 编号 | 物质的起始浓度(mol·L-1) | 物质的平衡浓度(mol·L-1) | ||
c(PCl5) | c(PCl3) | c(Cl2) | c(Cl2) | |
Ⅰ | 0.4 | 0 | 0 | 0.2 |
Ⅱ | 1.05 | 0.05 | 1.95 | |
Ⅲ | 0.8 | 0 | 0 | |
A.达平衡时,容器Ⅰ中![]() 比容器Ⅱ中的大
比容器Ⅱ中的大
B.达平衡时,容器Ⅰ与容器Ⅱ中的总压强之比为6∶31
C.达平衡时,容器Ⅲ中Cl2的体积分数大于![]()
D.达平衡时,容器Ⅲ中0.4mol·L-1<c(PCl5)<0.8mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1 L含有0.4 mol Cu(NO3)2和0.4 mol KCl的水溶液,用惰性电极电解一段时间后,在一电极上析出19.2 g Cu。此时,在另一电极上放出气体的体积在标准状况下为(不考虑产生的气体在水中的溶解)( )
A.6.72 LB.13.44 LC.3.36 LD.5.6 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是 ( )
A. AlCl3溶液中滴加过量NH3·H2O:Al3+ + 4OH-= AlO2-+ 2H2O
B. 钠与水的反应:Na+2 H2O =Na++2OH-+H2↑
C. NaHSO4溶液中加BaCl2溶液:SO42-+Ba2+=BaSO4↓
D. 氯气与水的反应:Cl2 + H2O = 2 H+ + ClO-+ Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NaHSO4在水中的电离方程式为:NaHSO4 = Na+ + H+ + SO42—。某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。下列对该溶液的叙述中,不正确的是( )
A.该温度高于25℃
B.由水电离出来的H+的浓度是1.0×10-10mol·L-1
C.NaHSO4晶体的加入抑制了水的电离
D.该温度下加入等体积pH为12的NaOH溶液可使该溶液恰好呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
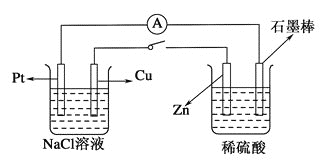
【题目】如下图所示,将两烧杯用导线相连,Pt、Cu、Zn、石墨棒分别为四个电极,当闭合开关后,下列叙述正确的是( )
A.Cu极附近![]() 浓度增大
浓度增大
B.Cu极为电解池阳极
C.电子由石墨棒流向Pt极
D.当石墨棒上有![]() 电子转移时,Pt极上有
电子转移时,Pt极上有![]() 生成
生成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com