
已知反应A2(g)+2B2(g) 2AB2(g)△H <0,下列说法正确的
2AB2(g)△H <0,下列说法正确的
A.升高温度,正向反应速率增加,逆向反应速率减小
B.升高温度有利于反应速率增加,从而缩短达到平衡的时间
C.达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动
D.达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源:2016-2017学年四川省乐山市高一上学期教学质检化学试卷(解析版) 题型:选择题
下列不涉及氧化还原反应的是( )
A.钢铁生锈 B.用铂丝蘸取NaCl溶液进行焰色反应
C.自然界中“氮的固定 ” D.铜铸塑像上出现铜绿[Cu2(OH)2CO3]
” D.铜铸塑像上出现铜绿[Cu2(OH)2CO3]
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省等三校高二上第二次联考化学试卷(解析版) 题型:选择题
只用NaOH溶液不能除去下列各组物质中的杂质(括号内为杂质)的是
A.Mg(Al2O3) B.MgCl2(A1Cl3) C.Mg(Si) D.MgO(SiO2)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省等三校高一12月联考化学卷(解析版) 题型:选择题
在某种强碱性的无色透明溶液中,下列一定能大量共存的离子组是( )
A.K+、AlO2-、Cl-、NO3-
B.MnO4—、SO32-、K+、Cl-
C.Ba2+、CO32-、Cl-、K+
D.HCO3-、K+、SO42—、Cl-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省等三校高一12月联考化学卷(解析版) 题型:选择题
下列有关混合物的分离与提纯的说法正确的是
A. 碘在乙醇中的溶解度较大,可用乙醇把碘水中的碘萃取出来
B. 乙醇的沸点为 78.5℃,可用加生石灰蒸馏的方法使含水乙醇变为无水乙醇
C. 汽油和水不互溶,可用过滤的方法将二者分离
D. NaCl 的溶解度随温度下降而减小,可用冷却法从含少量 KNO3 的热饱和 NaCl 溶液中分离得到纯净的 NaCl
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江省大庆市杜蒙县高二12月月考化学试卷(解析版) 题型:选择题
已知葡萄糖的燃烧热是-2804 kJ/mol,当它氧化生成 1 g 液态水时放出的热量是( )
1 g 液态水时放出的热量是( )
A.26.0 kJ B.51.9 kJ C.155.8 kJ D.467.3 kJ
查看答案和解析>>
科目:高中化学 来源:2017届福建省宁德市高三上学期单科质检模拟化学试卷(解析版) 题型:实验题
为探究某铁碳合金与浓硫酸在加热条件下的反应的部分产物并测定铁碳合金中铁元素的质量分数,某化学活动小组设计了如图所示的实验装置,并完成以下实验探究。
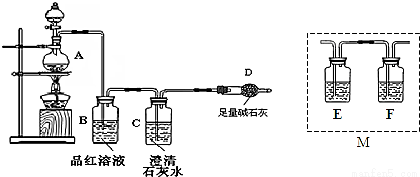
(1)往圆底烧瓶中加入m g铁碳合金,并滴入过量浓硫酸,未点燃酒精灯前,A、B均无明显现象,其原因是:①常温下碳与浓硫酸不反应;② 。
(2)点燃酒精灯,反应一段时间后,从A中逸出气体的速率仍然较快,除因反应温度较高外,还可能的原因是 。
(3)装置B的作用是 。
(4)甲同学观察到装置C中有白色沉淀生成,他得出了使澄清石灰水变浑浊的气体是二氧化碳。装置A中能产生二氧化碳的化学方程式为 。
(5)乙同学认为甲同学的结论是错误的,他认为为了确认二氧化碳的存在,需在装置B-C之间添加装置M。装置E、F中盛放的试剂分别是 、 。重新实验后观察到装置F中的现象是 。
(6)有些同学认为合金中铁元素的质量分数可用KMnO4溶液来测定。(5Fe2+ + MnO4- + 8H+=5Fe3+ + Mn2+ + 4H2O)。测定铁元素质量分数的实验步骤如下:
Ⅰ.往烧瓶A中加入过量铜使溶液中的Fe3+完全转化为Fe2+,过滤,得到滤液B;
Ⅱ.将滤液B稀释为250mL;
Ⅲ.取稀释液25.00mL,用浓度为c mol·L-1的酸性KMnO4溶液滴定,三次滴定实验所需KMnO4溶液体积的平均值为V mL。
① 步骤Ⅱ中,将滤液B稀释为250mL需要用到的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还必须要用到的是 。
② 判断滴定终点的标志是 。
③ 铁碳合金中铁元素的质量分数为 。
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江、吉林省两省六校高三上学期期中联考化学试卷(解析版) 题型:实验题
西安北郊古墓中曾出土一青铜锤(一种酒具),表面附着有绿色固体物质,打开盖子酒香扑鼻,内盛有26 kg青绿色液体,专家认定是2000多年前的“西汉美酒”。这是我国考古界、酿酒界的一个重大发现。
(1)上述报道引发了某校化学兴趣小组同学的关注,他们收集家中铜器表面的绿色固体进行探究。
提出问题:铜器表面附着绿色固体物质是由哪些元素组成的?
猜想:查阅相关资料后,猜想绿色固体物质可能是铜绿。
实验步骤:
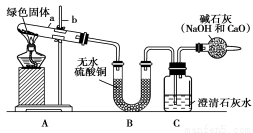
①对试管内的绿色固体进行加热,至完全分解。观察到A装置中绿色固体逐渐变成黑色,B装置中无水硫酸铜变成蓝色,C装置中澄清石灰水变浑浊。
②取少量加热后生成的黑色固体于试管中,加入稀硫酸。观察到黑色固体逐渐溶解,溶液变成蓝 色。
色。
③取少量上述蓝色溶液于试管中,浸入一根洁净的铁丝。观察到铁丝表面有红色物质析出。
④实验结论:绿色固体物质中含有________、________、________、________等元素(用元素符号作答)。(提示:装置内的空气因素忽略不计)
(2)表达与交流
①上述实验步骤③中发生反应的离子方程式________________________。
②干燥管中的碱石灰作用是什么? _。
若反应结束后,如果先移去酒精灯,可能出现的现象是什么? _。
③如果将B、C两装置对调行吗?________。为什么? _____ _______。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省杭州市五校高一上学期联考化学试卷(解析版) 题型:选择题
下列物质分类中,前者包含后者的是
A.氧化物 化合物 B.化合物 电解质 C.溶液 胶体 D.溶液 分散系
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com