
【题目】已知常温下HF酸性强于HCN,分别向1Ll mol/L的HF和HCN溶液中加NaOH固体调节pH(忽略温度和溶液体积变化),溶液中 (X表示F或者CN)随pH变化情况如图所示,下列说法不正确的是
(X表示F或者CN)随pH变化情况如图所示,下列说法不正确的是

A.直线I对应的是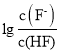
B.I中a点到b点的过程中水的电离程度逐渐增大
C.c点溶液中:![]()
![]()
D.b点溶液和d点溶液相比:cb(Na+)<cd(Na+)
【答案】D
【解析】
A.纵坐标为0时即![]() =1,此时Ka=
=1,此时Ka=![]() =c(H+),因此直线I对应的Ka=10-3.2, 直线II对应的Ka= 10-9.2, 由于HF酸性强于HCN,因此直线I对应
=c(H+),因此直线I对应的Ka=10-3.2, 直线II对应的Ka= 10-9.2, 由于HF酸性强于HCN,因此直线I对应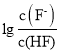 ,A正确;
,A正确;
B.a点到b点的过程中HF浓度逐渐减小,NaF浓度逐渐增大,因此水的电离程度逐渐增大,B正确;
C.Ka(HCN)= 10-9.2 ,NaCN的水解常数Kh(NaCN)=10-4.8>Ka(HCN),因此等浓度的HCN和NaCN的混合溶液中c(CN-)<c(HCN),c点是HCN和NaCN的混合溶液且c(CN-)=c(HCN),因此c(NaCN)>c(HCN),即有c(Na+)>c(CN-);由于OH-、H+来自水的电离,浓度比较小且此时溶液的pH为9.2,C点溶液中存在:c(Na+)>c(CN-)=c(HCN) >c(OH-)>c(H+),C正确;
D.由于HF酸性强于HCN,要使溶液均显中性,HF溶液中要加入较多的NaOH,因此cb(Na+)>cd(Na+),D错误;
答案选D。


科目:高中化学 来源: 题型:
【题目】下列说法均正确的组合为
①s-s σ键与s-p σ键的电子云形状相同
②第四周期的元素基态原子中,4s能级只有1个电子的元素共有3种
③钨的配合物离子[W(CO)5OH]-能催化固定CO2,该配离子中钨显0价
④中心原子采取sp3杂化的分子,其立体构型一定是正四面体
⑤2-丁醇中存在手性碳原子
⑥相对分子质量:CH3CH2OH>CH3CHO,所以沸点:CH3CH2OH>CH3CHO
A.②③⑤B.③⑤C.①②④D.④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某科学工作者通过![]() 射线衍射分析推测胆矾中既含有配位键,又含有氢键,其结构可能如图所示,其中配位键和氢键均用虚线表示。
射线衍射分析推测胆矾中既含有配位键,又含有氢键,其结构可能如图所示,其中配位键和氢键均用虚线表示。
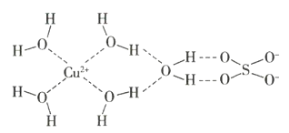
①写出基态Cu原子的核外电子排布式:__。
②写出图中水合铜离子的结构简式(必须将配位键表示出来):__。
(2)很多不饱和有机物在Ni的催化作用下可以与H2发生加成反应,如①CH2=CH2、②CH![]() CH、③
CH、③![]() 、④HCHO等,其中碳原子采取sp2杂化的分子有__(填序号),推测HCHO分子的立体构型为__形。
、④HCHO等,其中碳原子采取sp2杂化的分子有__(填序号),推测HCHO分子的立体构型为__形。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期元素的性质或结构信息如下表所示,请回答下列问题。
元素 | A | B | C | D |
性质或结构信息 | 单质在常温下为固体,难溶于水,易溶于CS2。能形成两种二元含氧酸 | 原子的M层有1个未成对的p电子,核外p电子总数大于7 | 单质曾被称为“银色的金子”与锂形成的合金常用于制造航天飞行器。单质能溶于强酸和强碱溶液 | 原子核外电子层上s电子总数比p电子总数少2。单质和氧化物均为空间网状结构,具有很高的熔、沸点 |
(1)A原子的最外层电子排布式为_______________,D原子核外共有____________个电子。
(2)写出C的单质与强碱溶液反应的离子方程式:______________________________________________。
(3)A、B两元素的氢化物分子中键能较小的是__________________________(填分子式);分子较稳定的是__________________(填分子式)。
(4)E、D同主族,均为短周期元素。它们的最高价氧化物晶体中熔点较高的是________________。
(5)已知D的单质的晶体结构与SiC的晶体结构相似,其中C原子的杂化方式为______________。SiC与D的单质的晶体的熔、沸点高低顺序是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学和生活、社会发展息息相关,从古代文物的修复到现在的人工智能,我们时时刻刻能感受到化学的魅力。下列说法不正确的是
A. 银器发黑重新变亮涉及了化学变化
银器发黑重新变亮涉及了化学变化
B. 煤综合利用时采用了干馏和液化等化学方法
煤综合利用时采用了干馏和液化等化学方法
C. 瓷器主要成分属于硅酸盐
瓷器主要成分属于硅酸盐
D. 芯片制造中的“光刻技术”是利用光敏树脂在曝光条件下成像,该过程并不涉及化学变化
芯片制造中的“光刻技术”是利用光敏树脂在曝光条件下成像,该过程并不涉及化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧化锂(LiOH)是重要的初加T锂产品之一,可用于继续生产氟化锂、锰酸锂等,用天然锂辉石(主要成分LiAISi2O3,含有Fe (III)等杂质)生产LiOH的一种工艺流程如图所示:

已知溶液1中含有Li+、K+、A13+、Na+、Fe3+、SO42-等离子,请回答相关问题。
(l)将LiAlSi2O6改写为氧化物的形式:____。
(2)高温烧结的目的是____。操作1是 __ 。
(3)净化过滤过程中溶液的pH不能过低也不能过高,原因是____。
(4)流程中的某种物质可循环利用,该物质的化学式是____。
(5)工业生产中通过电解LiCI溶液的方法也可制得LiOH,其原理如图所示,电极a应连接电源的____(选填“正极”或“负极”),电极b发生的反应是 ___,阳离子交换膜的作用是___
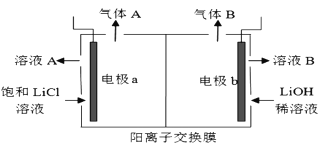
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是一种有机光电材料中间体。实验室由芳香化合物A制备H的一种合成路线如下:

已知:①![]()
②![]()
回答下列问题:
(1)A的化学名称是______________________。
(2)由C生成D和E生成F的反应类型分别是_____________________、____________________。
(3)E的结构简式为______________________________。
(4)G为甲苯的同分异构体,由F生成H的化学方程式为______________________________。
(5)芳香化合物X是F的同分异构体,X能与饱和碳酸氢钠溶液反应放出CO2,其核磁共振氢谱显示有4种不同化学环境的氢,峰面积比为6:2:1:1,写出2种符合要求的X的结构简式:_______________。
(6)写出用环戊烷和2-丁炔为原料制备化合物的合成路线(其他试剂任选) _______________。
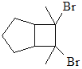
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知苯与液溴的反应是放热反应,某校学生为探究苯与溴发生的反应,用如图装置进行实验。根据相关知识回答下列问题:
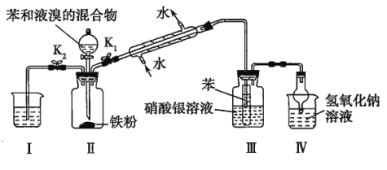
(1)实验开始时,关闭K2,打开K1和漏斗活塞,滴加苯和液溴的混合液,反应开始。一段时间后,在装置Ⅲ中可能观察到的现象是_________。
(2)实验中能防止倒吸的装置有___________(填装置序号)。
(3)反应结束后要使装置Ⅰ中的水倒吸入装置Ⅱ中。这样操作的目的是_________,简述这一操作:________。
(4)通过该实验,可知苯与溴的反应是_______反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知C—C键可以旋转,下列对结构简式如下图的烃的说法正确的是( )
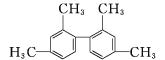
A.该烃属于苯的同系物
B.分子中至少有9个碳原子处于同一平面上
C.分子中至少有10个碳原子处于同一平面上
D.分子中至少有11个碳原子处于同一平面上
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com