
已知某微粒的结构示意图如图所示,请回答:
(1)当x-y=10时,该微粒为 (填“原子”、 “阳离子” 或“阴离子”);
(2)当y=8时,该微粒可能是: 、 、 、 、 (写名称)。
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案科目:高中化学 来源: 题型:
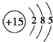
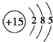

查看答案和解析>>
科目:高中化学 来源: 题型:
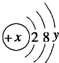 .试回答:
.试回答: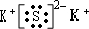
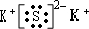
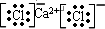
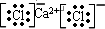
查看答案和解析>>
科目:高中化学 来源: 题型:
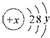 ,试回答:
,试回答:查看答案和解析>>
科目:高中化学 来源:2010—2011学年四川省绵阳中学高一下学期第一次月考化学试卷 题型:填空题
(7分)已知某粒子的结构示意图为
试回答:
(1)当x-y=10时,该粒子为 (填“原子”、“阳离子”或“阴离子”)
(2)写出y =3与y =7的元素最高价氧化物对应水化物间发生反应的离子方程式:
。
(3)当y=8时,粒子可能为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com