
⑴ 在一定温度下,有下列反应发生:
Fe2O3 (s) + 3CO (g) ![]() 2Fe (s) + 3CO2 (g)
2Fe (s) + 3CO2 (g)
① 该反应的平衡常数表达式 K = 。
② 该温度下,在 2L 盛有 Fe2O3 粉末的密闭容器中通入 CO 气体,10min 后,生成了单质铁 11.2g 。则 10min 内 CO 的平均反应速率是 。
③ 请用上述反应中某种气体的有关物理量来说明该反应已达到平衡状态:
a. ;
b. 。
⑵ 在配制 FeCl3 溶液时,加入少许浓盐酸,其目的是:
;
不断加热 FeCl3 溶液,蒸干其水分并灼烧固体,最后得到的物质是 。
⑶ 已知:Fe2O3 (s) + ![]() C(s) =
C(s) = ![]() CO2 (g) + 2Fe(s)
CO2 (g) + 2Fe(s)
△H=+234.1kJ/mol
C (s) + O2 (g) = CO2 (g) △H=-393.5 kJ / mol
则 2Fe (s) + ![]() O2 (g) = Fe2O3 (s)的△H 是 。
O2 (g) = Fe2O3 (s)的△H 是 。
⑷ Fe (OH)2 在空气中短时间内可被氧化为 Fe (OH)3 ,发生的反应为:4Fe(OH)2+O2+2H2O = 4Fe(OH)3 ,下列说法中错误的是
(填字母)。
A. 该反应是能自发进行的反应
B. 该反应是熵增加的反应
C. 该反应是化合反应
D. 该反应是氧化还原反应
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:阅读理解
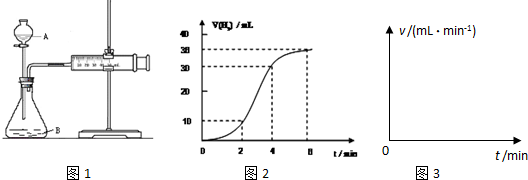
| 编号 | 实验目的 | 锌粒 | 温度 | c(H2SO4) | 需测量的数据 |
| Ⅰ | 为以下实验作参照 | 3粒 | 25℃ | c1 | a |
| Ⅱ | 探究温度对反应速率的影响 | 3粒 | 50℃ | c1 c1 |
b |
| Ⅲ | 探究浓度对反应速率的影响 | 3粒 | 25℃ 25℃ |
c2 | d |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com