
一定温度下,将一定量的冰醋酸加水稀释,稀释过程中溶液的导电性变化如图所示。

则下列说法错误的是
A.醋酸的电离程度:a<b<c
B.溶液的pH值:b<a<c
C.蘸取a点溶液滴在湿润的pH试纸上,测得pH值一定偏大
D.若分别取a、b、c三点的溶液各10 mL,各用同浓度的氢氧化钠溶液中和,消耗NaOH溶液的体积a=b=c
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016-2017学年广东省汕头市高二上学业水平测试化学卷(解析版) 题型:选择题
发展“绿色食品”是提高人类生存质量,维护健康水平的重要措施。所谓“绿色食品”是指( )
A.绿颜色的营养食品 B.有叶绿素的营养食品
C.经济附加值高的食品 D.安全、无公害的食品
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省汕头市高二上学期期中化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.已知C2H6的燃烧热为1090 kJ·mol-1,则表示C2H6燃烧热的热化学方程式为:
C2H6(g)+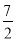 O2(g) = 2CO2(g)+3H2O(g) ΔH=-1090 kJ·mol-1
O2(g) = 2CO2(g)+3H2O(g) ΔH=-1090 kJ·mol-1
B.已知2CO(g)+O2(g) = 2CO2(g) ΔH=-566 kJ·mol-1,则CO的燃烧热ΔH=-283 kJ
C.测定HCl和NaOH反应的中和热时,每次实验均应测量3个温度
D.在稀溶液中:H+(aq)+OH-(aq)=H2O(l) △H=-57.3kJ·mol-1,说明稀醋酸与稀NaOH溶液反应生成1 mol H2O(l)时放出57.3 kJ的热量
查看答案和解析>>
科目:高中化学 来源:2016-2017学年福建省龙岩四校高一上学期期中联考化学试卷(解析版) 题型:选择题
某固体物质只含有钠和氧两种元素,将它放在足量的水中反应产生两种气体,这两种气体又可以在一定条件下反应牛成水。则原固体物质的组成是( )
A.Na2O2与Na2O B.Na2O2 C.Na2O2与Na D.Na和Na2O
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南师大附中高二上期中理化学试卷(解析版) 题型:填空题
向100 mL BaCl2、AlCl3、FeCl3的混合溶液A中逐滴加入Na2SO4和NaOH的混合溶液B,产生沉淀的物质的量n和加入溶液B的体积关系如下图所示:

(1)当加入110 mL B溶液时,溶液中的沉淀是___________(填化学式)。
(2)溶液 B中Na2SO4和NaOH的物质的量浓度之比是___________。当B溶液加到90 mL~100 mL这一段时间中,所发生的离子反应方程式是____________________。
B中Na2SO4和NaOH的物质的量浓度之比是___________。当B溶液加到90 mL~100 mL这一段时间中,所发生的离子反应方程式是____________________。
(3)将A、B溶液中各溶质的物质的量浓度(c)填入下表中。
溶质 | Na2SO4 | NaOH | BaCl2 | AlCl3 | FeCl3 |
c/mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南师大附中高二上期中理化学试卷(解析版) 题型:实验题
用中和滴定法测定某盐酸的物质的量浓度。
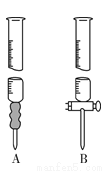
(1)标准溶液应盛于________(填“A”或“B”)滴定管中。
(2)若选用酚酞作指示剂,以0.125 0 mol·L-1的标准氢氧化钠溶液滴定,如何判断滴定终点________________________。
(3)实验数据记录如下表,请分析数据并计算,盐酸的物质的量浓度=__________mol·L-1。
滴定次数 | 待测溶液体积/mL | ||
标准碱液 | |||
滴定前读数/mL | 滴定后读数/mL | ||
1 | 20.00 | 0.00 | 16.02 |
2 | 20.00 | 0.00 | 15.98 |
3 | 20.00 | 0.00 | 16.00 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南师大附中高二上期中理化学试卷(解析版) 题型:选择题
准确移取20.00 mL某待测HCl溶液于锥形瓶中,用0.1000 mol·L-1NaOH溶液滴定,下列说法正确的是
A.滴定管用蒸馏水洗涤后,装入NaOH溶液进行滴定
B.随着NaOH溶液滴入,锥形瓶中溶液pH由小变大
C.用酚酞作指示剂,当锥形瓶中溶液由红色变无色时停止滴定
D.滴定达终点时,发现滴定管尖嘴部分有悬滴,则测定结果偏小
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高一上期中化学试卷(解析版) 题型:填空题
(本题 包括2小题,共8分)
包括2小题,共8分)
I、 向KI和硫酸混合溶液中加入过氧化氢溶液,迅速反应放出大量气泡,溶液呈棕色。
查阅资料知,反应过程如下:
①H2O2+2KI+H2SO4=I2+K2SO4+2H2O;
②H2O2+I2=2HIO;
③H2O2+2HIO=I2+O2↑+2H2O
(1)用双线桥法表示过程①电子转移情况:
H2O2+2KI+H2SO4=I2+K2SO4+2H2O
(2)上述实验过程②与③中,I2起到了___________的作用。
(3) 试判断,酸性条件下HIO、H2O2、O2三种物质氧化性的强弱:___________(填化学式)。
试判断,酸性条件下HIO、H2O2、O2三种物质氧化性的强弱:___________(填化学式)。
II、一定条件下,向含硝酸的废水中加入CH3OH,将HNO3还原成N2。若参加反应的还原剂和氧化剂的物质的量之比是5∶6,则该反应的氧化产物是 ;每转移3 mol电子,反应消耗 g CH3OH。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高一上期中化学试卷(解析版) 题型:选择题
我国科技创新成果斐然,下列成果中获得诺贝尔奖的是( )
A.徐光宪建立稀土串级萃取理论
B.屠呦呦发现抗疟新药青蒿素
C.闵恩泽研发重油裂解催化剂
D.侯德榜创立联合制碱法
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com