
分析 (1)酸溶液的pH小于碱溶液,氢离子浓度越大,溶液的pH越小,据此进行判断;
(2)从盐类的水解和弱电解质的电离程度角度分析;
(3)③和④等体积混合后,溶液溶质为NaCl和NH4Cl、NH3.H2O,从盐类的水解角度分析;
(4)硫酸为二元强酸,醋酸为一元弱酸,则同体积、同物质的量浓度时硫酸溶液完全反应消耗的氢氧化钠溶液体积较大.
解答 解:(1)④氯化铵为强酸弱碱盐,铵根离子水解,溶液呈弱酸性,②醋酸为弱酸,酸性大于氯化铵,①硫酸为强酸,氢离子浓度最大,溶液的pH最小,③氢氧化钠溶液为强碱溶液,其pH最大,所以四种溶液的pH大小顺序为:③④②①,
故答案为:③④②①;
(2)④氯化铵、⑤醋酸铵、⑥硫酸氢铵等溶液中存在:NH4++H2O?NH3•H2O+H+,硫酸氢铵存在大量的H+,抑制NH4+的水解,醋酸铵为弱酸弱碱盐,发生相互促进的水解,三种物质中NH4+浓度最小,⑦氨水为弱电解质,难以电离,在这四种溶液中NH4+浓度最小,所以NH4+浓度由大到小的顺序是:⑥④⑤⑦,
故答案为:⑥④⑤⑦;
(3)③和④按体积比1:2混合后,溶液溶质为NaCl和NH4Cl、氨水,根据物料守恒知,c(Cl-)>c(NH4+),由于溶液中存在:NH3•H2O?NH4++OH-,一水合氨的电离程度大于铵根离子水解程度,则c(NH4+)>c(Na+),溶液呈碱性得c(OH-)>c(H+),故有:c(Cl-)>c(NH4+)>c(Na+)>c(OH-)>c(H+),
故答案为:c(Cl-)>c(NH4+)>c(Na+)>c(OH-)>c(H+);
(4)同体积、同物质的量浓度的①硫酸和②醋酸溶液,硫酸为二元强酸,醋酸为一元弱酸,则硫酸中氢离子的物质的量大于醋酸,所以分别用同浓度的NaOH溶液完全中和,所需NaOH体积大小关系①>②,
故答案为:>.
点评 本题考查溶液离子浓度大小的比较以及盐类的水解和弱电解质的电离等问题,题目难度较大,注意把握影响盐类水解以及电解质的电离的因素,试题培养了学生的分析能力及灵活应用能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题

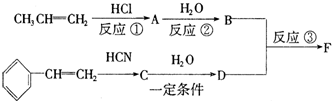
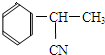 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
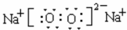 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6种 | B. | 7种 | C. | 5种 | D. | 4种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氟酸存放在棕色玻璃瓶中 | |
| B. | 金属钠存放在盛有煤油的试剂瓶中 | |
| C. | 氢氧化钠溶液保存在磨口玻璃塞的试剂瓶中 | |
| D. | 浓硝酸保存在磨口玻璃塞无色试剂瓶中,并置于阴凉处 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{a}{m+A}$(A-N+m)mol | B. | $\frac{a}{A}$(A一N)mol | C. | $\frac{a}{m+A}$(A-N)mol | D. | $\frac{a}{A}$(A一N+m)mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图,图1表示白磷(P4)的分子结构,图2表示三氧化二磷(P4O6)的分子结构,图3表示五氧化二磷(P4O10)的分子结构,下列说法中正确的是( )
如图,图1表示白磷(P4)的分子结构,图2表示三氧化二磷(P4O6)的分子结构,图3表示五氧化二磷(P4O10)的分子结构,下列说法中正确的是( )| A. | P4O6中的磷原子采用sp2方式杂化 | |
| B. | 三氧化二磷、五氧化二磷这两个名称都表示分子的实际组成 | |
| C. | P4、P4O6和P4O10分子中同一P原子上两个化学键之间的夹角都是60° | |
| D. | P4O6分子中4个P原子构成正四面体,6个O原子构成正八面体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 宇宙飞船中使用的碳纤维,是一种新型无机非金属材料 | |
| B. | 不可用铝制餐具长时间存放酸性、碱性食物 | |
| C. | 明矾可用于净水,氢氧化铝常用于治疗胃病 | |
| D. | 日常生活中人们大量使用铝制品,是因为常温下铝不能与氧气反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com