
【题目】有5种混合溶液,分别由等体积0.1mol/L的两种溶液混合而成:
(1)CH3COONa与NaHSO4 (2)CH3COONa与NaOH, (3)CH3COONa与NaCl
(4)CH3COONa与NaHCO3 (5)CH3COONa与NaHSO3
下列各项排序正确的是( )
A. pH:(2)>(4)>(5)>(3)>(1) B. c(CH3COOH):(1)>(3)>(5)>(4)>(2)
C. c(CH3COO-):(2)>(3)>(4)>(5)>(1) D.  :(1)>(5)>(3)>(4)>(2)
:(1)>(5)>(3)>(4)>(2)
【答案】D
【解析】A、(1)CH3COONa与NaHSO4,溶液显酸性;(2)CH3COONa与NaOH,溶液呈碱性;(3)CH3COONa与NaCl,溶液中醋酸根离子水解显碱性;(4)CH3COONa与NaHCO3,醋酸根离子和碳酸氢根离子水解呈碱性;(5)CH3COONa与NaHSO3 醋酸根离子水解呈碱性,亚硫酸氢根离子电离大于水解显酸性;得到溶液中pH大小为:(2)>(4)>(3)>(5)>(1),故A错误;B、(1)CH3COONa与NaHSO4,溶液显酸性;生成醋酸;(2)CH3COONa与NaOH,溶液呈碱性;氢氧化钠溶液中氢氧根离子抑制醋酸根离子水解;(3)CH3COONa与NaCl,溶液中醋酸根离子水解显碱性;(4)CH3COONa与NaHCO3,醋酸根离子和碳酸氢根离子水解呈碱性,相互抑制;(5)CH3COONa与NaHSO3 醋酸根离子水解呈碱性,亚硫酸氢根离子电离大于水解显酸性;促进醋酸根离子水解;c(CH3COOH)浓度为:(1)>(5)>(3)>(4)>(2),故B错误;C、依据上述分析判断,c(CH3COO-)浓度大小为:(2)>(4)>(3)>(5)>(1);故C错误;D、(1)CH3COONa与NaHSO4,溶液显酸性;生成醋酸;(2)CH3COONa与NaOH,溶液呈碱性;氢氧化钠溶液中氢氧根离子抑制醋酸根离子水解;(3)CH3COONa与NaCl,溶液中醋酸根离子水解显碱性;(4)CH3COONa与NaHCO3,醋酸根离子和碳酸氢根离子水解呈碱性,相互抑制;(5)CH3COONa与NaHSO3 醋酸根离子水解呈碱性,亚硫酸氢根离子电离大于水解显酸性;促进醋酸根离子水解; 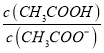 比值大小顺序为:(1)>(5)>(3)>(4)>(2),故D正确;故选D。
比值大小顺序为:(1)>(5)>(3)>(4)>(2),故D正确;故选D。


科目:高中化学 来源: 题型:
【题目】0.5 L某浓度的NaCl溶液中含有0.5 mol Na+,下列对该溶液的说法中不正确的是
A. 量取100 mL,该溶液中溶质的物质的量浓度为1 mol·L-1
B. 该溶液中含有29.25 g NaCl
C. 配制100 mL该溶液,用托盘天平称5.85 g NaCl
D. 量取100 mL该溶液倒入烧杯中,烧杯中Na+的物质的量为0.1 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)有关下列有机物的说法中错误的是
A. 石油经分馏后再通过裂化和裂解得到汽油
B. 植物油通过氢化加成可以变成脂肪
C. 用灼烧的方法可以区别蚕丝和合成纤维
D. 在做淀粉的水解实验时,用碘水检验淀粉是否完全水解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.(1)在2L定容密闭容器中通入1molN2(g)和3molH2(g),发生反应:
3H2(g)+N2(g)![]() 2NH3(g)△H<0,测得压强一时间图像如图甲,测得p2=0.6p1,此时温度与起始温度相同,在达到平衡前某一时刻(t1)若仅改变一种条件,得到如乙图像。
2NH3(g)△H<0,测得压强一时间图像如图甲,测得p2=0.6p1,此时温度与起始温度相同,在达到平衡前某一时刻(t1)若仅改变一种条件,得到如乙图像。

①若图中c=1.6mol,则改变的条件是__________(填字母,下同);
A.升温 B.降温 C.加压 D.减压 E.加催化剂
②若图中c<1.6mol,则改变的条件是__________(填字母);此时该反应的平衡常数__________(填“增大”、“减小”、“不变”)。
(2)如图甲,平衡时氢气的转化率为____________。
Ⅱ.粗制的CuCl2·2H2O晶体中常含有Fe3+、Fe2+杂质,为制得纯净的氯化铜晶体,首先将其制成水溶液,再按下图所示的操作步骤进行提纯。
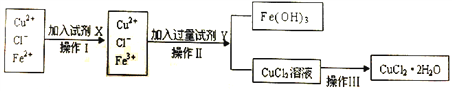
(1)操作Ⅰ时,常先加入合适的氧化剂,将Fe2+氧化为Fe3+,下列可选用的氧化剂是__________。
A.KMnO4 B.H2O2 C.Cl2 D.HNO3
(2)操作Ⅱ调整溶液的pH的Y试剂可选用下列中的__________。
A.NaOH(s) B.氨水 C.CuO(s) D.Cu(OH)2(s)
(3)已知溶度积常数如下表:
物质 | Cu(OH) | Fe(OH)2 | Fe(OH)3 |
Ksp | 2.2×10-20 | 8.0×10-16 | 4.0×10-38 |
将溶液的pH调至pH=4时,使Fe3+完全转化为Fe(OH)3沉淀而除去,此时c(Fe3+)=__________。
(4)若将CuCl2溶液蒸干后,再灼烧,得到的固体是__________(填化学式);操作Ⅲ后由CuCl2·2H2O晶体得到纯净无水CuCl2的合理操作是_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温恒容的密闭容器中通入lmolX和2molY,发生下列反应:X(g)+2Y(g)![]() M(g)+2N(g) △H=akJ/mol(a>0),下列说法中正确的是
M(g)+2N(g) △H=akJ/mol(a>0),下列说法中正确的是
A. 到达平衡状态时,加入催化剂,平衡不移动,反应速率也不会发生改变
B. 反应达到平衡时,X和Y的转化率相等
C. v正(X)=2v逆(N)时,反应到达平衡状态
D. 到达平衡状态时,反应吸收akJ能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X.Y、Z、W四种短周期元素,它们在周期表中位置如图所示,下列说法正确的是

A. 四种元素的原子半径由小到大的顺序为:r(X)<r(Z)<r(W)<r(Y)
B. X、Y、Z既能形成离子化合物,又能形成共价化合物
C. X与其余三种元素之间形成的核外电子总数为10的微粒只有2种
D. H2Z的熔点比HW高,是因为它们的晶体类型不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pH是溶液中c(H+)的负对数,若定义pc是溶液中溶质物质的量浓度的负对数,则常温下,某浓度的草酸(H2C2O4)水溶液中pc(H2C2O4)、pc(HC2O4-)、pc(C2O42-)随着溶液pH的变化曲线如图所示:己知草酸的电离常数Ka1=5.6×10-2,Ka2=5.4×10-5 下列叙述正确的是( )

A. 曲线I表示H2C2O4的变化
B. pH=4时,c(HC2O4-)>c(C2O42-)
C. c(H2C2O4)+c(HC2O4-)+c(C2O42-)在a点和b点一定相等
D. 常温下,  随pH的升高先增大后减小
随pH的升高先增大后减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
①标准状况下,0.2 mol任何物质的体积均为4.48 L ②若1 mol气体的体积为22.4 L,则它一定处于标准状况下 ③标准状况下,1 L HCl和1 L H2O的物质的量相同 ④标准状况下,1 g H2和14 g N2的体积相同 ⑤28 g CO的体积为22.4 L ⑥两种物质的物质的量相同,则它们在标准状况下的体积也相同 ⑦在同温同体积时,气体物质的物质的量越大,则压强越大 ⑧同温同压下,气体的密度与气体的相对分子质量成正比
A. ①②③④ B. ②③⑥⑦⑧ C. ⑤⑥⑦⑧ D. ④⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各物质中所含原子个数由大到小的顺序正确的是( )
①0.3molNH3 ②标准状况下22.4L氯气 ③9mL H2O (4℃) ④0.2mol H3PO4
A. ①④③② B. ④③②① C. ②④③① D. ①④②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com