
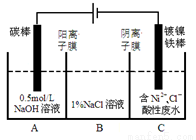
已知:①Ni2+在弱酸性溶液中发生水解 ②氧化性:
Ni2+(高浓度)>H+>Ni2+(低浓度)
A. 碳棒上发生的电极反应:4OH--4e-═O2↑+2H2O
B. 电解过程中,B中NaCl溶液的物质的量浓度将不断减少
C. 为了提高Ni的产率,电解过程中需要控制废水pH
D. 若将图中阳离子膜去掉,将A、B两室合并,则电解反应总方程式发生改变
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源:2016-2017学年山东省济南市高一下学期开学考试化学试卷(解析版) 题型:选择题
某溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-、CO32-等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化的图像如图所示。下列说法正确的是( )

A. 原溶液中含有的阳离子是H+、NH4+、Mg2+、Al3+
B. 原溶液中一定含有SO42-和Na+
C. 原溶液中含有的Fe3+和Al3+的物质的量之比为1:1
D. 反应最后形成的溶液中含有的溶质为Na2SO4
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高二下学期学业水平模拟化学试卷(解析版) 题型:选择题
著名化学家张青莲教授精确测得铟(In)元素的相对原子质量为114.8,该值被国际原子量委员会确认为新标准。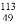 In中含有的中子数是
In中含有的中子数是
A. 49 B. 64 C. 113 D. 114.8
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三下学期期初考试化学试卷(解析版) 题型:简答题
含硫化物是自然界中最为重要的自然资源之一,在生产生活中应用非常广泛。
(1)燃煤烟气的脱硫(除SO2)技术和脱硝(除NOx)技术是环境科学研究的热点。以下是用硫和氮的氧化物之间的相互转化联合进行的脱硫和脱硝技术反应的热化学方程式。
NO2(g)+SO2(g)+H2O(l)=H2SO4(l) +NO(g) △H=a kJ·mol-1
2NO(g)+O2(g)=2NO2(g) △H=b kJ·mol-1
① 反应2SO2(g)+O2(g)+2H2O(l)=2H2SO4(l) 的△H=_______KJ/mol-1。
② 将SO2通入硫酸铁溶液也能发生类似的反应。请写出该反应的离子方程式____________ 。
(2)MnSO4是重要的基础锰盐。工业上,生产MnSO4的方法有多种。
①一种较为环保的方法是:利用纤维素水解产物还原软锰矿的方法生产MnSO4,其反应方程式如下:(C6H10O5)n+nH2SO4→n(C6H11O5)HSO4
n(C6H11O5)HSO4 +nH2O →n C6H12O6+nH2SO4
C6H12O6 +12H2SO4+12MnO2→12MnSO4+6CO2↑+18H2O
从理论上讲,每生产1吨MnSO4需要的纤维素的质量为____吨。
②软锰矿中都含有一定量的砷的化合物,如果不除砷很难达到饲料级的生产标
准。工业上常用氧化剂来除去其中的砷。可以除去砷的氧化剂有:ClO-、KMnO4、(NH4)2S2O8、O3、H2O2等,但在实际生产中,选用的氧化剂是软锰矿,可能的原因是_________。
③在生产MnSO4的浸出渣中常会产生一些硫磺,可以利用四氯乙烯来回收硫磺,
回收硫磺过程中受外界影响较大的因素主要有:萃取温度、液固比等。下图1是上述3种因素对萃取硫磺质量影响的关系图。

请根据以上图表信息,选择最佳的萃取温度和液固比_____________。
(3)有人设想用电化学法将SO2转化为H2SO4的原理如图2所示。

① 该电解质溶液中质子的流向是_____;(填“从正极流向负极”或“从负极流向正极”)
② 写出该电池负极反应的电极反应方程式:_________
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三下学期期初考试化学试卷(解析版) 题型:选择题
下列实验操作、现象与结论对应关系不正确的是
选项 | 操作 | 现象 | 结论 |
A | 向溶有SO2的BaCl2溶液中通入气体X | 产生白色沉淀 | X一定是NO2 |
B | 向NaAlO2溶液中滴入NaHCO3溶液 | 产生白色沉淀 | AlO2-结合H+能力比CO32-强 |
C | 向NaHCO3溶液中加入醋酸,将产生的气体 直接通入苯酚钠溶液中 | 产生白色沉淀 | 酸性:醋酸>碳酸>苯酚 |
D | 浓度均为0.10mol/L的 Na2CO3和Na2S的混合溶液中滴入少量AgNO3溶液 | 产生黑色沉淀 | Ksp(Ag2S)>Ksp(Ag2CO3) |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:2017届江苏省高三下学期期初考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A. 因为液态氨气化时吸热,可用液态氨作制冷剂
B. 用铝制容器盛放浓硝酸,是因为铝和浓硝酸不反应
C. 明矾溶于水生成氢氧化铝胶体,起消毒杀菌的作用
D. 铝能置换出氧化铁中的铁,钢铁工业利用铝热反应冶炼铁
查看答案和解析>>
科目:高中化学 来源:2017届海南省高三第七次月考化学试卷(解析版) 题型:实验题
氧化还原滴定实验与中和滴定类似,是用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之。现用0. 00lmol/L酸性KMnO4溶液滴定未知浓度的NaHSO3溶液,请回答下列问题:
(1)完成滴定的离子方程式(在__中填系数,在___上填物质或离子):_____
____MnO4-+____HSO3-+____=____Mn2++___ ____+___H2O
(2)该滴定实验的仪器除了铁架台、滴定管夹外,还需要下列用品中的_____(填序号)
A.酸式滴定管 B.碱式滴定管 C.漏斗 D.锥形瓶 E.烧杯 F.白纸
(3) KMnO4溶液不能用____(酸、碱)式滴定管盛装,原因是:_______。
(4)是否需要选择指示剂?_____。滴定终点的现象是___________。
(5)滴定前平视KMnO4液面,刻度为amL,滴定后俯视液面刎度为bmL,则(b-a)mL比实际消耗KMnO4溶液体积_______(填“大”、“小”或“无影响”,下同)。根据(b-a) mL计算,得到NaHSO3的浓度比实际的浓度_______。
查看答案和解析>>
科目:高中化学 来源:2017届陕西省高三上学期第二次模考化学试卷(解析版) 题型:填空题
实验室可由软锰矿(主要成分为MnO2)制备KMnO4,方法如下:软锰矿与过量固体KOH和KClO3在高温下反应,生成锰酸钾(K2MnO4)和KCl;用水溶解,滤去残渣,滤液酸化后,K2MnO4转变为MnO2和KMnO4;滤去MnO2沉淀,浓缩滤液,结晶得到深紫色的针状KMnO4。请回答:
(1)软锰矿制备K2MnO4的化学方程式是_______________________;
(2)K2MnO4制备KMnO4的离子方程式是_______________;
(3)若用2.5g软锰矿(含MnO2 80%)进行上述实验,KMnO4的理论产量为_______________。
(4)KMnO4能与热的经硫酸酸化的Na2C2O4溶液反应生成Mn2+和CO2,该反应的化学方程式是________________________;
(5)上述制得KMnO4产品0.165g,恰好与0.335g Na2C2O4反应完全,该KMnO4的纯度为___。
查看答案和解析>>
科目:高中化学 来源:2017届浙江省高三3月选考化学试卷(解析版) 题型:选择题
下列关于能源的说法不正确的是
A. 植物通过光合作用,将太阳能转化为生物质能
B. 在农村推广建造沼气池,是对生物质能的有效利用
C. 天然气的主要成分是甲烷,是一种可再生的清洁能源
D. 氢能是重要的清洁能源,在蓝绿藻、微生物和太阳光作用下使水分解制氢是目前科学家研究的新方法之一
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com