
如右图两个电解槽中,A、B、C、D均为石墨电极。如果电解过程中共有0.02mol电子通过,下列叙述中正确的是
A.甲烧杯中A极上最多可析出铜0.64g
B.甲烧杯中B极上电极反应式4OH--4e-==2H2O+O2↑
C.乙烧杯中滴入酚酞试液,D极附近变红
D.乙烧杯中C极上电极反应式为4H++4e-==2H2↑

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2012-2013学年重庆市杨家坪中学高二12月月考化学试卷(带解析) 题型:单选题
如右图两个电解槽中,A、B、C、D均为石墨电极。若电解过程中共有0.02mol电子通过,正确的是( )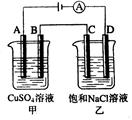
A.甲烧杯中A极上最多可析出铜0.64g
B.甲烧杯中B极上电极反应式4OH--4e-=2H2O+O2↑
C.乙烧杯中滴入酚酞试液,D极附近先变红
D.烧杯中C极上电极反应式为4H++4e-=2H2↑
查看答案和解析>>
科目:高中化学 来源:2014届重庆市高二12月月考化学试卷(解析版) 题型:选择题
如右图两个电解槽中,A、B、C、D均为石墨电极。若电解过程中共有0.02mol电子通过,正确的是( )

A.甲烧杯中A极上最多可析出铜0.64g
B.甲烧杯中B极上电极反应式4OH--4e-=2H2O+O2↑
C.乙烧杯中滴入酚酞试液,D极附近先变红
D.烧杯中C极上电极反应式为4H++4e-=2H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:
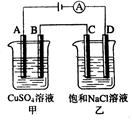
如右图两个电解槽中,A、B、C、D均为石墨电极。若电解过程中共有0.02mol电子通过,下列叙述中正确的是( )
A.甲烧杯中A极上最多可析出铜0.64g
B.甲烧杯中B极上电极反应式4OH--4e-= 2H2O+O2↑
C.烧杯中C极上电极反应式为4H+ + 4e-=2H2↑
D.乙烧杯中滴入酚酞试液,D极附近先变红

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com