
【题目】按以下步骤可由![]() 合成
合成![]() (部分试剂和反应条件已略去)。
(部分试剂和反应条件已略去)。
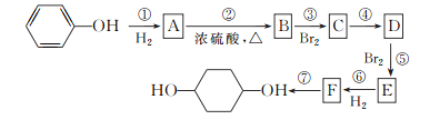
请回答下列问题:
(1)分别写出B、D的结构简式:B__,D___。
(2)反应①~⑦中属于消去反应的是__,属于加成反应的是__(填写序号)。
(3)如果不考虑⑥、⑦反应,对于反应⑤,得到E的可能的结构简式为__。
(4)试写出C→D反应的化学方程式:__(有机物写结构简式并注明反应条件)。
【答案】![]()
![]() ②④ ①③⑤⑥
②④ ①③⑤⑥ 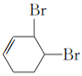 、
、 、
、
![]() +2NaOH
+2NaOH![]()
![]() +2NaBr+2H2O
+2NaBr+2H2O
【解析】
苯酚与氢气发生加成反应生成A,A为![]() ,A发生消去反应生成B,B为
,A发生消去反应生成B,B为![]() ,环己烯与溴发生加成反应生成C,C为
,环己烯与溴发生加成反应生成C,C为![]() ,从C经过系列转化得到
,从C经过系列转化得到![]() ,官能团有-Br转化为-OH且由邻位转化为对位,故C发生消去反应生成D,D为
,官能团有-Br转化为-OH且由邻位转化为对位,故C发生消去反应生成D,D为![]() ,D与溴发生1,4-加成反应生成E,E为
,D与溴发生1,4-加成反应生成E,E为![]() ,E与氢气发生加成反应生成F,F为
,E与氢气发生加成反应生成F,F为![]() ,F发生水解反应生成
,F发生水解反应生成![]() ,据此分析解答。
,据此分析解答。
(1)由上述分析可知,B为![]() ,D为
,D为![]() ,故答案为:
,故答案为:![]() ;
;![]() ;
;
(2)由上述分析可知,反应①~⑦中,①为加成反应,②为消去反应,③加成反应,④为消去反应,⑤为加成反应,⑥为加成反应,⑦为取代反应,故答案为:②④;①③⑤⑥;
(3)如果不考虑⑥、⑦反应,对于反应⑤,![]() 可与溴发生1,2-加成,1,4-加成或完全加成,得到的E可能的结构简式为
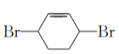
可与溴发生1,2-加成,1,4-加成或完全加成,得到的E可能的结构简式为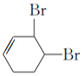 、
、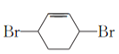 、
、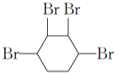 ,故答案为:
,故答案为: 、
、 、
、 ;
;
(4)C→D的反应方程式为:![]() +2NaOH
+2NaOH![]()
![]() +2NaBr+2H2O,故答案为:
+2NaBr+2H2O,故答案为:![]() +2NaOH
+2NaOH![]()
![]() +2NaBr+2H2O。
+2NaBr+2H2O。


科目:高中化学 来源: 题型:
【题目】Mg-H2O2电池可用于驱动无人驾驶的潜航器。该电池以海水为电解质溶液,示意图如下。该电池工作时,下列说法正确的是( )
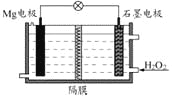
A. Mg 电极是该电池的正极
B. H2O2在石墨电极上发生氧化反应
C. 石墨电极附近溶液的pH 增大
D. 溶液中Cl-向正极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃的结构简式为![]() ,它可能具有的性质是
,它可能具有的性质是
A. 它能使溴水褪色,但不能使酸性高锰酸钾溶液褪色
B. 它既能使溴水褪色,也能使酸性高锰酸钾溶液褪色
C. 易溶于水,也易溶于有机溶剂
D. 能发生加成反应,一定条件下最多可与三倍物质的量的氢气加成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制备丙烯的方法有多种,具体如下(本题丙烯用C3H6表示):
(1)丙烷(C3H8)脱氢制备丙烯(C3H6)
由下图可得,C3H8(g)![]() C3H6(g)+H2(g),△H=_________kJ/.mol
C3H6(g)+H2(g),△H=_________kJ/.mol

(2)用惰性电极电解CO2的酸性溶液可得丙烯(C3H6),其原理如下图所示。则b的电极反应式为__________。
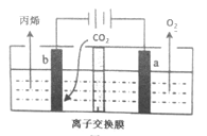
(3)以丁烯(C4H8)和乙烯(C2H4)为原料反应生成丙烯(C3H6)的方法被称为“烯歧化法”,反应为:C4H8(g)+C2H4(g)![]() 2C3H6(g) △H>0
2C3H6(g) △H>0
一定温度下,在一体积恒为VL的密闭容器中充入一定量的C4H8和C2H4,发生烯烃歧化反应。
I.该反应达到平衡的标志是______________
a.反应速率满足:2v生成(C4H8)=v生成(C3H6)
b.C4H8、C2H4、C3H6的物质的量之比为1:1:2
c.混合气体的平均相对分子质量不再改变
d.C4H8、C2H4、C3H6的浓度均不再变化
Ⅱ.已知t1min时达到平衡状态,测得此时容器中n(C4H8)=mmol,n(C2H4)=2mmol,n(C3H6)=nmol,且平衡时C3H6的体积分数为![]() 。
。
①该时间段内的反应速率v(C4H8)= _______mol/(L·min)。(用只含m、V、t1的式子表示)。
②此反应的平衡常数K=______________。
③t1min时再往容器内通入等物质的量的C4H8和C2H4,在新平衡中C3H6的体积分数_______![]() (填“>”“<”“=”)。
(填“>”“<”“=”)。
(4)“丁烯裂解法”是另一种生产丙烯的方法,但生产过程中伴有生成乙烯的副反应发生,具体反应如下:主反应:3C4H8![]() 4C3H6;副反应:C4H8
4C3H6;副反应:C4H8![]() 2C2H4
2C2H4
①从产物的纯度考虑,丙烯和乙烯的质量比越高越好。则从下表现的趋势来看,下列反应条件最适宜的是__________(填字母序号)。
a.300℃0.1MPa b.700℃0.1MPa c.300℃0.5MPa d.700℃0.5MPa
②下图中,平衡体系中丙烯的百分含量随压强增大呈上升趋势,从平衡角度解释其可能的原因是_____。
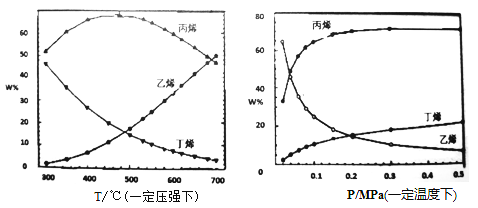
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以两种烃为主要原料合成香料M的路线如下:
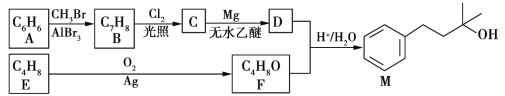
已知:①A分子只有一种氢原子。E能使酸性高锰酸钾溶液褪色,与HBr发生反应可得到2种产物。
②RX![]() R-MgX(X为卤原子)
R-MgX(X为卤原子) ![]() RCH2CH2OMgX
RCH2CH2OMgX![]() RCH2CH2OH
RCH2CH2OH
回答下列问题:
(1)C中官能团名称是__________________;E的名称是__________________。
(2)F的结构简式为__________________;B→C的反应类型是__________________。
(3)写出A→B的化学方程式:____________________________________。
(4)在F的单官能团同分异构体中,除环醚外,还有____________种。其中,在核磁共振氢谱上有3个峰且峰的面积比为1∶1∶6的结构简式为__________________。
(5)写出鉴别A、B两种有机物可选用的化学试剂__________________。
(6)以苯和环氧乙烷(![]() )为原料制备苯乙醇,设计不超过4步的合成路线_________________(无机试剂任选)。
)为原料制备苯乙醇,设计不超过4步的合成路线_________________(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含有对氯苯酚和醋酸钠的废水净化原理如图所示。下列说法错误的是( )

A.本装置集净化、供电于一体,产物之一还有消毒作用
B.每消耗1mol CH3COO-,通过质子交换膜的质子的物质的量为8mol
C.在该装置中,B极上的电势比A极上的电势高
D.A极的电极反应为![]() +H++2e-→
+H++2e-→![]() +Cl-
+Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝及其化合物广泛应用于金属冶炼、有机合成等领域。
⑴铝热反应可以冶炼金属铬,Cr基态核外电子排布式为_______。
⑵已知反应:

①乙酸酐分子中碳原子轨道的杂化类型为______。
②1 mol对甲基苯乙酮分子中含有的σ键的数目为_____。
③甲苯分子难溶于水的原因是______。
④单个AlCl3气态分子的空间构型为______,AlCl3可与Cl-形成AlCl![]() ,与AlCl
,与AlCl![]() 互为等电子体的分子为______。
互为等电子体的分子为______。
(3)某遮光剂的晶胞如右图所示,则n=______。
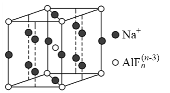
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁有两种氯化物,都是重要的化工试剂,它们的一些性质及制备方法如下所示:
Ⅰ.氯化铁:熔点为306 ℃,沸点为315 ℃,易吸收空气中的水分而潮解。工业上采用向500~600 ℃的铁粉中通入氯气来生产无水氯化铁。
Ⅱ.氯化亚铁:熔点为670 ℃,易升华。工业上采用向炽热铁粉中通入氯化氢来生产无水氯化亚铁。
实验室可用下图所示的装置模拟工业生产无水氯化铁,请回答相关问题:
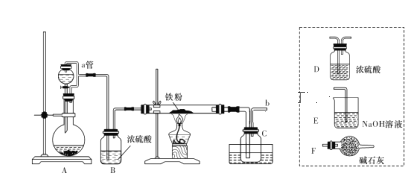
(1)装置A用于KMnO4固体与浓盐酸反应制氯气,a管的作用是______________,反应的离子方程式为__________。
(2)导管b口应与_______________(从虚线框内装置中选择一个装置,用字母代号填空)连接,这样可避免反应系统与环境间的相互影响。
(3)实验完成后,取广口瓶C中收集到的产物进行如下测定
①称取4.2 g样品溶于过量的稀盐酸中;②加入足量H2O2;③再加入足量NaOH溶液;④过滤、洗涤后灼烧沉淀;⑤称量所得红棕色固体为2.40 g。则该样品中铁元素的质量分数为_________。
(4)由以上数据分析和计算得出结论:
①用此装置制得的无水氯化铁含铁量___________ (填“偏高”或“偏低”),显然其中含有较多的___________(填化学式)杂质。
②若要得到较纯净的无水氯化铁,可采取的装置改进措施是 ______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上采用酸性高浓度含砷废水(砷主要以亚砷酸HAsO2形式存在,还含有少量Fe3+等杂质)提取重要化工原料As2O3。工艺流程如下:

(1)“中和”时调节废水的pH为6,NaOH的作用是_____。
(2)“沉砷”时生成的沉淀是Cu(AsO2)2,发生反应的离子方程式是_____;此时使用了过量的CuSO4,原因是_____;沉砷时需控制体系的pH略显碱性,测得Cu(AsO2)2产物中铜元素含量较高,原因是_____。
(3)“还原”时发生反应的化学方程式是_____。
(4)下图表示其他条件不变下“还原”时,反应温度对砷浸出率和铜浸出率的影响(浸出率表示溶液中所要提取的元素被浸出的程度,即元素被浸出的百分率):

为达到铜砷分离尽量彻底的目的,应选择的最佳温度是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com