
| ||
| 3 |
| 4 |
| 3 |
| 4 |


科目:高中化学 来源: 题型:阅读理解
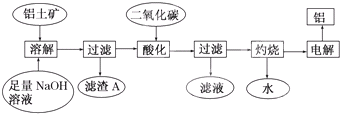
 铝是一种重要的金属,在生产、生活中具有许多重要的用途,如图是从铝土矿中制备铝的工艺流程:
铝是一种重要的金属,在生产、生活中具有许多重要的用途,如图是从铝土矿中制备铝的工艺流程:查看答案和解析>>
科目:高中化学 来源: 题型:
(12分)铝是一种重要的金属,在生产、生活中具有许多重要的用途,右图是从铝土矿中制备铝的工艺流程:
已知:铝土矿的主要成分是Al2O3,此外还含有少量Fe2O3等杂质。
回答下列问题:
(1)写出向铝土矿中加入足量氢氧化钠溶液后,该步操作中铝土矿主要成分发生反应的离子方程式 ,滤渣A的主要成分为 。
(2)在工艺流程第三步中,选用二氧化碳作酸化剂而不使用盐酸的原因是____
__________,通入过量的二氧化碳时,生成沉淀的离子方程式为 _______ 。
(3)电解氧化铝,每生成1molAl时,生成 g氧气。
查看答案和解析>>
科目:高中化学 来源: 题型:
铝是一种重要的金属。
(1)铝在元素周期表中的位置是________。
(2)生产中曾用铝热反应焊接钢轨,铝与氧化铁发生反应的化学方程式为__________________________。
(3)铝与NaOH溶液反应的离子方程式为:__________________________;
同温同压下,在浓度和体积均为100 mL 2 mol/L的盐酸及NaOH溶液中各加入等质量的Al,产生气体的体积比为5:6,则所加Al的质量为________。
查看答案和解析>>
科目:高中化学 来源:2011—2012学年福州八中高一上学期期末考试化学试卷 题型:填空题
(12分)铝是一种重要的金属,在生产、生活中具有许多重要的用途,右图是从铝土矿中制备铝的工艺流程:
已知:铝土矿的主要成分是Al2O3,此外还含有少量Fe2O3等杂质。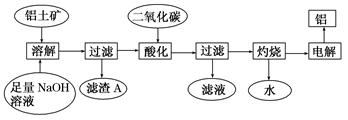
回答下列问题:
(1)写出向铝土矿中加入足量氢氧化钠溶液后,该步操作中铝土矿主要成分发生反应的离子方程式 ,滤渣A的主要成分为 。
(2)在工艺流程第三步中,选用二氧化碳作酸化剂而不使用盐酸的原因是____
__________,通入过量的二氧化碳时,生成沉淀的离子方程式为 _______ 。
(3)电解氧化铝,每生成1molAl时,生成 g氧气。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com