
【题目】已知![]() 在不同的溶剂中可形成不同的分散系:
在不同的溶剂中可形成不同的分散系:![]() 溶解在水中形成无色透明的分散系一;
溶解在水中形成无色透明的分散系一;![]() 溶解在乙醇中形成无色透明的分散系二。下列说法正确的是( )
溶解在乙醇中形成无色透明的分散系二。下列说法正确的是( )
A. 分散系二与雾、霾为同一种类型的分散系
B. 在两个分散系中,![]() 都是以
都是以![]() 和
和![]() 的形式存在
的形式存在
C. 分散系二中,分散质粒子的个数为![]() 个
个
D. 两个分散系都是电解质且性质较稳定
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】五种短周期元素在周期表中的位置如图所示,其中R元素原子的最外层电子数和K层电子数之和等于其次外层电子数,下列判断正确的是
![]()
A. 简单离子的半径大小:Y>Z>R
B. Z的氢氧化物虽然溶解度很小,导电性很差,但它是强电解质
C. Y与X能形成熔点很高的晶体,它是由极性键组成的非极性分子
D. Y与M的最高价氧化物对应的水化物的导电性,Y的不一定比M的强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据下列信息完成所需回答的问题:

其中氧化物A是白色固体;氧化物B是黑色固体;单质D为有毒的黄绿色气体,单质C不溶于冷的浓硝酸。
(1)D是_______;G是_______(填化学式)
(2)写出下列反应的离子方程式:M+NaOH溶液生成G_____________________、G+NaOH溶液生成N______________________________________________________。
(3)单质C不溶于冷的浓硝酸的原因是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】测定![]() 溶液先升温再降温过程中的
溶液先升温再降温过程中的![]() ,数据如下表。实验过程中,取①、④时刻的溶液,加入盐酸酸化的
,数据如下表。实验过程中,取①、④时刻的溶液,加入盐酸酸化的![]() 溶液做对比实验,④产生白色沉淀多。下列说法不正确的是
溶液做对比实验,④产生白色沉淀多。下列说法不正确的是
时刻 | ① | ② | ③ | ④ |
温度 | 25 | 30 | 40 | 25 |
| 9.66 | 9.52 | 9.37 | 9.25 |
A. ![]() 溶液中存在水解平衡:
溶液中存在水解平衡:![]()
B. ④产生的白色沉淀是![]()
C. ①→③的过程中,![]() 在降低
在降低
D. ①→③的过程中,温度与![]() 相比,前者对水解平衡的影响更大
相比,前者对水解平衡的影响更大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应![]()
![]() 在平衡移动时的颜色变化可以用来指示放热过程和吸热过程。下面是某同学的部分实验报告。
在平衡移动时的颜色变化可以用来指示放热过程和吸热过程。下面是某同学的部分实验报告。
| 1.向甲烧杯中加入 2.向乙烧杯中投入一定量的 |
(1)甲烧杯中![]() 球的红棕色变浅,说明平衡
球的红棕色变浅,说明平衡![]() 向______________(填“正反应”或“逆反应”)方向移动,所以
向______________(填“正反应”或“逆反应”)方向移动,所以![]() 晶体溶于水是__________________(填“放热”或“吸热”)过程。
晶体溶于水是__________________(填“放热”或“吸热”)过程。
(2)根据乙烧杯中的现象,补全![]() 与
与![]() 反应过程的能量变化示意图_____。
反应过程的能量变化示意图_____。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电化学原理在防止金属腐蚀、能量转换等方面应用广泛。
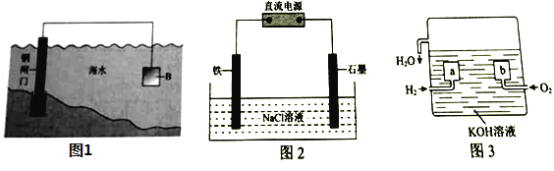
(1)①钢铁在海水中容易发生电化学腐蚀,负极反应式是____________。
②图1中,为减缓钢闸门的腐蚀,材料![]() 可以选择____________(填“
可以选择____________(填“![]() ”或“
”或“![]() ”)。
”)。
(2)图2为钢铁防护模拟实验装置,则铁做_________极,检测钢铁保护效果的方法是:取少量铁电极附近的溶液于试管中,___________,则说明保护效果好。
(3)氢氧燃料电池是一种新型的化学电源,其构造如图3所示:![]() 为多孔石墨电极,通入的气体由孔隙中逸出,并在电极表面放电。
为多孔石墨电极,通入的气体由孔隙中逸出,并在电极表面放电。
①![]() 的电极反应式是__________________;
的电极反应式是__________________;
②若电池共产生![]() 水,则电路中通过了___________
水,则电路中通过了___________![]() 的电子。
的电子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是闪锌矿(主要成分是![]() ,含有少量
,含有少量![]() )制备
)制备![]() 的一种工艺流程:
的一种工艺流程:
![]()
资料:相关金属离子浓度为![]() 时形成氢氧化物沉淀的
时形成氢氧化物沉淀的![]() 范围如下:
范围如下:
金属离子 |
|
|
|
开始沉淀的 | 1.5 | 6.3 | 6.2 |
沉淀完全的 | 2.8 | 8.3 | 8.2 |
(1)闪锌矿在溶浸之前会将其粉碎,目的是______________。
(2)溶浸过程使用过量的![]() 溶液和
溶液和![]() 浸取矿粉,发生的主要反应是:
浸取矿粉,发生的主要反应是:
![]() 。下列判断正确的是____________(填字母序号)。
。下列判断正确的是____________(填字母序号)。
a.浸出液中含有![]() 等阳离子
等阳离子
b.加入硫酸,可以抑制![]() 水解
水解
c.若改用![]() 溶液进行浸取,将发生反应:
溶液进行浸取,将发生反应:![]()
(3)工业除铁过程需要控制沉淀速率,因此分为还原和氧化两步先后进行,如下图。还原过程将部分![]() 转化为
转化为![]() ,得到
,得到![]() 小于1.5的溶液。氧化过程向溶液中先加入氧化物a,再通入
小于1.5的溶液。氧化过程向溶液中先加入氧化物a,再通入![]() 。
。
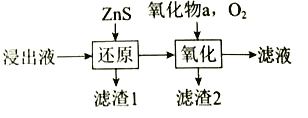
①a可以是______________,加入a的作用是_______________。
②除铁过程中可以控制溶液中![]() 的操作是_______________。
的操作是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三种常见元素结构信息如下表,试根据信息回答有关问题:
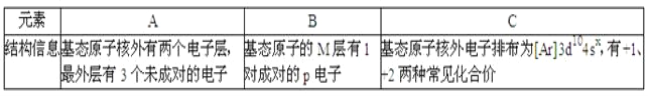
(1)写出B原子的基态电子排布式__;
(2)用氢键表示式写出A的氢化物溶液中存在的氢键__(任写一种);A的氢化物分子结合一个H+形成阳离子后,其键角__(填写“变大”、“变小”、“不变”);
(3)往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,可生成的配合物的化学式为__,简要描述该配合物中化学键的成键情况__;
(4)下列分子结构图中的“●”表示上述相关元素的原子中除去最外层电子的剩余部分,“○”表示氢原子,小黑点“”表示没有形成共价键的最外层电子,短线表示共价键.

在以上分子中,中心原子采用sp3杂化形成化学键是__(填写序号);在②的分子中有__个σ键和__个π键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究含N、S的污染排放物并妥善处理和利用,意义重大。回答下列问题:
(1)![]() 尾气先用氨水吸收生成
尾气先用氨水吸收生成![]() ,反应为
,反应为![]()
![]() ,再将
,再将![]() 氧化为
氧化为![]() ,最终实现副产氮肥,变废为宝。两种氧化方案如下:
,最终实现副产氮肥,变废为宝。两种氧化方案如下:
方案1:![]()
方案2:![]() ,
,
![]() 。
。
30℃时,分别向两相同容器中加入100L 0.4![]() 溶液,加入足量相同物质的量的氧化剂,测得
溶液,加入足量相同物质的量的氧化剂,测得![]() 的氧化率X(%)随时间的变化如图所示。
的氧化率X(%)随时间的变化如图所示。
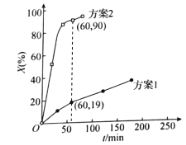
据上述图像判断,氧化![]() 为
为![]() 的能力是
的能力是![]() ____(填“大于”或“小于”)
____(填“大于”或“小于”)![]() ,可能的原因是___。
,可能的原因是___。
②60min内测得方案2体系中用![]() 表示的反应速率为__
表示的反应速率为__![]() 。
。
(2)方案2中,![]() 会被氧化成
会被氧化成![]() ,而
,而![]() 不能结合氧气(活化分子氧),为了保持钴氨溶液的吸收能力,需添加
不能结合氧气(活化分子氧),为了保持钴氨溶液的吸收能力,需添加![]() 将
将![]() 还原成
还原成![]() ,同时生成
,同时生成![]() 。反应历程如下:
。反应历程如下:
i:![]()
ii:_____
iii:![]()
iv:![]()
则第ii步反应为____。
(3)利用废气中的![]() 将(2)中生成的
将(2)中生成的![]() 还原成
还原成![]() ,以实现
,以实现![]() 再生。反应的离子方程式为____。
再生。反应的离子方程式为____。
![]() 再生后,实现了利用方案2完整地氧化
再生后,实现了利用方案2完整地氧化![]() 为
为![]() 的过程,则整个过程中起催化剂作用的是___(填离子符号)。
的过程,则整个过程中起催化剂作用的是___(填离子符号)。
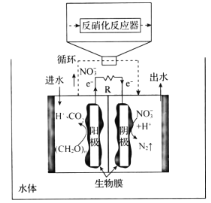
(4)关于微生物电化学系统处理含氮废水的研究快速发展,如图是一种新型的浸没式双极室脱盐-反硝化电池。由阳极室和阴极室组成,中间由质子交换膜隔开,阳极室中的有机物则被微生物氧化降解产生电子和质子,其中的![]() 通过泵循环至阴极室,经过反硝化反应器中反硝化菌的作用被还原成
通过泵循环至阴极室,经过反硝化反应器中反硝化菌的作用被还原成![]() 。
。
①微生物电化学系统处理有机含氮废水的优点是____。
②写出负极发生反应的电极反应式:_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com