
已知反应X+Y═M+N为放热反应,对该反应的说法正确是( )
A. X的能量一定高于M
B. Y的能量一定高于N
C. X和Y的总能量一定高于M和N的总能量
D. 因为该反应为放热反应,故不必加热就可发生
科目:高中化学 来源: 题型:
反应:L(s)+aG(g)
 bR(g)达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡时混合气体中G的体积分数。据此可判断( )
bR(g)达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡时混合气体中G的体积分数。据此可判断( )

①上述反应是放热反应②上述反应是吸热反应③a>b④a<b
A.①③ B.①④ C.②③ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于热化学反应的描述中正确的是( )
A.HCl和NaOH反应的中和热ΔH=-57.3 kJ/mol,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3)kJ/mol
B.碳与二氧化碳反应既是吸热反应,又是化合反应
C.热化学方程式中化学计量系数可表示分子个数
D.1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
查看答案和解析>>
科目:高中化学 来源: 题型:
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池。已知H2(g)、CO(g)和CH3OH(l)的燃烧热ΔH分别为-285.8 kJ·mol-1、-283.0 kJ·mol-1和-726.5 kJ·mol-1。请回答下列问题:
(1)用太阳能分解10 mol水消耗的能量是________kJ;
(2)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为
查看答案和解析>>
科目:高中化学 来源: 题型:
水溶液中能大量共存的一组离子是( )
A. K+、NH4+、OH﹣、SO42﹣ B. H+、Fe2+、SO42﹣、ClO﹣
C. Na+、Ca2+、Cl﹣、CO32﹣ D. K+、Ca2+、Cl﹣、NO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W均为短周期元素,它们在元素周期表中相对位置如图所示,若Z原子的最外层电子数是第一层电子数的3倍,下列说法正确的是( )
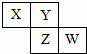
A. Z单质与氢气反应较Y剧烈
B. 最高价氧化物对应水化物酸性W比Z强
C. X单质氧化性强于Y单质
D. X与W的原子核外电子数相差9
查看答案和解析>>
科目:高中化学 来源: 题型:
)某班学生分成甲,乙两小组分别探究硫,氮及其化合物的性质:
(一)甲组同学用图1装置来探究浓硫酸与木炭粉加热反应并验证反应所产生的各种产物.
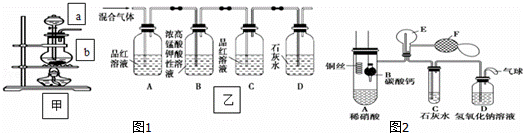
(1)装置甲中盛放浓硫酸的仪器a名称是 ,装置甲中仪器b中发生反应的化学方程式为
(2)实验中可观察到装置乙中,A瓶的溶液褪色,C瓶的溶液不褪色.
A瓶溶液的作用是 ,
D瓶溶液的现象是 .
(二)乙组同学用图2装置来证明铜与稀硝酸反应产生一氧化氮,B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球.(1)实验时,先将B装置下移,使碳酸钙与稀硝酸接触产生气体,当C处产生白色沉淀时,立刻将B装置上提,使之与稀硝酸分离.该组学生设计此步操作的目的是 .
(2)装置E中开始时出现浅红棕色气体,用F向E中鼓入空气后,可观察到烧瓶E内气体颜色加深,产生上述现象的原因是 .
(3)一段时间后,C中白色沉淀溶解,其原因是
(4)装置D的作用是
查看答案和解析>>
科目:高中化学 来源: 题型:
硫元素有多种化合价,可形成多种化合物.
(1)常温下用1mol•L﹣1200mLNaOH溶液恰好完全吸收0.1molSO2气体,此反应的离子方程式为 ,请用离子方程式表示该溶液PH>7的原因 H ,该溶液放置于空气中一段时间后,溶液的PH (填“增大”“减小”或“不变”)
(2)SO2能使酸性高锰酸钾溶液褪色,该反应的离子方程式为 ,实验室通常选择 (选填“稀盐酸”、“稀硫酸”)对高锰酸钾溶液进行酸化.
(3)课本中选用Na2S2O3与稀硫酸的反应来研究物质的温度对化学反应速率的影响.选用Na2S2O3来比较化学反应速率快慢的原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值,则下列叙述正确的是( )
|
| A. | 常温下,4.48L N2和O2的混合气体中所含原子数为0.4NA |
|
| B. | 常温下,1.0L1.0mol•L﹣1 NaAlO2溶液中含有的氧原子数为2NA |
|
| C. | 7.8g Na2S和Na2O2的混合物中含有的阴离子数等于0.1NA |
|
| D. | 0.1mol Fe参加氧化还原反应,转移的电子数目一定是0.2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com