


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源:2012-2013学年安徽省蚌埠市第一次教学质量检查考试化学试卷(解析版) 题型:选择题
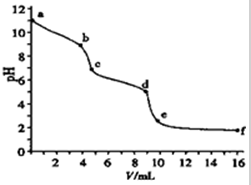
在实验室中我们用标准浓度的盐酸滴定未知浓度的碳酸钠,通过pH传感器绘制了如下图像。通过对图像的分析,你认为下列推断正确的是

A.碳酸钠的浓度为0.001mol·L-1
B.在pH=7时溶液中[Na-]=[Cl-]
C.在pH=6时:[Na+]>[HCO3-]>[CO32-]
D.c→d发生的主要离子反应:CO32-+H+=HCO3-
查看答案和解析>>
科目:高中化学 来源:2012年鲁科版高中化学选修6 3.2 物质中某组分含量的测定练习卷(解析版) 题型:填空题
有一未知浓度的食醋,某学生为测定CH3COOH的浓度在实验室中进行如下实验。请完成下列填空:
(1)配制100 mL 0.10 mol·L-1NaOH标准溶液。
①主要操作步骤:计算→称量→溶解→(冷却后)________→洗涤(并将洗涤液移入容量瓶)→________→________→将配制好的溶液倒入试剂瓶中,贴上标签。
②称量0.4 g氢氧化钠固体所需仪器有:天平(带砝码、镊子)、________、________。
(2)取20.00 mL待测食醋放入锥形瓶中,由于食醋颜色较深,我们先____________________________________,并滴加2~3滴________做指示剂,用自己配制的标准NaOH溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
|
实验 编号 |
NaOH溶液的浓度/(mol·L-1) |
滴定完成时,NaOH溶液滴入的体积/mL |
待测CH3COOH溶液的体积/mL |
|
1 |
0.10 |
22.62 |
20.00 |
|
2 |
0.10 |
22.72 |
20.00 |
|
3 |
0.10 |
22.80 |
20.00 |
①滴定达到终点的标志是
________________________________________________________________________。
②根据上述数据,可计算出该食醋中CH3COOH的浓度约为________(保留两位有效数字)。
③在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有________。
A.滴定终点时俯视读数
B.移液管水洗后未用食醋溶液润洗
C.锥形瓶水洗后未干燥
D.称量前NaOH固体中混有Na2CO3固体
E.配制好的NaOH标准溶液保存不当,部分与空气中的CO2反应生成了Na2CO3
F.碱式滴定管尖嘴部分有气泡,滴定后消失
查看答案和解析>>
科目:高中化学 来源: 题型:单选题

查看答案和解析>>
科目:高中化学 来源: 题型:
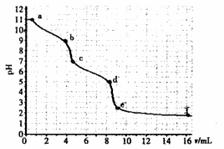
在实验室中我们用标准浓度的盐酸滴定未知浓度的碳酸钠,通过pH传感器绘制了如下图像。通过对图像的分析,你认为下列推断正确的是
A.碳酸钠的浓度为0.001mol·L-1
B.在pH=7时溶液中[Na-]=[Cl-]
C.在pH=6时:[Na+]>[HCO3-]>[CO32-]
D.c→d发生的主要离子反应:CO32-+H+=HCO3-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com