
【题目】下列有关第ⅦA族元素的单质和化合物性质说法正确的是
A. 还原性:HF>HCl>HBr>HI B. 稳定性:HF<HCl<HBr<HI
C. 从F2到I2,颜色逐渐加深 D. 与氢气化合由易到难:I2>Br2> Cl2>F2
科目:高中化学 来源:2017届江苏省南通市高三高考全真模拟(六)化学试卷(解析版) 题型:简答题
银精矿(其化学成分有:Ag、Zn、Cu、Pb、S及SiO2等)从其中提取银及铜和铅的工艺流程如下:
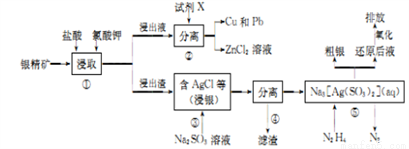
(1)步骤①当盐酸的浓度和KClO3的量一定时,为提高浸取率可采取的措施是___________(举两项)。
(2)步骤②试剂X为____,步骤④滤渣中除含单质硫外,还含有的成分有______。
(3)步骤③反应的化学方程式为____________。
(4)步骤⑤反应的离子方程式为___________。
(5)“还原后液”经氧化后,排放液中溶质的主要成分为_______。
(6)“粗银”(含Ag、Cu、Zn、Au)可用立式电解槽点解精炼,纯银作阴极,电解液采用含Ag60-150g·L-1的硝酸银溶液,可加入含HNO32-8g·L-1的溶液来提高电解液的导电率。
①电解产生的阳极泥中所含金属为______。
②硝酸浓度不能过大,其原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y为短周期元素,X位于IA族,X与Y可形成化合物X2Y,下列说法正确的是( )
A.X的原子半径一定大于Y的原子半径
B.X与Y的简单离子不可能具有相同的电子层结构
C.两元素形成的化合物中,原子个数比不可能为1 :1
D.X2Y可能是离子化合物,也可能是共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是
A.构成原电池的正极和负极的材料必须是两种金属
B.由铜、锌作电极与硫酸铜溶液组成的原电池中铜是负极
C.马口铁(镀锡铁)破损时与电解质溶液接触时锡先被腐蚀
D.铜锌原电池工作时,若有13 g锌被溶解,电路中就有0.4 mol电子通过
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列递变规律不正确的是
A. Na、Mg、Al还原性依次减弱 B. Cl2、Br2、I2氧化性依次增强
C. Be、Mg、Ca与盐酸反应越来越剧烈 D. P、S、Cl最高正价依次升高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为检验某卤代烃中的卤元素,进行如下操作,正确的顺序是( )
①加热 ②加入 AgNO3溶液 ③取少量该卤化物 ④加入足量稀硝酸酸化 ⑤加入NaOH溶液 ⑥冷却
A.③①⑤⑥②④ B.③⑤①⑥④②
C.③②①⑥④⑤ D.③⑤①⑥②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】共价键、离子键和分子间作用力是构成物质的粒子间的不同作用方式。下列物质中,只含有上述一种作用方式的是( )
A.干冰 B.氯化钠
C.氢氧化钠 D.碘
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表和元素周期律对于其他与化学相关的科学技术有指导作用。下列说法中不正确的是( )
A. 在元素周期表左下方区域的金属元素中寻找半导体材料
B. 利用元素周期表中氟、氯、硫、磷附近的元素研制新型农药
C. 在过渡金属中寻找催化剂和耐高温、耐腐蚀的合金材料
D. 在周期表一定区域内寻找元素、发现物质的新用途是一种相当有效的方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列做法不利于金属防护的是( )
A.菜刀切菜后不洗净就放回刀架 B.将钢铁制成不锈钢
C.在铁塔的表面喷上一层油漆 D.埋在地下的钢管与锌块连接
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com