
下列陈述中,Ⅰ、Ⅱ都正确且两者间具有因果关系的一组是( )
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | FeCl3溶液能腐蚀Cu | Fe的金属性强于Cu |
| B | Na2O2使酚酞溶液变红 | Na2O2使品红溶液褪色 |
| C | Cl2可部分与水反应 | 用排饱和食盐水法收集Cl2 |
| D | 浓H2SO4可干燥NO和SO2 | NO和SO2还原性都弱 |
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:
Al、Fe、Cu都是重要的金属元素.下列说法正确的是( )
|
| A. | 三者对应的氧化物均为碱性氧化物 |
|
| B. | 三者的单质放置在空气中均只生成氧化物 |
|
| C. | 制备AlCl3、FeCl3、CuCl2均不能采用将溶液直接蒸干的方法 |
|
| D. | 电解AlCl3、FeCl3、CuCl2的混合溶液时阴极上依次析出Cu、Fe、Al |
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化还原反应在生产和生活中使用非常广泛。
一个体重50 kg的健康人含铁2 g,这2 g铁在人体中不是以金属单质的形式存在,而是以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收。
(1)以下为常见的铁元素的几种微粒,其中既有氧化性又有还原性的是__________。
A. Fe B. Fe2+ C. Fe3+
(2)工业盐的主要成分是NaNO2,以前有许多起因误食NaNO2而中毒的事件,其原因是NaNO2把人体内的Fe2+转化为Fe3+而失去与O2结合的能力,这说明NaNO2具有________性。下列也能实现这种转化的物质是________。
A. H2O B. O2 C. FeCl3 D.铁粉
(3)工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有________性。
(4)NaHSO4在水中的电离方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述错误的是( )
A.用金属钠可区分乙醇和乙醚
B.用溴水可区分己烷和3--己烯
C.用水可区分苯和溴苯
D.用新制的氢氧化铜悬浊液可区分甲酸甲酯和乙醛
查看答案和解析>>
科目:高中化学 来源: 题型:
黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:
S(s)+2KNO3(s)+3C(s)==K2S(s)+N2(g)+3CO2(g) ΔH= x kJ·mol-1
已知:碳的燃烧热 ΔH1= a kJ·mol-1
S(s)+2K(s)==K2S(s) ΔH2= b kJ·mol
2K(s)+N2(g)+3O2(g)==2KNO3 (s) ΔH3= c kJ·mol-1
则x为( )
A.3a+b-c B.c +3a-b C.a+b-c D.c+a-b
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室中,可利用碳酸氢钠、氯化钠、氯化铵等物质溶解度的差异,通过饱和食盐水、氨和二氧化碳反应,获得碳酸氢钠晶体,反应原理可用如下化学方程式表示:NH3 + CO2 + NaCl + H2O == NH4Cl + NaHCO3↓,依据此原理,欲制得碳酸钠晶体,某校学生设计了如下实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和:
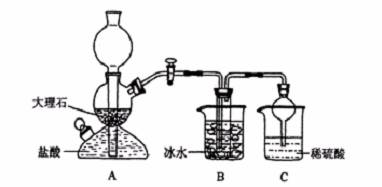
(1)A装置中所发生反应的离子方程式为: 。
C装置中稀硫酸的作用为: 。
(2)下表中所列出的是相关物质在不同温度下的溶解度数据(g/100g水)
| 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
参照表中数据,请分析B装置中使用冰水是因为 。
(3)该校学生在检查完此套装置气密性后进行实验,结果没有得到碳酸氢钠晶体,指导教师指出应在 装置之间(填写字母)连接一个盛有 的洗气装置,其作用是 。
(4)若该校学生进行实验时,所用饱和食盐水中含NaCl的质量为5.85g,实验后得到干燥的NaHCO3晶体的质量为5.04g,则NaHCO3的产率为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
用如图所示装置探究碳酸和苯酚的酸性强弱,下列叙述不正确的是(部分夹持仪器省略)( )
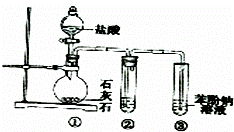
A.②中试剂为饱和NaHCO3溶液
B.打开分液漏斗旋塞,①中产生无色气泡,③中出现白色浑浊
C.苯酚的酸性弱于碳酸
D.③中发生反应的化学方程式是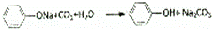
查看答案和解析>>
科目:高中化学 来源: 题型:
下表为各物质中所含有的少量杂质以及除去这些杂质应选用的试剂或操作方法。
| 序号 | 物质 | 杂质 | 除杂质应选用的试剂或操作方法 |
| ① | KNO3溶液 | KOH | 加入FeCl3溶液,并过滤 |
| ② | FeSO4溶液 | CuSO4 | 加入过量铁粉,并过滤 |
| ③ | H2 | CO2 | 通过盛有NaOH溶液的洗气瓶,再通过盛有浓硫酸的洗气瓶 |
| ④ | NaNO3 | CaCO3 | 溶解、过滤、蒸发 |
正确的一组是( )
A.①②③④ B.③④ C.②③④ D.①②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com