
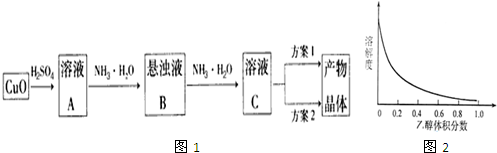
分析 (1)①根据加热蒸发操作所用的仪器分析判断,加热蒸发需要蒸发皿、酒精灯、玻璃棒等仪器;
②氨气具有挥发性,物质的电离是吸热过程,加热促进使反应[Cu(NH3)4]2+?Cu2++4NH3平衡往右移动,且铜离子是弱碱离子易水解,所以导致产生杂质;
(2)①根据图象分析,[Cu(NH3)4]SO4•H2O在乙醇•水混合溶剂中的溶解度随乙醇体积分数的增大而减小,为了减少[Cu(NH3)4]SO4•H2O的损失,应加入乙醇,降低其溶解度,然后过滤得晶体;
②根据图象[Cu(NH3)4]SO4•H2O在乙醇•水混合溶剂中的溶解度随乙醇体积分数的变化曲线示意图及实验目的分析;
③含结晶水的晶体加热易失水,不宜采用加热干燥的方法.
解答 解:(1)①蒸发时,需要使用蒸发皿;需要铁架台和铁圈支撑蒸发皿;需要玻璃棒进行搅拌,以防止液体受热不均匀,造成液体飞溅;需要酒精灯进行加热;坩埚钳用于夹持蒸发皿,
故答案为:蒸发皿;玻璃棒;
②该方案存在明显缺陷,因为得到的产物晶体中往往含有Cu(OH)2或Cu2(OH)2SO4杂质,产生该杂质的原因是加热蒸发过程中NH3挥发,使反应[Cu(NH3)4]2+?Cu2++4NH3平衡向右移动,且Cu2+发生水解.
故答案为:Cu(OH)2或Cu2(OH)2SO4;加热蒸发时氨溶解度降低逸出,使反应[Cu(NH3)4]2+?Cu2++4NH3平衡往右移动,且Cu2+发生水解;
(2)①根据Cu(NH3)4]SO4•H2O在乙醇•水混合溶剂中的溶解度随乙醇体积分数的变化曲线示意图知,随着乙醇体积分数的增大,Cu(NH3)4]SO4•H2O的溶解度降低,为了得到Cu(NH3)4]SO4•H2O,应向溶液C中加入适量乙醇,然后进行过滤,
故答案为:乙醇;过滤;
②根据Cu(NH3)4]SO4•H2O在乙醇•水混合溶剂中的溶解度随乙醇体积分数的变化曲线示意图知,随着乙醇体积分数的增大,Cu(NH3)4]SO4•H2O的溶解度降低,为了减少Cu(NH3)4]SO4•H2O的损失,应降低Cu(NH3)4]SO4•H2O的溶解度,所以应选用乙醇和水的混合液;
故答案为:C;
③[Cu(NH3)4]SO4•H2O在加热条件下能分解生成水和氨气,从而得不到纯净的[Cu(NH3)4]SO4 •H2O,所以不宜采用加热干燥的方法,
故答案为:加热易使[Cu(NH3)4]SO4•H2O 分解(失去水或失去氨气).
点评 本题考查一水硫酸四氨合铜合成的方案设计与评价,题目难度中等,注意把握实验操作原理,把握题给信息,掌握实验操作方法,学习中注意积累.


科目:高中化学 来源: 题型:填空题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
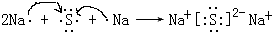 .
. ,该化合物是由极性(填“极性”“非极性”)键形成的.
,该化合物是由极性(填“极性”“非极性”)键形成的.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 438.6 kJ/mol | B. | 241.8 kJ/mol | C. | 285.8kJ/mol | D. | -285.8 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 仪器及装置图 |  | 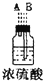 | 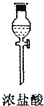 | 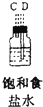 | 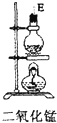 | 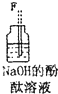 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
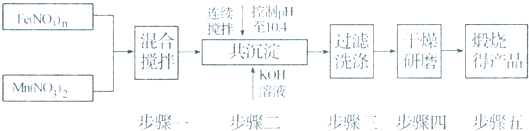
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等.实验室制备氨基甲酸铵(NH2COONH4)的反应如下:
氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用做肥料、灭火剂、洗涤剂等.实验室制备氨基甲酸铵(NH2COONH4)的反应如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 已知某可逆反应:mA(g)+nB(g)?pC(g)△H=Q kJ•mol-1,在密闭容器中进行,如图表示在不同时间t、温度T和压强P与生成物C的百分含量的关系曲线,下列判断正确的是( )
已知某可逆反应:mA(g)+nB(g)?pC(g)△H=Q kJ•mol-1,在密闭容器中进行,如图表示在不同时间t、温度T和压强P与生成物C的百分含量的关系曲线,下列判断正确的是( )| A. | T1<T2 P1>P2 m+n<P Q<0 | B. | T1>T2 P1<P2 m+n>P Q>0 | ||
| C. | T1<T2 P1<P2 m+n<P Q>0 | D. | T1>T2 P1<P2 m+n>P Q<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | BaSO4?Ba2++SO42- | B. | 2H2O?H3O++OH- | ||
| C. | NaHCO3═Na++H++CO32- | D. | NH3•H2O═NH4++OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com