
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2016-2017学年陕西省西安市高二下学期第一次教学检测化学试卷(解析版) 题型:实验题
溴苯是一种常用的化工原料。实验室制备溴苯的实验步骤如下:

步骤1:在a中加入15 mL苯和少量铁屑,再将b中4.0 mL液溴慢慢加入到a中,充分反应。,有___________(填现象)产生; 将b中的液溴慢慢加入到a中,而不能快速加入的原因是___________,继续滴加液溴滴完。装置d的作用是___________________;
步骤2:向a中加入10 mL水,然后________(填操作名称)除去未反应的铁屑。
步骤3:滤液依次用10 mL水、8 mL 10%的NaOH溶液、10 mL水洗涤,分液得粗溴苯。NaOH溶液洗涤的作用是____________;
步骤4:向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤即得粗产品。加入氯化钙的目的是______________;
已知苯、溴苯的有关物理性质如上表:
苯 | 溴 | 溴苯 | |
密度/g·cm-3 | 0.88 | 3.10 | 1.50 |
沸点/℃ | 80 | 59 | 156 |
在水中的溶解度 | 微溶 | 微溶 | 微溶 |
(1)实验装置中,仪器c的名称为_____,作用是冷凝回流,回流的主要物质有___________________(填化学式)
(2)步骤4得到的粗产品中还含有杂质苯,,则要进一步提纯粗产品,还必须进行的实验操作名称是__________________。
查看答案和解析>>
科目:高中化学 来源:2017届湖北省新联考高三第四次联考理科综合化学试卷(解析版) 题型:选择题
用电解乙二醛制备乙二酸(HOOC-COOH)的装置如图所示,通电后,b电极上产生的氯气将乙二醛氧化为乙二酸,下列说法正确的是

A. b接电源的负极,发生还原反应
B. a极上的电极反应为:2H2O-4e-=O2↑+4H+
C. 盐酸的作用是提供CI-和增强导电性
D. 电路上每转移1mol电子产生45g乙二酸
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏省高二下学期第一次月考化学试卷(解析版) 题型:填空题
X、Y、Z、W是元素周期表前四周期中常见的元素,其相关信息如下表:
元素 | 相关信息 |
X | X原子基态时最外层电子数是其内层电子数的2倍 |
Y | Y原子基态2p原子轨道上有3镉未成对的电子 |
Z | Z的基态原子最外曾电子排布式为:nsnnpn+2 |
W | W的原子序数为24 |
(1)W的元素符号是______;基态W原子的电子排布式为______
(2)Z元素属于元素周期表中____区元素,其最外层电子排布图为______。
(3)X、Y、Z三种元素第一电离能由大到小的顺序是_____(用元素符号表示)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏省高二下学期第一次月考化学试卷(解析版) 题型:选择题
某元素价电子构型3d54S2,是该元素是
A. Fe B. Co C. Mn D. Ni
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏省高二下学期第一次月考化学试卷(解析版) 题型:选择题
向ZnSO4溶液中加入Na2S溶液时,得到白色沉淀,然后向白色沉淀中滴加CuSO4溶液,发现沉淀变为黑色,则下列说法不正确的是
A.白色沉淀为ZnS,黑色沉淀为CuS
B.上述现象说明ZnS的Ksp小于CuS的Ksp
C.利用该原理可实现一种沉淀转化为更难溶的沉淀
D.该过程破坏了ZnS的溶解平衡
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏省高二下学期第一次月考化学试卷(解析版) 题型:选择题
对可逆反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g),下列叙述正确的是( )
4NO(g)+6H2O(g),下列叙述正确的是( )
A.达到化学平衡时,4v正(O2)=5v逆(NO)
B.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态
C.达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大
D.化学反应速率关系是:2v正(NH3)=3v正(H2O)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高一3月月考化学试卷(解析版) 题型:填空题
如图所示,把试管放入盛有25 ℃饱和石灰水的烧杯中,试管中开始放入几小块镁片,再滴入5 mL稀盐酸,试完成下列问题。

(1)实验中观察到的现象是__________________。
(2)产生上述现象的原因是__________________。
(3)写出有关反应的离子方程式__________________
(4)由实验推知,MgCl2溶液和H2的总能量_______________
(填“大于”“小于”或“等于”)镁片和盐酸的总能量。
(5)写出下列物质的电子式:Mg HCl NH4+ NaOH Na2O2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一下学期第一次月考化学试卷(解析版) 题型:填空题
(14分)铜是与人类关系非常密切的有色金属。已知:常温下,在溶液中Cu2+稳定,Cu+易在酸性条件下发生反应:2Cu+ =Cu2++Cu。大多数+1价铜的化合物是难溶物,如:Cu2O、CuI、CuCl、CuH等。
(1)在新制Cu(OH)2悬浊液中滴入葡萄糖溶液,加热生成不溶物的颜色为: ,某同学实验时却有黑色物质出现,这种黑色物质的化学式为: 。
(2)在CuCl2溶液中逐滴加入过量KI溶液可能发生:
a.2Cu2++4I- =2CuI↓(白色)+I2
b.2Cu2++2Cl-+2I- =2CuCl↓(白色)+I2。
为顺利观察到白色沉淀可以加入的最佳试剂是 。
A.SO2 B.苯 C.NaOH溶液 D.乙醇
(3)一定条件下,在CuSO4中加入NH5反应生成氢化亚铜(CuH)。
①已知NH5是离子晶体且所有原子都达到稀有气体的稳定结构,请写出NH5的电子式: 。
②写出CuH在过量稀盐酸中有气体生成的离子方程式 。
③将CuH溶解在适量的稀硝酸中, 完成下列化学方程式
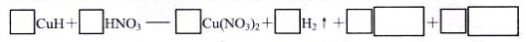
(4)常温下,向0.20 mol • L-1硫酸铜溶液中加入氢氧化钠溶液,生成浅蓝色氢氧化铜沉淀,当溶液的pH = 6时,c(Cu2+)=________________mol.L‑1。
[已知: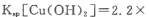
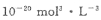 ]
]
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com