
【题目】(1)0.3molNH3分子中所含氢原子数与___个H2O分子中所含氢原子数相等。
(2)含0.4molAl3+的Al2(SO4)3中所含的SO42-的物质的量是___。
(3)2.3gNa中含___mole-,在跟足量水反应中失去___mole-。
(4)如果ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是(设NA为阿伏加德罗常数)______。
【答案】2.709×1023 0.6 mol 1.1 0.1 ![]() L
L
【解析】
(1)0.3molNH3中含有H原子0.9mol,1个水分子中含有2个H原子,则水分子中需要含有相同数目的H原子数需要0.9mol/2=0.45molH2O,则水分子的个数为0.45mol×6.02×1023mol-1= 2.709×1023;
(2) Al2(SO4)3中Al3+和SO42-的物质的量的比例为2:3,Al3+含有0.4mol,则SO42-含有0.4mol÷2×3=0.6mol;
(3)Na为11号元素,1molNa原子中含有11mol电子,2.3gNa为0.1molNa,则含有0.1×11 mol =1.1mol电子。2Na+2H2O=2NaOH+H2↑,Na原子变成Na+,1molNa失去1mol电子,则0.1molNa与水反应失去0.1mol电子;
(3)利用连等式![]() ,ag某气体中含有的分子数为b,有
,ag某气体中含有的分子数为b,有![]() ,cg该气体在标准状况下的体积V,有
,cg该气体在标准状况下的体积V,有![]() ,VM=22.4L/mol,求出V需要知道M。根据
,VM=22.4L/mol,求出V需要知道M。根据![]() ,得
,得![]() ,带入
,带入![]() ,得V=
,得V=![]() L。
L。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】焦亚硫酸钠(Na2S2O5)常用作食品漂白剂。其制备工艺流程如图:

已知:反应Ⅱ包含2NaHSO3![]() Na2S2O5+H2O等多步反应。
Na2S2O5+H2O等多步反应。
(1)实验室制取氨气的化学方程式:______。
(2)反应I的化学方程式为______。
(3)“灼烧”时发生反应的化学方程式:______。
(4)已知Na2S2O5与稀硫酸反应放出SO2,其离子方程式为______。
(5)副产品X的化学式是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对水样中溶质M的分解速率影响因素进行研究。在相同温度下,M的物质的量浓度(mol·L-1)随时间(min)变化的有关实验数据见下表。
时间 水样 | 0 | 5 | 10 | 15 | 20 | 25 |
Ⅰ(pH=2) | 0.40 | 0.28 | 0.19 | 0.13 | 0.10 | 0.09 |
Ⅱ(pH=4) | 0.40 | 0.31 | 0.24 | 0.20 | 0.18 | 0.16 |
Ⅲ(pH=4) | 0.20 | 0.15 | 0.12 | 0.09 | 0.07 | 0.05 |
Ⅳ(pH=4,含Cu2+) | 0.20 | 0.09 | 0.05 | 0.03 | 0.01 | 0 |
下列说法不正确的是
A. 在0~20min内,I中M的分解速率为0.015 mol·L-1·min-1
p>B. 水样酸性越强,M的分解速率越快C. 在0~25min内,III中M的分解百分率比II大
D. 由于Cu2+存在,IV中M的分解速率比I快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,甲容器中充满![]() ,乙容器中充满
,乙容器中充满![]() ,下列叙述不正确的是()
,下列叙述不正确的是()
A. 若两种气体体积相等,甲、乙两容器中气体的密度之比为35:37
B. 若两种气体体积相等,甲、乙两容器中气体分子数之比为35:37
C. 若两种气体质量相等,甲、乙两容器中气体所含质子数之比为37:35
D. 若两种气体体积相等,甲、乙两容器中气体所含中子数之比为9:10
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:


(1)从氯化钾溶液中得到氯化钾固体,选择装置________(填代表装置图的字母,下同);除去自来水中 的Cl-等杂质,选择装置________________。
(2)从碘水中分离出I2,选择装置________,该分离方法的名称为________________。
(3)装置A中①的名称是________,进水的方向是从________(填“上”或“下”)口进水。装置B在分液时为使液体顺利下滴,应进行的具体操作是__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法不正确的是( )
A.  水合铜离子的模型如图所示,1个水合铜离子中有4个配位键
水合铜离子的模型如图所示,1个水合铜离子中有4个配位键
B.  CaF2晶体的晶胞如图所示,每个CaF2晶胞平均占有4个Ca2+
CaF2晶体的晶胞如图所示,每个CaF2晶胞平均占有4个Ca2+
C.  H原子的电子云图如图所示,H原子核外的大多数电子在原子核附近运动
H原子的电子云图如图所示,H原子核外的大多数电子在原子核附近运动
D.  金属Cu中Cu原子堆积模型如图所示,该金属晶体为最密堆积,每个Cu原子的配位数均为12
金属Cu中Cu原子堆积模型如图所示,该金属晶体为最密堆积,每个Cu原子的配位数均为12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列装置进行相应实验,能达到实验目的的是

图1 图2 图3 图4
A. 图1所示装置制取并收集氨气
B. 图2所示装置用于制备并收集NO气体
C. 图3所示装置用于除去碳酸氢钠固体中的少量碳酸钠
D. 图4所示装置用于Na2CO3和稀H2SO4反应制取少量的CO2气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用化学原理对工厂排放的废水、废渣等进行有效检测与合理处理。
某工厂对制革工业污泥中Cr元素的回收与再利用工艺如图(硫酸浸取液中金属离子主要是Cr3+,其次是Fe3+、Fe2+、Al3+、Ca2+、Mg2+):
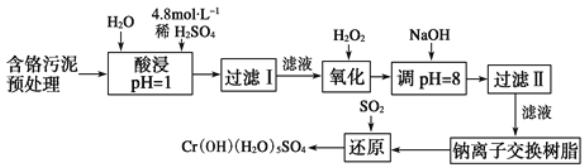
常温下部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cr3+ |
开始沉淀时的pH | 1.9 | 7.0 | - | - | - |
沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8 | 9(>9溶解) |
(1) 酸浸时,为了提高浸取率可采取的措施是____(至少写两条)。
(2)H2O2的作用是_____。
(3)调pH=8是为了除去___(填Fe3+、Fe2+、Al3+、Ca2+、Mg2+)。
(4)钠离子交换树脂的原理为Mn++nNaR→MRn+nNa+,被交换的杂质离子是___(填Fe3+、Fe2+、Al3+、Ca2+、Mg2+)。
(5)已知以下氧化还原反应方程式(未配平):Na2Cr2O7+SO2+H2O=Cr(OH)(H2O)5SO4+Na2SO4;以上反应各物质的配平系数依次为___。每生成1 mol Cr(OH)(H2O)5SO4转移电子的数目为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃,下列各组离子在指定溶液中一定能大量共存的是
A.![]() =1×10-12的溶液:K+、Na+、[Al(OH)4]-、CO32-
=1×10-12的溶液:K+、Na+、[Al(OH)4]-、CO32-
B.能溶解Al2O3的溶液:Na+、K+、HCO3-、NO3-
C.饱和氯水中:Cl-、NO3-、Na+、SO32-
D.能使甲基橙显红色的溶液:K+、Fe2+、Cl-、NO3-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com