
科目: 来源:2015-2016学年宁夏唐徕回民中学高二上10月月考化学卷(解析版) 题型:选择题
下列对化学平衡移动的分析中,不正确的是
①已达平衡的反应C(s)+H2O(g)  CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动
CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动
②已达平衡的反应N2(g)+3H2(g)  2NH3(g),当增大N2的浓度时,平衡向正反应方向移动,N2的转化率一定升高
2NH3(g),当增大N2的浓度时,平衡向正反应方向移动,N2的转化率一定升高
③有气体参加的反应达平衡时,若减小反应器容积时平衡一定向气体体积增大的方向移动
④有气体参加的反应达平衡后,在恒压反应器中充入稀有气体,平衡一定不移动
A. ①④ B. ①②③ C. ②③④ D. ①②③④
查看答案和解析>>
科目: 来源:2015-2016学年宁夏唐徕回民中学高二上10月月考化学卷(解析版) 题型:选择题
在密闭容器中发生下列反应aA(g)  cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
A.A的转化率变大 B.平衡向正反应方向移动
C.D的体积分数变大 D.a < c+d
查看答案和解析>>
科目: 来源:2015-2016学年宁夏唐徕回民中学高二上10月月考化学卷(解析版) 题型:选择题
某体积可变的密闭容器中盛有适量的A和B的混合气体,在一定条件下发生反应,A(g) +3 B(g)  2 C(g)若维持温度和压强不变,达到平衡时,容器的体积为V L。其中C气体的体积占20%,下列推断正确的是
2 C(g)若维持温度和压强不变,达到平衡时,容器的体积为V L。其中C气体的体积占20%,下列推断正确的是
①原混合气体的体积为1.1V L ②原混合气体的体积为1.2V L
③反应达平衡时气体B消耗掉0.1V L ④反应达平衡时气体A消耗掉0.1V L
A.②③ B.②④ C.①③ D.①④
查看答案和解析>>
科目: 来源:2015-2016学年宁夏唐徕回民中学高二上10月月考化学卷(解析版) 题型:选择题
化学平衡移动原理,同样也适用于其他平衡,已知在氨水中存在下列平衡:
NH3+H2O NH3·H2O
NH3·H2O NH4++OH-
NH4++OH-
(1)向氨水中加入MgCl2固体时,平衡向______反应方向移动,现象为____________。
(2)向氨水中通入HCl,平衡向_______反应方向移动,此时溶液中浓度减小的粒子有___________、___________、___________。
(3)向浓氨水中加入少量碱石灰,平衡向______反应方向移动,溶液pH值_________(填“增大”、“减小”或“不变”),现象为______________________。实验室常利用该原理制备氨气,在此过程中碱石灰的另一个作用是_______。
查看答案和解析>>
科目: 来源:2015-2016学年宁夏唐徕回民中学高二上10月月考化学卷(解析版) 题型:填空题
在某一容积为5 L的密闭容器内,加入 0.2 mol的CO和0.2 mol的H2O,在催化剂存在和800℃的条件下加热,发生如下反应:CO(g)+H2O(g)  CO2(g)+H2(g),ΔH<0,反应中CO2的浓度随时间变化情况如右图:
CO2(g)+H2(g),ΔH<0,反应中CO2的浓度随时间变化情况如右图:

(1)根据图中数据计算反应开始至达到平衡时CO的化学反应速率为v(CO)= ;若升高温度,则化学平衡常数K (填“增大”“减小”或“不变”)。
(2)如要一开始加入0.1 mol的CO、0.1 mol的H2O、0.1 mol的CO2和0.1 mol的H2,在相同的条件下,反应CO(g)+H2O(g)  CO2(g)+H2(g)向 (填“正反应”或“逆反应”)方向进行,其依据是 。反应达平衡时,c(H2O)= 。
CO2(g)+H2(g)向 (填“正反应”或“逆反应”)方向进行,其依据是 。反应达平衡时,c(H2O)= 。
查看答案和解析>>
科目: 来源:2015-2016学年宁夏唐徕回民中学高二上10月月考化学卷(解析版) 题型:填空题
能源是人类生存和发展的重要支柱。研究化学反应过程中的能量变化在能源紧缺的今天具有重要的理论意义。已知下列热化学方程式:
① 2H2(g)+O2(g)=2H2O(l) △H =-570kJ/mol ;
② H2(g)+1/2O2(g)=H2O(g) △H =-242kJ/mol ;
③ C(s)+1/2O2(g)=CO (g) △H = —110.5kJ/moL ;
④ C(s)+O2(g)=CO2(g) △H = —393.5kJ/moL;
⑤ CO2(g) +2H2O(g)=2CH4(g) +2 O2(g) △H = +890kJ/moL
回答下列问题:
(1)上述反应中属于燃烧热的热化学方程式的是 。
(2)H2的燃烧热为 。
(3)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然难直接测定,但可通过间接的方法求得。试写出碳与水蒸气反应的热化学方程式_ ;该反应的熵△S 0 (选填“>”、“=”、“<”);已知自由能△HG可推知该反应在______条件下可自发进行。
查看答案和解析>>
科目: 来源:2015-2016学年宁夏唐徕回民中学高二上10月月考化学卷(解析版) 题型:填空题
在一固定容积的密闭容器中,保持一定条件进行以下反应:X(g)+2Y(g) 3Z(g),已知加2molX和3molY达到平衡后,生成amolZ。
3Z(g),已知加2molX和3molY达到平衡后,生成amolZ。
(1)在相同实验条件下,若在同一容器中改为加入4molX和6molY,达到平衡后,Z的物质的量为 mol。
(2)在相同实验条件下,若在同一容器中改为加入3molX和2molY,若要求在反应混合气体中Z体积分数不变,则还需加入Z mol。
(3)在相同实验条件下,若在同一容器中改为加入0.5molX,则需加 molY, mol Z,才能使平衡时Z为0.6amol。
查看答案和解析>>
科目: 来源:2015-2016学年宁夏唐徕回民中学高二上10月月考化学卷(解析版) 题型:计算题
已知CO(g)+ O2(g)=CO2(g),△H =-283 kJ/mol;H2(g)+
O2(g)=CO2(g),△H =-283 kJ/mol;H2(g)+  O2(g)=H2O(l),△H =-285.8 kJ/mol;取CO和H2组成的混合气体0.5mol完全燃烧共放出142.34KJ的热量。若将此0.5mol混合气体充入密闭容器中置于900℃下发生 CO(g)+2 H2(g)
O2(g)=H2O(l),△H =-285.8 kJ/mol;取CO和H2组成的混合气体0.5mol完全燃烧共放出142.34KJ的热量。若将此0.5mol混合气体充入密闭容器中置于900℃下发生 CO(g)+2 H2(g) CH3OH(g),在一定条件下达到平衡。平衡后容器内压强是相同条件下反应前压强的0.8倍,求:
CH3OH(g),在一定条件下达到平衡。平衡后容器内压强是相同条件下反应前压强的0.8倍,求:
(1)反应前混合气体中CO和H2的体积比;
(2)平衡混合气体中CH3OH和H2的物质的量;
(3)达到平衡时CO的转化率。
查看答案和解析>>
科目: 来源:2015-2016学年辽宁省高二上12月月考化学试卷(解析版) 题型:选择题
下列实验中,所采取的分离方法与对应原理都正确的是
选项 | 目的 | 分离方法 | 原理 |
A. | 除去丁醇中的乙醚 | 蒸馏 | 丁醇与乙醚的沸点相差较大 |
B. | 分离乙酸乙酯和乙醇 | 分液 | 乙酸乙酯和乙醇的密度不同 |
C. | 除去KNO3固体中混杂的NaCl | 重结晶 | NaCl在水中的溶解度很大 |
D. | 分离溶于水的碘 | 乙醇萃取 | 碘在乙醇中的溶解度较大 |
查看答案和解析>>
科目: 来源:2015-2016学年辽宁省高二上12月月考化学试卷(解析版) 题型:选择题
下列化合物中,核磁共振氢谱只出现两组峰且峰面积之比为3:2的有
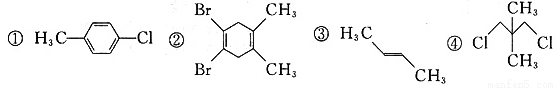
A.0种 B.1种 C.2种 D.3种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com