
科目: 来源:2017届甘肃省高三上第二阶段考化学试卷(解析版) 题型:选择题
某200 mL氯化镁和氯化铝混合液中c(Mg2+)为0.3 mol/L,c(Cl-)为1.2 mol/L。要使Mg2+全部转化为沉淀分离出来,至少需加4 mol/L NaOH溶液的体积为
A.70 mL B.60mL C.80 mL D.128 mL
查看答案和解析>>
科目: 来源:2017届甘肃省高三上第二阶段考化学试卷(解析版) 题型:选择题
某强酸性溶液X中可能含有Fe2+、Al3+、NH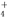 、CO
、CO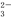 、SO
、SO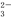 、SO
、SO 、Cl-中的若干种,现取X溶液进行连续实验,实验过程及产物如下:
、Cl-中的若干种,现取X溶液进行连续实验,实验过程及产物如下:

下列说法正确的是
A.气体A是NO2
B.X中肯定存在Fe2+、Al3+、NH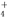 、SO
、SO
C.溶液E和气体F不能发生化学反应
D.X中不能确定的离子是Al3+和Cl-
查看答案和解析>>
科目: 来源:2017届甘肃省高三上第二阶段考化学试卷(解析版) 题型:选择题
向混合溶液甲中缓慢滴加溶液乙,反应生成沉淀的质量如图所示,其中可能符合图象的一组是
甲 | 乙 |
| |
A. | NH4NO3、Al(NO3)3、Fe(NO3)3、HCl | NaOH | |
B. | Na2CO3、NH4HCO3、Na2SO4 | Ba(OH)2 | |
C. | AlCl3、Mg(NO3)2、HNO3 | NaOH | |
D. | NaAlO2、NH3·H2O、NaOH | H2SO4 |
查看答案和解析>>
科目: 来源:2017届甘肃省高三上第二阶段考化学试卷(解析版) 题型:选择题
向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示。则下列离子组在对应的溶 液中,一定能大量共存的是
液中,一定能大量共存的是
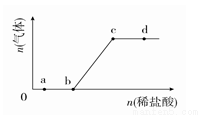
A.b点对应的溶液中:Al3+、Fe3+、MnO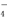 、Cl-
、Cl-
B.a点对应的溶液中:Na+、OH-、SO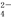 、NO
、NO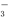
C.d点对应的溶液中:F-、NO 、Fe2+、Na+
、Fe2+、Na+
D.c点对应的溶液中:Na+、Ca2+、NO 、Cl-
、Cl-
查看答案和解析>>
科目: 来源:2017届甘肃省高三上第二阶段考化学试卷(解析版) 题型:选择题
为增强铝的耐腐蚀性,现以铅蓄电池为外电源,以Al作阳极、Pb作阴极,电解稀硫酸,使铝表面的氧化膜增厚。反应原理如下:
电池:Pb(s)+PbO2(s)+2H2SO4(aq)=2PbSO4(s)+2H2O
电解池:2Al+3H2O Al2O3+3H2↑ 电解过程中,以下判断正确的是
Al2O3+3H2↑ 电解过程中,以下判断正确的是
电池 | 电解池 | |
A. | H+移向Pb电极 | H+移向Pb电极 |
B. | 每消耗3 mol Pb | 生成2 mol Al2O3 |
C. | 正极:PbO2+4H++2e-===Pb2++2H2O | 阳极:2Al+3H2O-6e-===Al2O3+6H+ |
D. |
|
|
查看答案和解析>>
科目: 来源:2017届甘肃省高三上第二阶段考化学试卷(解析版) 题型:选择题
工业纯碱中常含有少量的NaCl杂质,某化学兴趣小组取m g纯碱样品与足量稀盐酸充分反应,加热、蒸干、灼烧,得ng固体。则该样品中纯碱的质量分数为( )
A.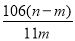 ×100% B.
×100% B.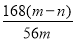 ×100% C.
×100% C.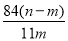 ×100% D.
×100% D.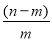 ×100%
×100%
查看答案和解析>>
科目: 来源:2017届甘肃省高三上第二阶段考化学试卷(解析版) 题型:推断题
下图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物。

已知:①G为红棕色固体,能发生反应C+G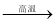 B+H,该反应会放出
B+H,该反应会放出
大量的热②I是一种常见的温室气体,它和E可以发生反应:
2E+I 2F+D,F中E元素的质量分数为60%。回答问题:
2F+D,F中E元素的质量分数为60%。回答问题:
(1)①中反应的化学方程式为_____________________;
(2)化合物I的电子式为___________,它的空间构型是________________;
(3)8.0g G溶于盐酸,得到的溶液与铜粉完全反应,计算至少所需铜粉的质量____________g;
(4)C与过量NaOH溶液反应后溶液与过量化合物I反应的离子方程式为_____________;
(5)E在I中燃烧观察到的现象是_________________。
查看答案和解析>>
科目: 来源:2017届甘肃省高三上第二阶段考化学试卷(解析版) 题型:填空题
(1)将一定量的铁粉加入到装有200 mL某浓度的稀硝酸溶液的容器中充分反应。
①容器中剩余m1 g铁粉,收集到NO标准状况下体积为672 mL。
所得溶液中溶质的化学式 ,原硝酸溶液的物质的量浓度 mol/L。
②向上述固、液混合物中逐滴加入稀硫酸,直到不再产生NO气体为止,此时容器中还剩余铁粉m2 g
则此时溶液中溶质的化学式 ,m1-m2 的值为 g(精确到0.1g )
(2)铝电池性能优越,Al-空气燃 料电池通常以NaCl溶液或KOH溶液为电解质溶液,通入空气的电极为正极,以多孔石墨为正极材料。若以NaCl溶液为电解质溶液,正极的反应式为______________;若以KOH溶液为电解质溶液,电池总反应为_______________________。
料电池通常以NaCl溶液或KOH溶液为电解质溶液,通入空气的电极为正极,以多孔石墨为正极材料。若以NaCl溶液为电解质溶液,正极的反应式为______________;若以KOH溶液为电解质溶液,电池总反应为_______________________。
查看答案和解析>>
科目: 来源:2017届甘肃省高三上第二阶段考化学试卷(解析版) 题型:实验题
有一含NaCl、Na2CO3·10H2O和NaHCO3的混合物,某同学设计如图所示的实验装置,通过测量反应产生的CO2和H2O的质量,来确定该混合物中各组分的质量分数。
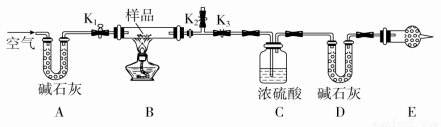
(1)实验步骤:
①按图(夹持仪器未画出)组装好实验装置后,首先进行的操作是 。
②称取样品,并将其放入硬质玻璃管中; 称量装浓硫酸的洗气瓶C的质量和装碱石灰的U形管D的质量。
称量装浓硫酸的洗气瓶C的质量和装碱石灰的U形管D的质量。
③打开活塞K1、K2,关闭K3,缓缓鼓入空气数分钟,其目的是______________________。
④关闭活塞K1、K2,打开K3,点燃酒精灯加热至不再产生气体。装置B中发生反应的化学方程式为____________ 、 。
⑤打开活塞K1,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C的质量和U形管D的质量。
(2)关于该实验方案,请回答下列问题。
①若加热反应后不鼓入空气,对测定结果的影响是NaCl________NaHCO3__________ Na2CO3·10H2O__________(填“偏大”“偏小”或“无影响”)
②E处干燥管中盛放的药品是___________,其作用是__________ ,如果实验中没有该装置,则会导致测量结果NaHCO3的质量分数___________(填写同①)。
③若样品质量为10.0 g,反应后C、D装置增加的质量分别为2.7 g、2.2 g,则混合物中Na2CO3·10H2O的质量分数为_______________。
查看答案和解析>>
科目: 来源:2017届甘肃省高三上第二阶段考化学试卷(解析版) 题型:实验题
某校化学兴趣小组探究SO2与FeCl3溶液的反应,所用装置如图所示。

(1)该小组同学预测SO2与FeCl3溶液反应的现象为溶液由棕黄色变成浅绿色,然后开始实验。
步骤① | 配制1 mol·L-1 FeCl3溶液(未用盐酸酸化),测其pH约为1, |
FeCl3溶液显酸性的原因是_______________________(用离子方程式表示)。写出装置A中产生SO2的化学方程式:______________________。
(2)当SO2通入到FeCl3溶液至饱和时,同学们观察到的现象是溶液由棕黄色变成红棕色,没有观察到丁达尔效应。将混合液放置12小时,溶液才变成浅绿色。
【资料】[Fe(HSO3)]2+离子为红棕色,它可以将Fe3+还原为Fe2+。生成[Fe(HSO3)]2+离子的反应为可逆反应。
解释SO2与FeCl3溶液反应生成红棕色[Fe(HSO3)]2+的原因:_____________________。
写出溶液中[Fe(HSO3)]2+离子与Fe3+反应的离子方程式:_________________。
(3)为了探究如何缩短红棕色变为浅绿色的时间,该小组同学进行了步骤②③的实验。
步骤② | 往5 mL 1 mol·L-1 FeCl3溶液中通入SO2气体,溶液立即变为红棕色。微热3 min,溶液颜色变为浅绿色 |
步骤③ | 往5 mL重新配制的1 mol·L-1 FeCl3溶液(用浓盐酸酸化)中通入SO |
用铁氰化钾K3[Fe(CN)6] 溶液检验步骤②和步骤③所得溶液中的Fe2+,其现象为______________
(4)综合上述实验探究过程,可以获得的实验结论:
Ⅰ.SO2与FeCl3溶液反应生成红棕色中间产物[Fe(HSO3)]2+离子;
Ⅱ.红棕色中间产物转变成浅绿色溶液是一个较慢的过程;
Ⅲ.___________________ ___ _______。
___ _______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com