
科目: 来源:2017届江苏省高三上学期期中化学卷(解析版) 题型:实验题
氯酸镁[Mg(ClO3)2]常用作催熟剂、除草剂等,制备少量Mg(ClO3)2·6H2O的工艺流程如下:

已知:
①卤块主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质。
②几种化合物的溶解度(S)随温度(T)变化曲线如右图所示。
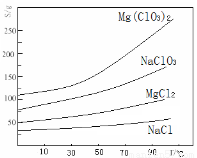
(1)过滤所需要的主要玻璃仪器有 ,加MgO后过滤所得滤渣的主要成分为 。
(2)加入NaClO3饱和溶液发生反应为:MgCl2+2NaClO3=Mg(ClO3)2+2NaCl↓再进一步制取Mg(ClO3)2·6H2O的实验步骤依次为:
① ;② ;③ ;④过滤、洗涤。
(3)产品中Mg(ClO3)2·6H2O含量的测定:
步骤1:准确称量3.50 g产品配成100 mL溶液。
步骤2:取10 mL于锥形瓶中,加入10 mL稀硫酸和20 mL 1.000  mol·L-1 FeSO4溶液,微热。此过程中反应的离子方程式为:ClO3-+6Fe2++6H+=6Fe3++Cl-+3H2O。
mol·L-1 FeSO4溶液,微热。此过程中反应的离子方程式为:ClO3-+6Fe2++6H+=6Fe3++Cl-+3H2O。
步骤3:冷却至室温,用0.100 mol·L-1 K2Cr2O7 溶液滴定步骤2中多余的Fe2+至终点。
此过程中反应的离子方程式为:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O。
步骤4: ,平均消耗K2Cr2O7 溶液15.00 mL。
①题中所用FeSO4溶液中,常加入适量稀硫酸和铁粉以抑制其变质。其中,加稀硫酸的作用是(用离子方程式解释): 。
②步骤4中空缺的内容为 。
③产品中Mg(ClO3)2·6H2O(摩尔质量为299g/mol)的质量分数为 。
查看答案和解析>>
科目: 来源:2017届江苏省高三上学期期中化学卷(解析版) 题型:填空题
(1)氮和碳的化合物与人类生产、生活密切相关。已知:
N2(g)+O2(g)===2NO(g);ΔH=+180.5 kJ·mol-1
2H2(g)+O2(g)===2H2O(g);ΔH=-483.6 kJ·mol-1
则反应2H2(g)+2NO(g)===2H2O(g)+N2(g);ΔH= 。
(2)在压强为0.1 MPa条件,将a mol CO和3a mol H2的混合气体在催化剂作用下转化为甲醇的反应为CO(g)+2H2(g) CH3OH(g);ΔH<0。
CH3OH(g);ΔH<0。
①该反应的平衡常数表达式为 。
②若容器容积不变,下列措施可增大甲醇产率的是 (填字母)。
A.升高温度
B.将CH3OH从体系中分离
C.充入He,使体系总压强增大
(3)如图所示的装置能吸收和转化NO2和SO2。

阳极区的电极反应式为 。
②阴极排出的溶液中含S2O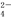 离子,能将NO2气体转化为无污染气体,同时生成的SO
离子,能将NO2气体转化为无污染气体,同时生成的SO 可在阴极区再生。写出该反应的离子方程式: 。
可在阴极区再生。写出该反应的离子方程式: 。
(4)将H2S和空气的混合气体通入FeCl3 、FeCl2 、CuCl2的混合溶液中反应回收S,其物质转化如图所示。
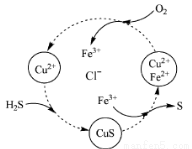
①在图示的转化中,化合价不变的元素是 。
②反应中当有1molH2S转化为硫单质时,保持溶液中Fe3+的物质的量不变,需要消耗O2的物质的量为 。
查看答案和解析>>
科目: 来源:2017届江苏省高三上学期期中化学卷(解析版) 题型:填空题
铜单质及其化合物在很多领域有重要的用途。
(1)超细铜粉可由[Cu(NH3)4]SO4制备。
① [Cu(NH3 )4]SO4中金属阳离子的核外电子排布式为 。N、O、S三种元素的第一电离能大小顺序为 。(填元素符号)
)4]SO4中金属阳离子的核外电子排布式为 。N、O、S三种元素的第一电离能大小顺序为 。(填元素符号)
②NH3分子中N原子的杂化方式为 ,与NH3互为等电子体的阳离子的化学式为 。
③ SO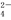 离子的空间构型为 。
离子的空间构型为 。
(2)氯化亚铜(CuCl)的某制备过程是:向CuCl2溶液中通入一定量SO2,微热,反应一段时间后即生成CuCl白色沉淀。
①写出上述制备CuCl的离子方程式: 。
②CuCl的晶胞结构如图所示,其中Cl原子的配位数为 。
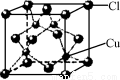
查看答案和解析>>
科目: 来源:2017届江西师大附中高三上学期期中化学试卷(解析版) 题型:选择题
化学与生产和生活密切相关。下列过程中没有发生化学变化的是( )
A.明矾净水  B.硅胶作袋装食品的干燥剂
B.硅胶作袋装食品的干燥剂
C.二氧化硫作纸浆的漂白剂 D.肥皂水作 蚊虫叮咬处的清洗剂
蚊虫叮咬处的清洗剂
查看答案和解析>>
科目: 来源:2017届江西师大附中高三上学期期中化学试卷(解析版) 题型:选择题
下列叙述Ⅰ和Ⅱ均正确并有因果关系的是( )
选项 | 叙述Ⅰ | 叙述Ⅱ |
A | 1?己醇的沸点比己烷的沸点高 | 1?己醇和己烷可通过蒸馏初步分离 |
B | 原电池可将化学能转化为电能 | 原电池需外接电源才能工作 |
C | 乙二酸可与KMnO4溶液发生反应 | 乙二酸具有酸性 |
D | Na在Cl2中燃烧的生成物含离子键 | NaCl固体可导电 |
查看答案和解析>>
科目: 来源:2017届江西师大附中高三上学期期中化学试卷(解析版) 题型:选择题
类比推理是化学中常用的思维方法。下列推理正确的是( )

A.HCl可以用如图装置完成喷泉实验, 推测HF可以用此装置完成喷泉实验
B.Fe与Cl2反应生成FeCl3,推测Fe与I2反应生成FeI3
C.SiH4的沸点高于CH4,推测H2Se的沸点高于H2S
D.NaCl与浓H2SO4加热可制HCl,推测NaBr与浓H2SO4加热可制HBr
查看答案和解析>>
科目: 来源:2017届江西师大附中高三上学期期中化学试卷(解析版) 题型:选择题
LiAlH4是金属储氢材料又是有机合成中的常用试剂,遇水能剧烈反应释放出氢气,LiAlH4在125 ℃时分解为LiH、H2和Al。下列叙 述错误的是( )
述错误的是( )
A.LiAlH4与乙醛作用 生成乙醇,LiAlH4作还原剂
生成乙醇,LiAlH4作还原剂
B.LiAlH4与D2O反应,所得氢气的摩尔质量为4 g·mol-1
C.1 mol LiAlH4在125 ℃时完全分解,转移3 mol电子
D. LiAlH4与水反应生成三种物质时,可能的化学方程式可表示为:
LiAlH4与水反应生成三种物质时,可能的化学方程式可表示为:
LiAlH4+4H2O=Al(OH)3↓+LiOH+4H2↑
查看答案和解析>>
科目: 来源:2017届江西师大附中高三上学期期中化学试卷(解析版) 题型:选择题
实验室制取少量干燥的氨气涉及下列装置,其中正确的是 ( )

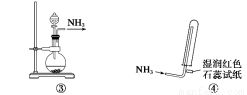
A.①是氨气发生装置 B.③是氨气发生装置
C.②是氨气吸收装置 D.④是氨气收集、检验装置
查看答案和解析>>
科目: 来源:2017届江西师大附中高三上学期期中化学试卷(解析版) 题型:选择题
下列现象或事实可用同一原理解释的是( )
A.SO2和FeSO4溶液使酸性高锰酸钾的紫色褪去
B.浓硫酸和浓盐酸长期暴露在空气中浓度降低
C.不能用pH试纸测定浓硫酸和新制氯水的pH
D.亚硫酸钠溶液和氯化铝溶液在空气中蒸干不能得到对应的溶质
查看答案和解析>>
科目: 来源:2017届江西师大附中高三上学期期中化学试卷(解析版) 题型:选择题
研究发现,空气中少量的NO2能参与硫酸型酸雨的形成,反应过程如下:
①SO2+NO2→SO3+NO ②SO3+H2O→H2SO4 ③2NO+O2→2NO2硫酸有下列变化:
①潮湿的氯气通过盛有浓H2SO4的洗气瓶
②硫化氢通入浓H2SO4中
③浓H2SO4滴入萤石(CaF2)中,加热制取HF
④加入少量H2SO4使乙酸乙酯水解.NO2在上述过程中的作用,与H2SO4在下列变化中的作用相似的是( )
A.①②③④ B.②④ C.④ D.②
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com