
科目: 来源:2016-2017学年广东省惠州市高二上学期高二质量检测化学试卷(解析版) 题型:选择题
下图各容器中盛有海水,铁在其中腐蚀时由快到慢的顺序是

A.(4)>(2)>(1)>(3)
B.(2)>(1)>(3)>(4)
C.(4)>(2)>(3)>(1)
D.(3)>(2)>(4)>(1)
查看答案和解析>>
科目: 来源:2016-2017学年广东省惠州市高二上学期高二质量检测化学试卷(解析版) 题型:选择题
某氢氧燃料电池的电解液是热的KOH溶液,在正极上氧气被还原,在负极上氢气被氧化,下列有关该电池的叙述正确的是
A.负极反应式为:
B.正极反应式为: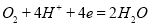
C.工作一段时间后,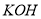 溶液的浓度不变
溶液的浓度不变
D.电池工作时,电子由正极通过外电路流向负极
查看答案和解析>>
科目: 来源:2016-2017学年广东省惠州市高二上学期高二质量检测化学试卷(解析版) 题型:选择题
如图曲线a表示放热反应X(g)+Y(g) Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是
Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是
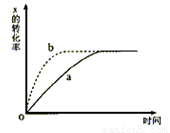
A.升高温度
B.加大X的投入量
C.加催化剂
D.增大体积
查看答案和解析>>
科目: 来源:2016-2017学年广东省惠州市高二上学期高二质量检测化学试卷(解析版) 题型:选择题
对室温下体积相同,浓度均为0.1 mol·L-1的盐酸和醋酸两种溶液分别采取下列措施。有关叙述一定正确的是
A.加水稀释100倍后,两溶液的pH相同
B.加入NaOH固体恰好中和后,两溶液的pH相同
C.分别加入足量锌粉充分反应,反应开始时两酸产生H2的反应速率相等
D.加人足量的小苏打固体充分反应后,两溶液中产生的CO2一样
查看答案和解析>>
科目: 来源:2016-2017学年广东省惠州市高二上学期高二质量检测化学试卷(解析版) 题型:选择题
某小组为研究电化学原理,设计如图装置,下列叙述正确的是
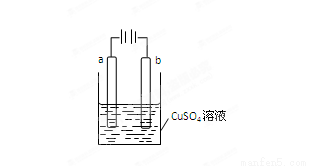
A.若a和b为石墨,通电后a电极上的反应为:Cu2++2e-=Cu
B.若a和b为石墨,通电后滴入酚酞,a电极附近溶液呈红色
C.若a为铜, b为铁,通电后Cu2+ 向a电极移动
b为铁,通电后Cu2+ 向a电极移动
D.若a为粗铜,b为纯铜,通电后b电极质量增加
查看答案和解析>>
科目: 来源:2016-2017学年广东省惠州市高二上学期高二质量检测化学试卷(解析版) 题型:选择题
下述实验不能达到预期目的的是
编号 | 实验内容 | 实验目的 |
A | 将SO2通入酸性KMnO4溶液中 | 证明SO2具有还原性 |
B | 将Cl2通入NaBr溶液中 | 比较氯与溴的氧化性强弱 |
C | 将铜与浓硝酸反应生成的气体收集后用冰水混合物冷却降温 | 研究温度对化学平衡的影响 |
D | 分别向2支试管中加入相同体积不同浓度的H2O2溶液,再向其中1支加入少量MnO2 | 研究催化剂对H2O2分解速率的影响 |
查看答案和解析>>
科目: 来源:2016-2017学年广东省惠州市高二上学期高二质量检测化学试卷(解析版) 题型:选择题
下列实验对应的结论不正确的是
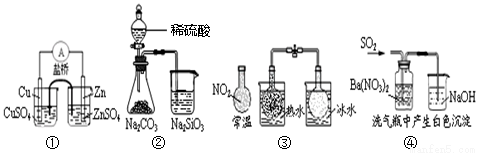
A.①能组成 Zn、Cu原电池 B.② 能证明非金属性:S>C>Si
Zn、Cu原电池 B.② 能证明非金属性:S>C>Si
C.③说明反应2NO2 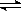 N2O4 △H<0 D.④ 白色沉淀为BaSO3
N2O4 △H<0 D.④ 白色沉淀为BaSO3
查看答案和解析>>
科目: 来源:2016-2017学年广东省惠州市高二上学期高二质量检测化学试卷(解析版) 题型:实验题
氧化铜矿石含有CuO和Cu2(OH) 2CO3,还含有Fe2O3、FeO和SiO2等。铜、铁是畜禽所必需的微量元素。某厂生产硫酸铜和硫酸亚铁流程如下:
(1)氧化铜矿石粉碎的目的是 。氧化时加入的KMnO4的作用是 。
(2)写出“酸浸”中Cu2(OH) 2CO3发生反应的化学方程式 。
(3)“中和/过滤”中加入CaCO3的目的是 。
(4)流程中多处涉及“过滤”,实验室中过滤需要使用的玻璃仪器有烧杯、 。
(5)加入铁屑的作用是 、 。
(6)下表为硫酸铜晶体“烘干粉碎”的试验结果。
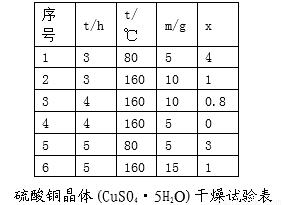
表中m为CuSO4·5H2O晶体的质量,x为干燥后所得晶体中结晶水个数。据此可确定由CuSO4·5H2O脱水得流程所示产品适宜工艺条件分别为 (指出条件的温度和时间)。
查看答案和解析>>
科目: 来源:2016-2017学年广东省惠州市高二上学期高二质量检测化学试卷(解析版) 题型:填空题
一定温度下,向一容积不变的密闭容器中加入2 molA和2 molB ,发生反应:2A ( g ) + B ( g ) 3C ( g ) ;ΔH=-akJ/mol ,达到平衡时放出bkJ热量,B的体积分数为ω1%;若向此平衡容器中再充入1 molB和3 mo1C ,在同温度下达到平衡时吸收c kJ的热量 ,B的体积分数为ω2 %,则:
3C ( g ) ;ΔH=-akJ/mol ,达到平衡时放出bkJ热量,B的体积分数为ω1%;若向此平衡容器中再充入1 molB和3 mo1C ,在同温度下达到平衡时吸收c kJ的热量 ,B的体积分数为ω2 %,则:
(1)ω1% ω2 % (填“ > ”、“=”或“ < " )。
(2)a、b数值的大小关系为a b(填“ > ”、“=”或“ < ”或“不确定”);
(3)b、c数值的大小关系为 b c (填“ > ”、“=”或“ < ”或“不确定”)。
(4)a 、b 、c三者的数学关系为 (用不等式或等式表示)。
若A、B、C的起始加入量分别为xmol、ymol、zmol,达到平衡时B的体积分数仍为ω1%,则x、y、z应满足的关系是 。
查看答案和解析>>
科目: 来源:2016-2017学年广东省惠州市高二上学期高二质量检测化学试卷(解析版) 题型:填空题
在一个固定容积的密闭容器中,有如下反应:
CO(g)+H2O(g) CO2(g)+H2(g);△H=QkJ·mol-1,其化学平衡常数K和温度t的关系如下
CO2(g)+H2(g);△H=QkJ·mol-1,其化学平衡常数K和温度t的关系如下
t/℃ | 700 | 800 | 850 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.25 |
(1) 上述反应中Q 0(选填“>”或“<”)
(2) 下列各项能判断该反应已达到化学平衡状态的是
a. 容器中压强不变 b. △H不变
c. v正(H2)=v逆(CO) d. CO的质量分数不变
(3) 温度为850℃时,可逆反应:CO(g)+H2O(g) CO2(g)+H2(g) 在固定容积的密闭容器中进行,容器 内各物质的浓度变化如下表:850℃时各物质的浓度(mol·L-1) 变化
CO2(g)+H2(g) 在固定容积的密闭容器中进行,容器 内各物质的浓度变化如下表:850℃时各物质的浓度(mol·L-1) 变化
时间(min) | CO | H2O | CO2 | H2 |
0 | 0.200 | 0.300 | 0 | 0 |
2 | 0.138 | 0.238 | 0.062 | 0.062 |
3 | c1 | c2 | c3 | c4 |
4 | c1 | c2 | c3 | c4 |
5 | 0.116 | 0.216 | 0.084 | |
6 | 0.096 | 0.266 | 0.104 |
① 计算:0~4min时, H2O(g)的转化率= 。
② 表中5min~6min之间数值发生变化,可能的原因是________。
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com