
科目: 来源:2017届浙江省“七彩阳光”新高考研究联盟高三下学期期初联考化学试卷(解析版) 题型:选择题
用 NA 表示阿伏加德罗常数的值。下列判断正确的是
A. 44g CO2 含有的原子数目为 NA
B. 1L1 mol·Lˉ1 的(NH4)2SO4 溶液中含有的 NH4+数目为2NA
C. 足量的 MnO2 与 100ml12 mol·L-1的浓盐酸充分反应,转移的电子数目为 0.6 NA
D. 常温常压下,18mL 水含有的分子数目约为 NA
查看答案和解析>>
科目: 来源:2017届浙江省“七彩阳光”新高考研究联盟高三下学期期初联考化学试卷(解析版) 题型:选择题
某工厂用 FeCl3 溶液腐蚀镀有铜的绝缘板生产印刷电路。课外活动小组为确认生产后的废液的组成,进行如下实验:(1)取10mL 废液加入足量的 AgNO3 溶液,生成沉淀 8.61g。(2)另取 10mL废液放入铜片充分反应,铜片质量减少了0.256g。下列关于原废液组成的判断错误的是
A. 一定含有 Fe 2+、 Fe 3+、 Cu2+、 Clˉ B. c(Fe2+):c(Cu2+) = 2:1
C. c(Clˉ) = 6mol / L, c(Fe 2+) = 1.2mol / L D. c (Fe2+):c(Fe 3+) = 3:1
查看答案和解析>>
科目: 来源:2017届浙江省“七彩阳光”新高考研究联盟高三下学期期初联考化学试卷(解析版) 题型:选择题
现有下列三个氧化还原反应:
① 2B- + Z2 = B2+2 Z - ② 2A2+ + B2 = 2A3+ + 2B- ③ 2XO4- + 10Z - + 16H+ = 2X2+ + 5Z2 + 8H2O
根据上述反应,判断下列结论中错误的是
A. 要除去含有 A2+、Z-和B-混合溶液中的A2+,而不氧化Z-和B-,应加入Z2
B. 还原性强弱顺序为: A2+﹥B-﹥Z-﹥X2+
C. X2+是 XO4- 的还原产物, B2 是 B-的氧化产物
D. 在溶液中可能发生反应: XO4- +5 A2++ 8H+ = X2+ + 5A3+ + 4H2O
查看答案和解析>>
科目: 来源:2017届浙江省“七彩阳光”新高考研究联盟高三下学期期初联考化学试卷(解析版) 题型:选择题
在15 mL0.10 mol·L-1NaOH 溶液中逐滴加入 0.20 mol·L-1 的氢氰酸(HCN,一元弱酸)溶液,溶液的pH和加入的氢氰酸溶液的体积关系曲线如下图所示,有关粒子浓度大小关系正确的是

A. 在 A、B 间任意一点:c(Na+)﹥c(CN-)﹥c(OH-)﹥c(H+)
B. 在 B 点:c(Na+) = c(CN-)﹥c( OH-) = c(H+),且 a=7.5
C. 在 C 点:c(CN-)﹥c(Na+)﹥c(OH-)﹥c(H+)
D. 在 D 点:c(HCN) + c(CN-)﹥2c(Na+)
查看答案和解析>>
科目: 来源:2017届浙江省“七彩阳光”新高考研究联盟高三下学期期初联考化学试卷(解析版) 题型:推断题
溶液 A中可能含有如下离子:Na+、NH4+、Ba2+、Mg2+、SO42-、SO32-、Cl-、OH-。某同学设计并完成了如下的实验:

下列说法正确的是
A. 溶液 A 中一定存在 NH4+、 SO42-、 SO32-,可能存在 Na+
B. 溶液 A 中一定存在 NH4+、 Mg2+、 SO42-、 SO32-,可能存在 Cl-
C. 溶液 A 中可能存在 Cl-,且 c(Na+) ≥ 0.20 mol·L-1
D. 如果气体 F 能使湿润的蓝色石蕊试纸变红,说明溶液中一定含有 NH4+
查看答案和解析>>
科目: 来源:2017届浙江省“七彩阳光”新高考研究联盟高三下学期期初联考化学试卷(解析版) 题型:推断题
常见有机物间的转化关系如下图所示(所示转化中,某些反应条件及产物未标明)。 B是天然有机高分子化合物, A、 E 均是常用调味品的主要成分,在相同条件下, G 的蒸气密度是氢气的 44 倍。

请回答:
(1)有机物 E 中含有的官能团名称是____________。
(2)检验 B 转化过程中有 C 生成,应先中和水解液,再需要加入的试剂名称是____________。
(3) A 和 E 反应生成 G 的化学方程式____________。
(4)某烃 T 的相对分子质量是 A 分子内脱水产物 Q 与 F 相对分子质量之和,分子中碳与氢的质量之比是5:1。下列说法正确的是____________。
A.T不溶于水,与甲烷互为同系物 B.T 性质稳定,高温下不会分解
C.T存在含有4个甲基的同分异构体 D.T可能和溴水发生加成反应
查看答案和解析>>
科目: 来源:2017届浙江省“七彩阳光”新高考研究联盟高三下学期期初联考化学试卷(解析版) 题型:推断题
某盐 A是由三种元素组成的化合物,某研究小组按如图流程探究其组成:
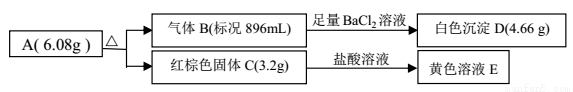
请回答:
(1)写出红棕色固体 C 的化学式____________。
(2)写出 A 受热分解反应的化学方程式____________。
(3)写出气体 B 与溶液 E 反应的离子方程式____________。
查看答案和解析>>
科目: 来源:2017届浙江省“七彩阳光”新高考研究联盟高三下学期期初联考化学试卷(解析版) 题型:实验题
下图为足量铜与浓硫酸反应的装置。请回答:

(1)写出盛放有铜片的仪器名称____________。
(2)检查装置气密性的操作为____________。
(3)下列有关该实验的说法中正确的是____________。
A.烧杯中氢氧化钠溶液的作用是吸收尾气,防止空气污染
B.实验时可以观察到圆底烧瓶中溶液由无色最终变为蓝色
C.含 0.08 mol 溶质的浓硫酸与足量的铜片反应,能收集到896mL(标准状况)的SO2
D.在该实验中浓硫酸体现了酸性和强氧化性
E.如果 B 中盛有少量 KMnO4 溶液,反应一段时间后,可以观察到紫色褪去,说明SO2具有漂白性。
查看答案和解析>>
科目: 来源:2017届浙江省“七彩阳光”新高考研究联盟高三下学期期初联考化学试卷(解析版) 题型:计算题
用沉淀法测定 KHCO3和 Na2CO3 固体混合物的组成,每次称取一定质量的样品溶于水制成溶液,向其中滴加相同浓度的 Ba(OH)2 溶液,每次实验均充分反应,反应前后溶液体积变化忽略不计,实验记录见下表:
实验序号 | I | II | III | IV | Ⅴ |
样品质量(g) | 3.06 | 6.12 | 9.18 | 12.24 | 15.30 |
Ba(OH)2溶液体积(mL) | 300 | 300 | 300 | 300 | 300 |
生成沉淀的质量(g) | 5.91 | 11.82 | 17.73 | 23.64 | 23.64 |
回答下列问题:
(1)样品中KHCO3 和Na2CO3 的物质的量之比_______。
(2)室温下第III组实验所得溶液中的 OH-物质的量浓度为_________。
查看答案和解析>>
科目: 来源:2017届浙江省“七彩阳光”新高考研究联盟高三下学期期初联考化学试卷(解析版) 题型:简答题
已知在298K和101kPa条件下,有如下反应:
反应Ⅰ:C(s) + O2(g) = CO2(g) △ H1=-393.5 kJ·mol-1
反应Ⅱ:2C(s) + O2(g) = 2CO(g) △ H2=-221 kJ·mol-1
反应Ⅲ:N2(g) + O2(g) = 2NO(g) △ H3=+180.5 kJ·mol-1
试回答下列问题:
(1)汽车尾气净化原理为反应Ⅳ:2NO(g) + 2CO(g)  N2(g) + 2CO2(g) △ H=______,该反应能自发进行的条件是_______。(填“高温”、“低温”或“任意温度”)。
N2(g) + 2CO2(g) △ H=______,该反应能自发进行的条件是_______。(填“高温”、“低温”或“任意温度”)。
(2)如果在一定温度下,体积为 2 升的密闭容器中发生化学反应Ⅳ,0~4min各物质物质的量的变化如下表所示:
物质(mol) 时间 | NO | CO | N2 | CO2 |
起始 | 0.40 | 1.0 | ||
2 min 末 | 2.0 | 0.80 | 1.6 | |
4 min 末 | 1.6 |
①求 0~2min 内用 CO 来表示的平均反应速率 v(CO)=________。
②试计算该温度下反应Ⅳ 的化学平衡常数 K=_________。
(3)若一定温度下,在容积可变的密闭容器中,上述反应Ⅳ达到平衡状态,此时容积为3L, c(N2)随时间 t 的变化曲线 x 如图所示。

①若在 t2min时改变一个条件,c(N2)随反应时间 t 的变化如曲线 y 所示,则改变的条件是______。
②若在t2min时升高温度,t3min时重新达到平衡,请在图中画出在 t2~t4 内 c(N2)的变化曲线______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com