
科目: 来源:2017届安徽省A10联盟高三下学期开年考试理综化学试卷(解析版) 题型:实验题
下图是实验室进行氯气的制备及性质实验的组合装置,部分固定装置未画出。
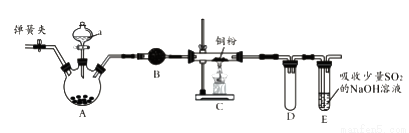
(1)A中固体是氯酸钾,液体a是浓盐酸,写出该反应的化学方程式:_________________。
(2)B为干燥装置,加入的固体是_________________;欲净化氯气,A、B间应添加一个盛有_________________的洗气瓶。
(3)C中的反应现象是_________________;D的作用是_________________。
(4)已知E中发生的反应为:Cl2+Na2SO3+2NaOH 2NaCl+Na2SO4+H2O。E中吸收尾气一段时间后,吸收液(强碱性)中肯定存在:Cl-、OH-和SO42-。某兴趣小组认为该吸收液中还可能存在ClO-和SO32-。
2NaCl+Na2SO4+H2O。E中吸收尾气一段时间后,吸收液(强碱性)中肯定存在:Cl-、OH-和SO42-。某兴趣小组认为该吸收液中还可能存在ClO-和SO32-。
a.甲同学认为该吸收液中ClO-和SO32-不能同时存在,其理由是_________________(用离子方程式表示)。
b.乙同学为了检验吸收液中是否含有SO32-,取少量吸收液于试管中,加适量稀硫酸酸化后,滴加品红溶液,发现品红溶液褪色。据此推断该吸收液中一定有SO32-。乙同学的推断是否正确?________________(填“正确”或“不正确”),理由是_________________。
c.请设计实验检验吸收液中是否含有ClO-_______________(写出实验步骤、现象和结论)。
查看答案和解析>>
科目: 来源:2017届安徽省A10联盟高三下学期开年考试理综化学试卷(解析版) 题型:简答题
工业采用氯化铵焙烧菱锰矿制备碳酸锰的流程如下图所示:
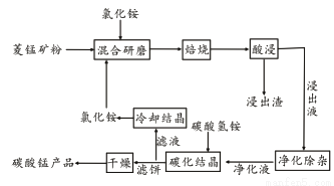
已知:①菱锰矿的主要成分是MnCO3 ,其中含Fe、Ca、Mg、Al等元素。
②焙烧过程中主要反应为:MnCO3 +2NH4Cl  MnCl2+2NH3↑ +CO2↑+ H2O。
MnCl2+2NH3↑ +CO2↑+ H2O。
③部分阳离子沉淀时溶液的pH的值:
Al3- | Fe3+ | Ca2+ | Mn2+ | Mg2+ | |
开始沉淀的pH值 | 4.1 | 2.2 | 10.6 | 8.8 | 9.6 |
沉淀完全的pH值 | 4.7 | 3.2 | 13.1 | 10.1 | 11.1 |
(1)实验室“焙烧”操作盛放固体的仪器为____________________。
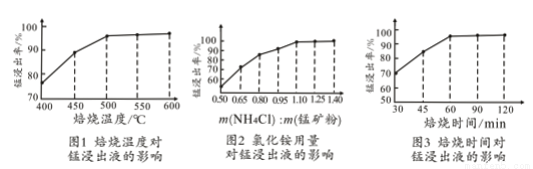
(2)结合图1、2、3,分析焙烧过程中对温度、NH4Cl用量[m(NH4Cl):m(锰矿粉)]、时间的最佳选择依次为________________、_______________、______________。
(3)对锰浸出液净化除杂时,先加入MnO2将Fe2+转化为Fe3+,再调节溶液pH的范围为_________________,将Fe3+和Al3+变为沉淀除去。然后加入NH4F将Ca2+、Mg2+变为氟化物沉淀除去。
(4)“碳化结晶”步骤中,加入碳酸氢铵是反应的离子方程式为________________。
(5)上述流程中可循环使用的物质是_______________。
(6)为测定产品中碳酸锰的含量,设计如下实验(杂质不参加反应):实验步骤为:称取16.80g试样,溶于适量的稀硫酸溶液中,向所得溶液中加入稍过量的磷酸和硝酸,加热使反应:2Mn2++NO3-+4PO43-+2H+ 2[Mn(PO4)2]3-+NO2-+H2O充分进行。除去溶液中存在的NO3-和NO2-后,加入l00.00mL2.00 mol·L-1的(NH4)2Fe(SO4)2溶液,发生的反应为:[Mn(PO4)2]3-+Fe2+=Mn2++Fe3++2PO3-;再用1.00mol·L-1酸性K2Cr2O7溶液滴定过量的Fe2+,滴定终点时消耗10.00mL酸性K2Cr2O7溶液。
2[Mn(PO4)2]3-+NO2-+H2O充分进行。除去溶液中存在的NO3-和NO2-后,加入l00.00mL2.00 mol·L-1的(NH4)2Fe(SO4)2溶液,发生的反应为:[Mn(PO4)2]3-+Fe2+=Mn2++Fe3++2PO3-;再用1.00mol·L-1酸性K2Cr2O7溶液滴定过量的Fe2+,滴定终点时消耗10.00mL酸性K2Cr2O7溶液。
①酸性K2Cr2O7溶液与Fe2+反应的离子方程式为_____________________(还原产物是Cr3+)。
②产品中碳酸锰的质量分数为_____________(结果保留3位有效数字)。
查看答案和解析>>
科目: 来源:2017届安徽省A10联盟高三下学期开年考试理综化学试卷(解析版) 题型:简答题
高炉炼铁中常见的反应为:Fe2O3(s)+3CO(g) 2Fe(s)+3CO2(g) △H
2Fe(s)+3CO2(g) △H
(1)某实验小组在实验室模拟上述反应。一定温度下,在2L盛有Fe2O3粉末的恒容密闭容器中通入0.1molCO,5min时生成2.24gFe。5min内有CO表示的平均反应速率是______________mol·L-1min-1;5min时CO2的体积分数为___________;若将此时反应体系中的混合气体通入100mL0.9mol/L的NaOH溶液中,充分反应后所得溶液中离子浓度由大到小的顺序是__________________ 。
(2)上述反应的平衡常数表达式为:K=_______________;下列能说明该反应已经达到平衡状态的是_____________(填序号)。
a.容器内固体质量保持不变
b.容器中气体压强保持不变
c.c(CO)=c(CO2)
d.v正(CO)=v逆(CO2)
(3)已知上述反应的平衡常数K与温度T(单位:K)之间的关系如图所示,其中直线的斜率为-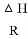 (气体常数R=8.3×10-3kJ·mol-1·K-1)。
(气体常数R=8.3×10-3kJ·mol-1·K-1)。
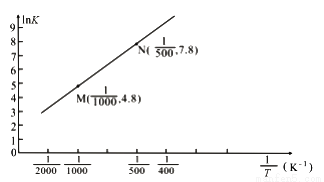
①根据图像可知,该反应的平衡常数随温度升高而____________(填“增大”、“减小”或“不变”)
②该反应的△H=_______________kJ·mol-1。
(4)结合上述有关信息,写出两条提高CO转化率的措施_____________、_______________。
查看答案和解析>>
科目: 来源:2017届安徽省A10联盟高三下学期开年考试理综化学试卷(解析版) 题型:填空题
铁和钴是两种重要的过渡元素。
(1)钴位于元素周期表得第_____________族,其基态原子中未成对电子的个数为______。
(2)[Fe(H2NCONH2)]6(NO3)3的名称是三硝酸六尿素合铁(Ⅲ),是一种重要的配合物。该化合物中Fe3+的核外电子排布式为____________________,所含非金属元素的电负性由大到小的顺序是____________________。
(3)尿素分子中、碳原子为________杂化,分子中σ键与π键的数目之比为____________________。
(4)FeO晶体与NaCl晶体结构相似,比较FeO与NaCl的晶格能大小,还需要知道的数据是______。
(5)Co(NH3)5BrSO4可形成两种钴的配合物,结构分别为[Co(NH3)5Br]SO4和[Co(SO4)(NH3)5]Br。已知Co3+的配位数是6,为确定钴的配合物的结构,现对两种配合物进行如下实验:在第一种配合物溶液中加硝酸银溶液产生白色沉淀,在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀。则第二种配合物的配体为____________________。
(6)奥氏体是碳溶解在γ-Fe中形成的一种间隙固溶体,无磁性,其晶胞为面心立方结构,如下图所示,则该物质的化学式为____________________。若晶体密度为dg·cm3,则晶胞中最近的两个碳原子的距离为____________________pm(阿伏伽德罗常数的值用NA表示,写出简化后的计算式即可)。

查看答案和解析>>
科目: 来源:2017届安徽省A10联盟高三下学期开年考试理综化学试卷(解析版) 题型:推断题
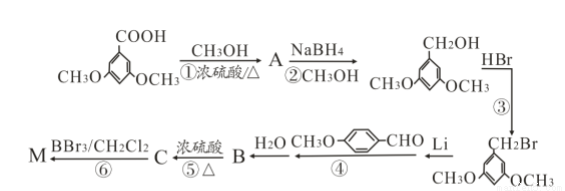
化合物M(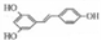 )具有预防心血管疾病的作用,其一种合成路线如下:
)具有预防心血管疾病的作用,其一种合成路线如下:
已知:RCH2Br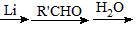


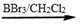
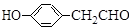
回答下列问题:
(1)M的官能团名称为_____________。③的反应类型是___________。
 核磁共振氢谱中不同化学环境的氢原子个数比为___________。
核磁共振氢谱中不同化学环境的氢原子个数比为___________。
(2)写出①的化学方程式____________________。
(3)B的结构简式为__________________。
(4) 有多种同分异构体,其中能发生银镜反应且苯环上一氯取代物只有两种的同分异构体有_________________种。
有多种同分异构体,其中能发生银镜反应且苯环上一氯取代物只有两种的同分异构体有_________________种。
(5)参照上述合成路线,设计由乙烯合成2-丁醇的合成路线(用合成路线流程图表示,并注明反应条件,合成过程中只有无机试剂可任选)_______________________。
查看答案和解析>>
科目: 来源:2017届陕西省宝鸡市高三教学质量检测(一)理综化学试卷(解析版) 题型:选择题
化学与生产、生活密切相关,下列说法正确的是
A. 煤的干馏可得到煤油、石蜡和沥青
B. 自来水厂可用明矾对水进行消毒杀菌
C. 氧化铝可用来制造耐高温的容器
D. 装有硅胶的透气袋可防止富含油脂的月饼被氧化
查看答案和解析>>
科目: 来源:2017届陕西省宝鸡市高三教学质量检测(一)理综化学试卷(解析版) 题型:选择题
下列反应的产物可使酸性高锰酸钾溶液褪色的是
A. 丙烯的加聚反应产物
B. 乙醇的消去反应产物
C. 甲烷与氯气的取代反应中的有机产物
D. 苯与氢气按1:3加成反应的产物
查看答案和解析>>
科目: 来源:2017届陕西省宝鸡市高三教学质量检测(一)理综化学试卷(解析版) 题型:选择题
某溶液中含有大量的K+、Cl-及X与Y两种离子,现向该溶液加入W试剂,根据实验现象得到的关于X、Y离子的推断能成立的是
W试剂 | 实验现象 | X、Y离子的推测 | |
A | KI—淀粉溶液 | 溶液变蓝 | Fe3+、SO42- |
B | 用pH试纸检测 | pH=7(常温) | CH3COO-、Na+ |
C | 硝酸酸化的AgNO3溶液 | 白色沉淀 | CO32-、NH4+ |
D | 过量NaOH溶液 | 无明显现象 | Al3+、Mg2+ |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源:2017届陕西省宝鸡市高三教学质量检测(一)理综化学试卷(解析版) 题型:选择题
X、Y、Z、M、R为五种短周期元素,其原子半径和最外层电子数之间的关系如下图所示。下列说法不正确的是

A. R的氧化物都含有离子键
B. 最高价含氧酸的酸性:Z < Y
C. M的氢化物常温常压下为气体
D. Y形成的化合物种类最多
查看答案和解析>>
科目: 来源:2017届陕西省宝鸡市高三教学质量检测(一)理综化学试卷(解析版) 题型:选择题
下列关于实验操作说法正确的是
A. 用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出
B. 中和滴定实验中,锥形瓶用蒸馏水洗净须经烤箱烘干后才可使用
C. 配制0.5mol·L–1 、480mL的NaOH溶液需称量9.6g的NaOH固体作溶质
D. 某溶液中滴入2滴K3[Fe(CN)6]溶液生成具有特征蓝色的沉淀,说明原溶液中含有Fe2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com