
科目: 来源:2016-2017学年江苏省扬州市宝应县高二下学期学业水平测试(三)化学试卷(解析版) 题型:简答题
(1)2015年为加强南海建设,我国对南海多个岛屿进行了“吹埋扩建”。
① 海岛生态环境十分脆弱,下列做法不利于海岛环境保护的是__________ (填字母)。
a.在海岛上植树造林,加强绿化
b.建设海水淡化厂,减少对海岛地下水的开采
c. 在海岛上开展风力发电,减少燃油发电机的使用
在海岛上开展风力发电,减少燃油发电机的使用
d.将生活垃圾运离海岛,就近抛入大海
② 建设岛屿时需用大量水泥。水泥属于 ___________________________ (填字母)。
a.金属材料 b.无机非金属材料 c.有机高分子材料
③ 建设岛屿的工程机械易生锈受损,下列措施中不能减缓工程机械生锈受损的是_____.
a.对机械配件进行发蓝处理 b.机械停用后及时擦干涂油
c.在机械表面刷上油漆  d.在机械表面上附着多块铜板
d.在机械表面上附着多块铜板
④ 海岛上往往缺少新鲜蔬菜,建岛工人需服用含______________ (填字母)的营养剂以防止患上“坏血病”。
a.维生素A b.维生素B c.维生素C d.维生素D
⑤ 海岛上生存环境恶劣,工人需准备一些常用药物,可选用 ______ (填字母)进行
镇热解痛。
a.阿司匹林 b.青霉素 c.胃舒平 d.吗啡
(2)我国新修订的《环境保护法》,使环境保护有了更严格的法律依据.
①空气污染指数API表明了空气的质量。空气污染指数主要是根据空气中________、NO2和可吸入颗粒物等污染物的浓度计算出来的数值。
②居室装修所使用的人造板材会释放出一种挥发性物质,长期接触会引起过敏性皮炎,免疫功能异常,该挥发性物质是________。
③工业废水需处理达标后才能排放。轧钢厂排出的废水主要是含盐酸的酸性废水,处理此废水可采用的方法是________。
④对汽车加装尾气催化净化装置,可以使其中的NOx、CO相互反应转化成无毒的气体,其原理可以用化学方程式表示为______________________________。
(3)材料是人类是赖以生存和发展的重要物质基础。
①右图所示的是战国初期的曾侯乙编钟,它是一套庞大的青铜乐器。铸造该器物的主要材料是________(填字母,下同)。
a. Cu、Zn b. Cu、Sn c. Al、Si
②不锈钢丝与棉纤维可织成一种防辐射布料。这种布料属于________。
a. 合金材料 b. 复合材料 c. 陶瓷材料
③为提高人体素质,要注意饮食健康。
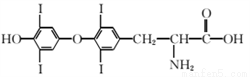
避免人体缺碘影响正常的生命活动,我国早已采取食 盐加碘措施。据报道,人从食物中摄取碘后碘便在甲状腺中积存下来, 通过一系列化学反应可形成甲状腺素。甲状腺素的结构如下
盐加碘措施。据报道,人从食物中摄取碘后碘便在甲状腺中积存下来, 通过一系列化学反应可形成甲状腺素。甲状腺素的结构如下 图,回答下列问题:
图,回答下列问题:
我们用稀盐酸和淀粉KI试纸可以检验食盐中碘酸钾的存在,反应的离子方程式为____________________________________________________________________________
碘在人体中属于________(填“常量元素 ”或“微量元素”)。
”或“微量元素”)。
④富含淀粉的面点老少皆宜,淀粉的化学式是___________________________;
查看答案和解析>>
科目: 来源:2016-2017学年江苏省扬州市宝应县高二下学期学业水平测试(三)化学试卷(解析版) 题型:计算题
下图为一些物质之间的转化关系,其中部分反应中反应物或生成物未列全。已知A、H、I、K均为家庭厨房中的常见物质,其中A是食品调味剂,H是消毒剂的有 效成分,I、K可用作食品发泡剂。B是一种有机酸盐,E、F、G均为氧化物,L是红褐色沉淀。
效成分,I、K可用作食品发泡剂。B是一种有机酸盐,E、F、G均为氧化物,L是红褐色沉淀。
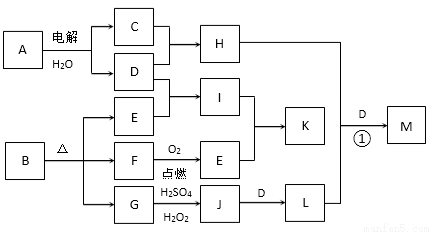
根据以上信息,回答下列问题:
⑴H的化学式为____________________________。
⑵ A的电子式___________________________________________。
⑶ G→J的离子方程式为________________________________________________________________。
⑷ M是含氧酸盐,化学式为Na2FeO4,则反应①的化学方程式为____________________________________________。
查看答案和解析>>
科目: 来源:2016-2017学年江苏省扬州市宝应县高二下学期学业水平测试(三)化学试卷(解析版) 题型:简答题
用磁铁矿(主要成分Fe3O4、含Al2O3和SiO2等杂质),制取高纯铁红的工艺流程如下。
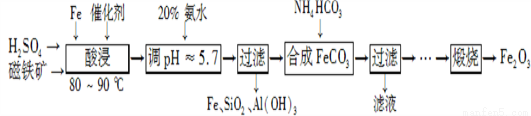
(1) 酸浸时,采用80-90℃的原因 _______________________________________________;
_______________________________________________;
铁粉的作用是____________________________________。
(2) 合成碳酸亚铁的离子方程式__________________________________________________________________。
(3) 图中“滤液”中主要阳离子是_______________________________________________________________;
(4)为了测定磁铁矿中铁的含量,称取80 g的磁铁矿样品加入足量稀硫酸使其充分溶解,过滤,得溶液100mL,取20mL溶液在酸性条件下用0.4 mol·L-1 KMnO4溶液滴定,当溶液中Fe2+ 全部被氧化时,消耗KMnO4溶液体积 10.00 mL。(已知MnO4-被还原为Mn2+)
mol·L-1 KMnO4溶液滴定,当溶液中Fe2+ 全部被氧化时,消耗KMnO4溶液体积 10.00 mL。(已知MnO4-被还原为Mn2+)
①写出滴定时反应的离子方程式__________________________________________
②当溶液中Fe2+ 全部被氧化时,c(Fe3+)=_____________________mol·L-1, (写出计算过程)。
查看答案和解析>>
科目: 来源:2017届安徽省“江南十校”高三3月联考理综化学试卷(解析版) 题型:选择题
化学与生产和生活密切相关,下列有关说法正确的是
A. 刚玉硬度仅次于金刚石,熔点也相当高,刚玉坩埚可用于熔融KHSO4
B. CO2是大量使用的灭火剂,但着火的镁条在CO2中继续燃烧说明它也可以助燃
C. 人血清中的血浆铜蓝蛋白相对分子质量为151000,是人工合成的高分子化合物
D. 三氯化铁易形成水合晶体,加热Fe2O3·6H2O晶体,可获得纯净的FeC13
查看答案和解析>>
科目: 来源:2017届安徽省“江南十校”高三3月联考理综化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列说法正确的是
A. 50mL18.4mol·L-1硫酸与足量Cu共热,转移的电子数为0.92NA
B. 2L0.5 mol·L-1醋酸溶液中含有的H+数为NA
C. 2.0gH218O与D2O的混合物中所含中子数为NA
D. 密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA
查看答案和解析>>
科目: 来源:2017届安徽省“江南十校”高三3月联考理综化学试卷(解析版) 题型:选择题
下列有关有机物说法不正确的是
A. CH3CH(OH)CH2COOH系统命名法命名3-羟基丁酸
B. 四苯基乙烯(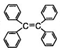 )中所有碳原子一定处于同一平面
)中所有碳原子一定处于同一平面
C. lmol 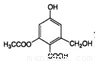 分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别是3mol、4mol、1mol
分别与足量的Na、NaOH溶液、NaHCO3溶液反应,消耗这三种物质的物质的量分别是3mol、4mol、1mol
D. 在一定条件下,苯与液溴、浓硝酸生成溴苯、硝基苯的反应都属于取代反应
查看答案和解析>>
科目: 来源:2017届安徽省“江南十校”高三3月联考理综化学试卷(解析版) 题型:选择题
高铁电池是一种可充电电池,其设计图如下所示:负极材料是Zn,氧化产物是Zn(OH)2,正极材料是K2FeO4(易溶盐),还原产物是Fe(OH)3,电解质溶液是KOH水溶液。下列有关说法正确的是
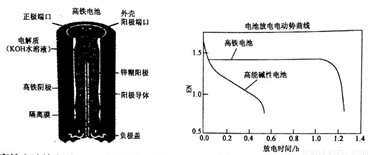
A. 高铁电池放电时正极反应为:Zn+2OH--2e-=Zn(OH)2
B. 高铁电池充电时阴极反应为Fe(OH)3+5OH--3e-=FeO42-+4H2O
C. 高铁电池放电时的总反应为:2FeO42-+8H2O+3Zn=2 Fe(OH)3+3 Zn(OH)2+4OH-
D. 高能碱性电池比高铁电池工作电压更稳定
查看答案和解析>>
科目: 来源:2017届安徽省“江南十校”高三3月联考理综化学试卷(解析版) 题型:选择题
用0.1000mol/L的标准盐酸分别滴定20.00mL的0.1000mol/L氨水和20.00mL的0.1000mol/L氢氧化钠溶液的滴定曲线如图所示,横坐标为滴定百分数(滴定用量/总滴定用量),纵坐标为滴定过程中溶液pH,甲基红是一种酸碱指示剂,变色范围为4.4-6.2,下列有关滴定过程说法正确的是
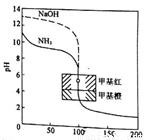
A. 滴定氨水溶液当滴定分数为50%时,各离子浓度间存在关系:c(NH4+)+c(H+)=c(OH-)
B. 滴定分数为100%时,即为滴定过程中反应恰好完全的时刻
C. 从滴定曲线可以判断,使用甲基橙作为滴定过程中的指示剂准确性更佳
D. 滴定氨水溶液当滴定分数为150%时,所得溶液中离子浓度有大小关系c(Cl-)>c(H+)
查看答案和解析>>
科目: 来源:2017届安徽省“江南十校”高三3月联考理综化学试卷(解析版) 题型:选择题
a、b、c、d为四种短周期元素,a的原子M电子层有l个电子,b是地壳中含量最多的金属元素,c的最高化合价为最低化合价绝对值的3倍,c与d同周期,d的原子半径小于c。关于这四种元素下列叙述错误的是
A. a、c、d均存在两种以上的氧化物
B. b的氧化物与d的最高价氧化物对应水化物反应后的溶液呈酸性
C. a是短周期中金属性最强的元素
D. 工业上是通过电解b、d形成的化合物制取b单质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com