
科目: 来源:2016-2017学年山西省高二下学期第一次月考化学试卷(解析版) 题型:选择题
钛号称“崛起的第三金属”,因具有密度小、强度大、无磁性等优良的机械性能,被广泛应用于军事、医学等领域。已知钛有48Ti、49Ti、50Ti等同位素,下列关于金属钛的叙述中不正确的是( )
A. 上述钛原子中,中子数不可能为22 B. 钛元素在周期表中处于第四周期ⅡB族
C. 钛原子的外围电子层排布为3d24s2 D. 钛元素位于元素周期表的d区,是过渡元素
查看答案和解析>>
科目: 来源:2016-2017学年山西省高二下学期第一次月考化学试卷(解析版) 题型:选择题
下表是部分短周期元素的原子半径及主要化合价,以下叙述正确的是( )
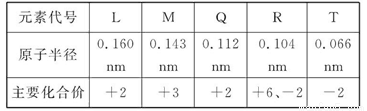
A. 气态氢化物的稳定性为H2T<H2R
B. 单质与稀盐酸反应的速率为L<Q
C. M与T形成的化合物具有两性
D. L2+与R2-的核外电子数相等
查看答案和解析>>
科目: 来源:2016-2017学年山西省高二下学期第一次月考化学试卷(解析版) 题型:选择题
分析原子的杂化方式,并根据等电子体原理判断下列各组分子中的所有原子,或者处于同一平面,或者在一条直线上的是
A.C2H2、HClO、C2H6 B.CO2、N2O、HC≡C—NH2
C.C6H5CH3、C3H4、CH4 D.C6H6、C2H4、HCN
查看答案和解析>>
科目: 来源:2016-2017学年山西省高二下学期第一次月考化学试卷(解析版) 题型:选择题
A、B、C、D都是短周期元素,原子半径:D > C > A > B。已知:A、B同周期,A、C处于同一主族;C原子核内的质子数等于A、B原子核内的质子数之和;C原子最外层电子数是D原子最外层电子数的3倍,下列说法正确的是( )
A. A的元素符号为Be B. B和D两种元素形成的化合物中只能含有离子键
C. D2B和D2B2阴、阳离子个数比分别为1:2和1:1 D. C和D两元素的最高价氧化物的水化物相互反应生成盐和水
查看答案和解析>>
科目: 来源:2016-2017学年山西省高二下学期第一次月考化学试卷(解析版) 题型:填空题
下图是元素周期表的一部分
① | |||||||||||||||||
② | ③ | ④ | ⑤ | ||||||||||||||
⑥ | ⑦ | ⑧ | |||||||||||||||
⑨ | ⑩ |
(1)元素⑨的外围电子的电子排布图为________,元素⑩原子结构示意图为____________
(2)元素③④⑤的电负性由大到小的顺序为____________(填化学用语,下同),其第一电离能由大到小的顺序为_______________,其简单离子半径由大到小的顺序为_______________。
(3)如果在温度接近373K(100℃)时,根据M=m/n测定⑤的气态氢化物的相对分子质量,结果发现测定结果比理论值高,其原因是_________________。
(4)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的氢氧化物有相似的性质。写出元素②的最高价氧化物的水化物与NaOH溶液反应的离子方程式________________。
(5)根据下列五种元素的第一至第四电离能数据(单位:kJ·mol-1),回答下面各题:
元素代号 | I1 | I2 | I3 | I4 |
Q | 2080 | 4000 | 6100 | 9400 |
R | 500 | 4600 | 6900 | 9500 |
S | 740 | 1500 | 7700 | 10500 |
T | 580 | 1800 | 2700 | 11600 |
U | 420 | 3100 | 4400 | 5900 |
①在周期表中,最可能处于同一主族的是____________。(填元素代号)
②T元素最可能是______(填“s”、“p”、“d”、“ds”等)区元素;若T为第二周期元素,Z是第三周期元素中原子半径最小的主族元素,则T、Z形成的化合物分子键角为________。
查看答案和解析>>
科目: 来源:2016-2017学年山西省高二下学期第一次月考化学试卷(解析版) 题型:填空题
A、B、C、D、E为短周期元素且它们的原子序数依次增大,A的核外电子总数与其周期数相同,其中D原子的L电子层中,成对电子与未成对电子占据的轨道数相同,并且无空轨道;B原子的L电子层中未成对电子数与D相同,但还有空轨道;D与E同族,请回答下列问题:
(1)A与其他元素形成的二元共价化合物中,一种化合物分子呈三角锥形,该分子的化学式为______,其中心原子的杂化方式为______,A分别与B、C、D形成的共价化合物中既含有极性共价键,又含有非极性键的化合物是________________________。(填化学式,任意写出三种)。
(2)这些元素形成的含氧酸根离子中,其中心原子的价层电子对数为3的酸根离子是______________________(填化学式,下同);酸根离子呈三角锥形结构的是____________。
(3)BA4分子的立体构型为__________;根据电子云重叠方式的不同,该分子里共价键的类型为_________。
(4)B的一种氢化物相对分子质量是26,其分子中σ键和π键的键数之比为_________。
(5)B与D形成BD2分子,与该分子互为等电子体的有____________________。(分子跟阴离子各写一个)
查看答案和解析>>
科目: 来源:2016-2017学年山西省高二下学期第一次月考化学试卷(解析版) 题型:填空题
配位键是一种特殊的共价键,即共用电子对由某原子单方面提供和另一提供空轨道的粒子结合。如NH 就是由NH3(氮原子提供电子对)和H+(提供空轨道)通过配位键形成的。据此,回答下列问题:
就是由NH3(氮原子提供电子对)和H+(提供空轨道)通过配位键形成的。据此,回答下列问题:
(1)下列粒子中可能存在配位键的是((____))
A.CO2 B.H3O+ C.CH4 D.[Ag(NH3)2] +
(2)向硫酸铜溶液中滴加氨水,会有蓝色沉淀产生,继续滴加,沉淀溶解,溶液变成深蓝色。请写出其中发生反应的离子方程式_______________、________________。
(3)请写出铜原子的核外电子排布式_________________。
(4)配位化学创始人维尔纳发现,将各为1mol的CoCl3·6NH3(黄色)、CoCl3·5NH3(紫红色)、CoCl3·4NH3(绿色)、CoCl3·4NH3(紫色)四种配合物溶于水,加入足量硝酸银溶液,生成氯化银沉淀分别为3mol、2mol、1mol、和1mol。已知上述配合物中配离子的配位数均为6。请根据实验事实用配合物的形式写出它们的化学式。
①CoCl3·5NH3________________、②CoCl3·4NH3(紫色)__________________。
查看答案和解析>>
科目: 来源:2016-2017学年河北省邯郸市高一下学期第一次月考化学试卷(解析版) 题型:选择题
下列关于氮的说法正确的是 ( )
A. N2分子的结构较稳定,因而氮气不能支持任何物质燃烧
B. 23g NO2和N2O4混合气含有0.5NA个氮原子(NA表示阿伏加德罗常数)
C. NO可用向上排空气法或者排水法收集
D.浓硝酸保存在棕色瓶内是因为硝酸易挥发
查看答案和解析>>
科目: 来源:2016-2017学年河北省邯郸市高一下学期第一次月考化学试卷(解析版) 题型:选择题
下列各组物质中,不能进行喷泉实验的是( )
A. NH3和H2O B. NO和H2O C. CO2和NaOH溶液 D. HCl和H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com