
科目: 来源: 题型:
(16分)臭氧层是地球生命的保护神,臭氧比氧气具有更强的氧化性。实验室可将氧气通过高压放电管来制取臭氧:
(1)若在上述反应中有30%的氧气转化为臭氧,所得混合气的平均摩尔质量为 g/mol(保留一位小数)。
(2)将8L氧气通过放电管后,恢复到原状况,得到气体6.5L,其中臭氧为 L。
(3)实验室将氧气和臭氧的混合气体0.896L(标准状况)通入盛有20.0g铜粉的反应器中,充分加热后,粉末的质量变为21.6g。则原混合气中臭氧的体积分数为 。
查看答案和解析>>
科目: 来源: 题型:
(16分)某强酸性反应体系中,反应物和生成物共六种物质:O2 、MnO4-、H2O 、Mn2+ 、H2O2 、H+ 。已知该反应中H2O2 只发生了如下过程:H2O2 →O2。
![]() (1)该反应应选择的酸是: (填序号)。
(1)该反应应选择的酸是: (填序号)。
![]() A.盐酸 B.浓硫酸 C.稀硫酸 D.醋酸。
A.盐酸 B.浓硫酸 C.稀硫酸 D.醋酸。
![]() (2)该反应中发生还原反应的过程是: → 。
(2)该反应中发生还原反应的过程是: → 。
![]() (3)写出该反应配平的离子方程式并标出电子转移的方向和数目:
(3)写出该反应配平的离子方程式并标出电子转移的方向和数目:
![]() 。
。
(4)如果上述反应中有6.72L(标准状况.)气体生成,转移的电子数为 mol。
![]() (5)H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称;如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:KCN + H2O2+H2O = A + NH3↑,试指出生成物A的化学式为 ,并阐明H2O2被称为绿色氧化剂的理由是 。
(5)H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称;如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:KCN + H2O2+H2O = A + NH3↑,试指出生成物A的化学式为 ,并阐明H2O2被称为绿色氧化剂的理由是 。
查看答案和解析>>
科目: 来源: 题型:
一定条件下,用甲烷可以消除氮氧化物(NOx)的污染。已知:
① CH4 (g)+4NO2 (g)=4NO (g) +CO2 (g)+2H2O (g) △H=574 kJ?mol-1
② CH4 (g)+4NO (g)=2N2 (g)+CO2 (g)+2H2O (g) △H=1160 kJ?mol一1。下列选项正确的是
A.CH4 (g)+2NO2 (g)= N2 (g)+CO2 (g)+2H2O (l) △H=867 kJ?mol-1
B.若0.2 mol CH4还原NO2至N2,在上述条件下放出的热量为173.4 kJ
C.1molCH4催化还原NOx为N2的过程中,若x=1.6,则转移的电子为3.2 mol
D.若用标准状况下2.24L CH4还原NO2至N2,整个过程中转移的电子为0.8 mol
查看答案和解析>>
科目: 来源: 题型:
(08闽行区模拟)(10分)某结晶水合物含有两种阳离子和一种阴离子。称取两份质量均为45.3g的该结晶水合物,分别制成溶液。向其中一份逐滴加入NaOH溶液,开始发现溶液中出现白色沉淀并逐渐增多;一段时间后有气体逸出,该气体有刺激性气味,能使湿润的红色石蕊试纸变蓝,加热后共计可收集到2.24L该气体(标准状况);最后白色沉淀逐渐减少并最终消失。另一份逐滴加入Ba(OH)2溶液,开始现象类似,但最终仍有白色沉淀;过滤,用稀硝酸处理沉淀物,经洗涤和干燥,得到白色固体46.6 g。请回答以下问题:
(1)该结晶水合物中含有的两种阳离子是________和________,阴离子是_________。
(2)试通过计算确定该结晶水合物的化学式。
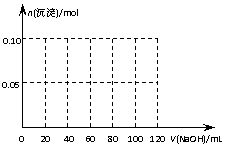
(3)假设反应过程中向该溶液中加入的NaOH溶液的物质的量浓度为5mol/L,请在下图中画出生成沉淀的物质的量与加入NaOH溶液体积的关系示意图。
 |
查看答案和解析>>
科目: 来源: 题型:
设NA表示阿伏加德罗常数的值,下列说法正确的是
A.18g D2O含有的电子数为10NA
B.标准状况下,11.2 L SO3中含有的分子数为0.5 NA
C.7.8 g Na2O2晶体中含有的阴离子数为0.1 NA
D.常温常压下,44 g CO2气体含有氧原子的个数为2 NA
查看答案和解析>>
科目: 来源: 题型:
某温度下,VmL不饱和![]() 溶液a g,蒸发掉b g水或加入b g
溶液a g,蒸发掉b g水或加入b g ![]() 固体(恢复到原温度)均可使溶液达到饱和,则下列量的计算结果正确的是
固体(恢复到原温度)均可使溶液达到饱和,则下列量的计算结果正确的是
A. 该温度下![]() 的溶解度为100g
的溶解度为100g
B. 原不饱和溶液中![]() 质量分数为
质量分数为![]()
C. 原不饱和溶液中![]() 物质的量浓度为
物质的量浓度为![]()
D. 原不饱和溶液的密度为![]()
查看答案和解析>>
科目: 来源: 题型:
向含有0.078molFeCl2的溶液中通入0.009molCl2,再向其中加入含0.01molX2O72-的酸性溶液,使溶液中的Fe2+恰好完全被氧化,且X2O72-被还原为Xn+,则n值为
A.2 B.3 C.4 D.5
查看答案和解析>>
科目: 来源: 题型:
下列离子方程式书写正确的是
A.将过量的NaOH溶液滴入同浓度的少量Ca(HCO3)2溶液中
Ca2++2HCO![]() +2OH-=CaCO3↓+2H2O+CO
+2OH-=CaCO3↓+2H2O+CO![]()
B.向Ba(OH)2溶液中逐滴加入NH4HSO4溶液至刚好沉淀完全
Ba2++OH-+H++SO![]() =BaSO4↓+H2O
=BaSO4↓+H2O
C.向Ca(ClO)2溶液中通入适量SO2 : Ca2++2ClO-+SO2+H2O=CaSO3↓+2HCl
D.向FeI2溶液中加少量氯水 : 2Fe2++Cl2=2Fe3++2Cl-
查看答案和解析>>
科目: 来源: 题型:
下列叙述正确的是
A.有单质参加或单质生成的化学反应一定是氧化还原反应
B.生成物只有一种的化学反应不一定是化合反应
C.向煮沸的NaOH溶液中滴加FeCl3溶液可制备Fe(OH)3胶体
D.有电解质参加的化学反应一定可以用离子方程式表示查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com