
科目: 来源: 题型:
用MnO2,和浓HCl反应制Cl2,当有0.4molHCl被氧化时,生成的Cl2全部用石灰水吸收,则(1)生成多少Cl2mol?
(2)可制得漂白粉多少克?
查看答案和解析>>
科目: 来源: 题型:
右图是实验室用铜片与浓硫酸制取SO2并验证其性质的装置图。往试管Ⅰ中加入一小块铜片,再加入3~5mL 浓硫酸,用带导管的单孔橡胶塞塞好试管,加热,将生成的气体通入试管Ⅱ的溶液中。
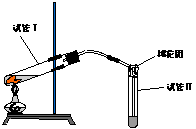 (1)若试管Ⅱ中的溶液是紫色石蕊试液,反应一段时间后,试管Ⅱ中看到的现象是
(1)若试管Ⅱ中的溶液是紫色石蕊试液,反应一段时间后,试管Ⅱ中看到的现象是
__________________________。(2分)
(2)若试管Ⅱ中的溶液是品红试液,反应一段时间后,看到的现象是__________________________,(2分)反应充分后,取下试管Ⅱ并在酒精灯上加热,看到的现象是__________________________。(2分)
(3)实验过程中,试管Ⅱ管口塞一团浸有NaOH溶液的棉花,作用是_____________,(2分)有关反应的离子方程式为 ______________________。(2分)
查看答案和解析>>
科目: 来源: 题型:
某氧化铝样品中含有氧化铁和二氧化硅(一种酸性氧化物)杂质,现欲制取纯净的氧化铝,某同学设计如下的实验方案。回答下列问题:
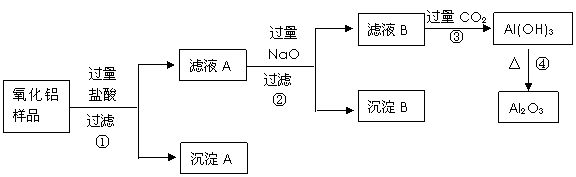
(1)沉淀A的化学式是________________,滤液B的成分除水外是_______________________;
(2)步骤③的离子方程式为______________________________________;
(3)在操作②中要用到的玻璃仪器有_____________________________________________
查看答案和解析>>
科目: 来源: 题型:
NO是一种剧毒气体,但近年来发现许多生物体组织中存在少量NO,它有扩张血管、免疫、增强记忆的功能,因而成为当前生命科学的研究热点。
(1)写出自然界形成NO的化学方程式:__________________________。(2分)
(2)NO在大气层中可发生反应:
NO+O3→NO2+O……………①, NO2+O==NO+O2……………②
上述反应①中,NO是__________剂(2分),上述反应②中,NO是_________产物。(2分)
(3)为了消除NO对环境的污染,根据氧化还原反应原理,可选用NH3使NO转化为两种无毒气体(其中之一是水蒸气),该反应需要催化剂参加,其化学方程式为____________________
_____________________________。(2分)
查看答案和解析>>
科目: 来源: 题型:
海水占地球总储水量的97.2%。若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海洋资源。
(1)海水中含有大量的氯化钠。请写出氯原子的原子结构示意图________________ ;(1分)
(2)目前国际上实用的“海水淡化”主要技术之一是蒸馏法。蒸馏法是将海水变成蒸汽,蒸汽经过冷却而得高纯度淡水,由此可判断蒸馏法是____________________ (填物理变化、化学变化);(1分)
(3)工业上利用电解饱和食盐水可制得重要化工产品,又称为“氯碱工业”。电解饱和食盐水的化学方程式为 ____________________________________________ ;(2分)
(4)近年来有人提出了一种利用氯碱工业产品及氯化钠循环治理含二氧化硫废气并回收二氧化硫的方法,该方法的流程如下:
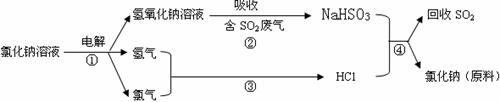 |
查看答案和解析>>
科目: 来源: 题型:
(1)实验室中萃取分液用到的玻璃实验仪器名称是 _____________。(1分)下列可以用于溴水中溴的萃取的试剂是 __________,(1分)(①乙醇,②四氯化碳,③盐酸)萃取后实验现象_______________________________________。(1分)分液后还要通过_________(实验操作方法)得到纯溴。(1分)
(2)合理利用化学反应可以造福人类。请写出下列反应的化学方程式:
①印刷电路板是由高分子材料和铜箔复合而成,用FeCl3溶液作“腐蚀剂”刻制印刷电路_______
__________________________________________。(2分)
②工业上制取漂白粉 __________________________ 。(2分)
③ “绿色化学”要求综合考虑经济、技术、环保等方面来设计化学反应路线。若以铜为原料制取硫酸铜,请你设计符合“绿色化学”思想的反应路线 ______________________________
________________________________________________。(4分)
查看答案和解析>>
科目: 来源: 题型:
 右图是某学校实验室从化学试剂商店买回的浓盐酸试剂标签上的部分内容。现用该浓盐酸配制100 mL 1 mol·L-1的稀盐酸。可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④ 药匙;⑤量筒;⑥托盘天平。请回答下列问题:
右图是某学校实验室从化学试剂商店买回的浓盐酸试剂标签上的部分内容。现用该浓盐酸配制100 mL 1 mol·L-1的稀盐酸。可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④ 药匙;⑤量筒;⑥托盘天平。请回答下列问题:
(1)配制稀盐酸时,还缺少的仪器有 (写仪器名称);(1分)
(2)经计算,配制100 mL1 mol·L-1的稀盐酸需要用量筒量取上述浓盐酸的体积为 mL,(1分)量取盐酸时应选用 mL(1分)(选填10 mL、50 mL 、100 mL)规格的量筒;
(3)对所配制的稀盐酸进行测定,发现其浓度大于1 mol·L-1,请你分析配制过程中可能引起误差的原因(写出其中一个即可) 。(1分)
查看答案和解析>>
科目: 来源: 题型:
对于某些离子的检验及结论一定正确的是( )
A.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO![]()
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO![]()
C.加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH![]()
D.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
查看答案和解析>>
科目: 来源: 题型:
在海水中提取溴的反应原理是5NaBr+NaBrO3+3H2SO4 = 3Br2+3Na2SO4+3H2O下列反应的原理与上述反应最相似的是( )
A.2NaBr+Cl2 = 2NaCl+Br2 B.2FeCl3+H2S = 2FeCl2+S↓+2HCl
C.2H2S+SO2 = 3S+2H2O D.AlCl3+3NaAlO2+6H2O=4Al(OH)3↓+3NaCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com