
科目: 来源: 题型:
在由水电离出的c(H+)= 1×10-13 mol·L-1的溶液中一定大量共存的离子组是( )
A. Fe2+, Na+, NO3-, Cl- B. Ba2+,Na+, NO3-,Cl-
C.SO42-,S2O32-,NH4+,Na+ D.Mg2+,Na+,Br -,[Al(OH)4]-
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是( )
A.强极性键形成的化合物不一定是强电解质
B.强电解质溶液的导电能力一定比弱电解质溶液强
C.NaCl溶液在电流的作用下电离成钠离子和氯离子
D.氯化钠晶体不导电是由于氯化钠晶体中不存在离子
查看答案和解析>>
科目: 来源: 题型:
下列关于平衡常数K的说法中,正确的是( )
A.在任何条件下,化学平衡常数是一个恒定值
B.改变反应物浓度或生成物浓度都会改变平衡常数K
C.平衡常数K只与温度有关,与反应物浓度、压强无关
D.从平衡常数K的大小不能推断一个反应进行的程度
查看答案和解析>>
科目: 来源: 题型:
甲烷是一种高效清洁的新能源,0.25mol甲烷完全燃烧生成液态水时放出222.5KJ热量,则下列热化学方程式中正确的是( )
A.2CH4(g) + 4O2(g) = 2CO2(g) + 4H2O(l);ΔH= +890KJ・mol―1
B. CH4(g) + 2O2(g) = CO2(g) +2H2O(l); ΔH=+890KJ・mol―1
C. CH4(g) + 2O2(g) = CO2(g) +2H2O(l); ΔH= -890KJ・mol―1
D. 2CH4(g) + 4O2(g) = 2CO2(g) + 4H2O(l);ΔH= -890KJ・mol―1
查看答案和解析>>
科目: 来源: 题型:
一定条件下,在体积为10 L的密闭容器中,1 mol X和1 mol Y进行反应:2X(g)+Y(g)![]() Z(g),经60 s达到平衡,生成0.3 mol Z,下列说法正确的是( )
Z(g),经60 s达到平衡,生成0.3 mol Z,下列说法正确的是( )
(A)以X浓度变化表示的反应速率为0.001 mol/(L·s)
(B)将容器体积变为20 L,Z的平衡浓度变为原来的1/2
(C)若增大压强,则物质Y的转化率减小
(D)若升高温度,X的体积分数增大,则该反应的DH>0
查看答案和解析>>
科目: 来源: 题型:
下列各表述与示意图一致的是
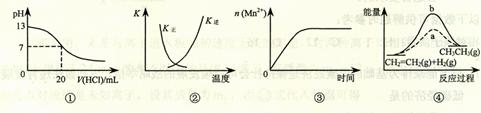
A.图①表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1 NaOH溶液,溶液的pH随加入酸体积的变化
B.图②中曲线表示反应2SO2(g) + O2(g) ![]() 2SO3(g);ΔH < 0 正、逆反应的平衡常数K随温度的变化
2SO3(g);ΔH < 0 正、逆反应的平衡常数K随温度的变化
C.图③表示10 mL 0.01 mol·L-1 KMnO4 酸性溶液与过量的0.1 mol·L-1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化
D.图④中a、b曲线分别表示反应CH2=CH2 (g) + H2(g)![]() CH3CH3(g);ΔH< 0使用和未使用催化剂时,反应过程中的能量变化
CH3CH3(g);ΔH< 0使用和未使用催化剂时,反应过程中的能量变化
查看答案和解析>>
科目: 来源: 题型:
一真空密闭容器中盛有amolPCl5,加热到200℃时发生如下反应:PCl5(气) PCl3(气)+Cl2(气)反应达平衡时,PCl5所占体积百分比为M %,若在同一温度和同一容器中,最初投入的是2amolPCl5,反应平衡时,PCl5所占体积百分比为N %,则M与N的关系是( )
(A)M>N (B)N>M (C)M=N (D)无法比较翰林汇
查看答案和解析>>
科目: 来源: 题型:
下列反应均处于平衡状态,在减压或升温时,平衡均能向右移动的是( )
(A)CO(g)+H2O(g)![]() CO2(g)+H2(g) △H>0
CO2(g)+H2(g) △H>0
(B)2HCl(g)![]() H2(g)+Cl2(g) △H>0
H2(g)+Cl2(g) △H>0
(C)2SO3(g)![]() 2SO2(g)+O2 △H>0
2SO2(g)+O2 △H>0
(D)CaO(s)+CO2(g)![]() CaCO3(s) △H﹤0
CaCO3(s) △H﹤0
查看答案和解析>>
科目: 来源: 题型:
容器体积不变,正反应是吸热反应的是( )
(A)2NO2![]() N2O4升温体系颜色加深
N2O4升温体系颜色加深
(B)N2+3H2![]() 2NH3升温NH3的浓度减小
2NH3升温NH3的浓度减小
(C)CO+H2O(g)![]() CO2+H2升温CO的转化率增大
CO2+H2升温CO的转化率增大
(D)2SO2+O2![]() 2SO3(g)降温SO2浓度减小
2SO3(g)降温SO2浓度减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com