
科目: 来源: 题型:
以电解食盐水为基础制取氯气等产品的工业称为“氯碱工业”,它是目前化学工业的重要支柱之一。
(1)电解饱和食盐水的化学方程式为 。
 (2)常温下,某化学兴趣小组在实验室中,用石墨电极以右图装置进行电解某浓度氯化钠溶液的实验,电解一段时间后,收集到标准状况下氢气2.24 L。(设电解前后溶液的体积均为1 L,不考虑水的消耗或气体的溶解)
(2)常温下,某化学兴趣小组在实验室中,用石墨电极以右图装置进行电解某浓度氯化钠溶液的实验,电解一段时间后,收集到标准状况下氢气2.24 L。(设电解前后溶液的体积均为1 L,不考虑水的消耗或气体的溶解)
①理论上,电解后溶液中c(OH—)= mol/L。
②若实际测得反应后溶液的c(OH—)=0.1mol/L,则造成这种误差的原因可能是:
a.2H2O![]() 2H2↑+O2↑;若仅考虑该原因,则电解过程中溶液减小的质量是 g。
2H2↑+O2↑;若仅考虑该原因,则电解过程中溶液减小的质量是 g。
b.还可能为 (用离子方程式表示)。
经测定,该实验中溶液实际减少的质量为4.23 g,则所产生的气体及其物质的量之比为 。
查看答案和解析>>
科目: 来源: 题型:
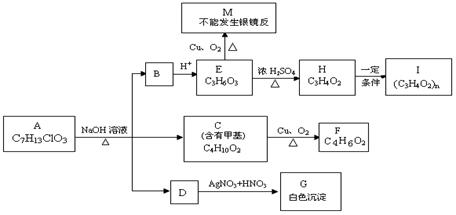
从物质A开始有如图所示的转化关系(其中部分产物已略去)。已知H能使溴的CCl4溶液褪色;1mol F(分子式C4H6O2)与足量新制Cu(OH)2在加热条件下充分反应可生成2molCu2O。分析图表回答问题:
(1)A的结构简式: 或
(2)写出反应类型: E→H 、H→I ;
(3)写出C→F的化学方程式: 。
(4)请设计出由丙烯合成E物质的反应流程图(有机物用结构简式表示,必须注明反应条件)。提示:①合成过程中无机试剂任选;②反应流程图表示方法
示例如下:
![]()
B C …… G
查看答案和解析>>
科目: 来源: 题型:
现有A、B、C、D、E、F六种化合物,它们分别由下列五种原子团中的两种不同的基团组成,这五种基团是-CH3,-C6H5,-OH,![]() 。
。
已知:(1)A是无色晶体,有特殊气味,在空气中易氧化成粉红色;(2)B、C能发生银镜反应,C的相对分子质量大于B;(3)D与少量氢氧化钠溶液反应,得到酸式盐;与过量氢氧化钠溶液反应,生成正盐。D可以和A的钠盐反应生成A;(4)E可以由B氧化制取;(5)F能氧化成最简单的醛。根据上述条件,请推断A B C
D E F 。在上述具有酸性的化合物中,相同条件下酸性由强到弱的顺序是 。(用结构简式表示)
查看答案和解析>>
科目: 来源: 题型:
 工业氢氧化钾的溶液中含有某些含氧酸的钾盐杂质,可用离子交换膜法电解提纯。电解槽内装有阳离子交换膜,其工作原理如图所示。
工业氢氧化钾的溶液中含有某些含氧酸的钾盐杂质,可用离子交换膜法电解提纯。电解槽内装有阳离子交换膜,其工作原理如图所示。
(1)该电解槽的阳极反应式为:
(2)阳离子交换膜的作用是
(3)通电开始后,阴极附近溶液pH会增大,其主要原因是 (填序号)
A.阳极区的OH-移向阴极所致
B.阴极产生的金属钾与水反应生成了大量OH-
C.阴极由H2O电离出的H+放电生成H2,促进水的电离,使OH-浓度增大
(4)除去杂质后的氢氧化钾溶液从溶液出口_____________(填写“A”或“B”)导出。
查看答案和解析>>
科目: 来源: 题型:
已知1,2-二氯乙烷常温下为无色液体,沸点为83.5 ℃,密度为1.23 g·mL-1,难溶于水,易溶于醇、醚、丙酮等有机溶剂。乙醇的沸点为78.5 ℃。某化学课外活动小组为探究1,2-二氯乙烷的消去反应,设计了如图所示的实验装置(加热装置略去)。
(1)如图所示,连接好仪器装置之后,首先需进行的操作是 。
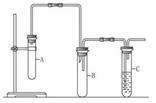 (2) 向装置A中大试管中加入1,2二氯乙烷和 (写名称);并向装置C中试管里加入适量溴水。A中发生反应的化学方程式是 。
(2) 向装置A中大试管中加入1,2二氯乙烷和 (写名称);并向装置C中试管里加入适量溴水。A中发生反应的化学方程式是 。
(3)与装置A中大试管相连接的长玻璃管除导气外的作用是 __________________,装置B的作用是 _________________。
(4)证明1,2-二氯乙烷已发生消去反应的现象是_______________,还可通过什么实验加以验证:________________________________________。
查看答案和解析>>
科目: 来源: 题型:
化学在能源开发与利用中起着十分关键的作用。
(1)蕴藏在海底的“可燃冰”是高压下形成的外观像冰的甲烷水合物固体。甲烷气体燃烧的热化学方程式为:CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890.3 kJ/mol。
356g“可燃冰”(若分子式为CH4·9H2O)释放的甲烷气体完全燃烧生成液态水.放出的热量为
kJ。
 (2)Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如右图所示,电解总反应为2Cu+H2O
(2)Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如右图所示,电解总反应为2Cu+H2O![]() Cu2O+H2
Cu2O+H2![]() 。该电解池中,铜电极接直流电源的 极;每生成1molCu2O,电路中通过的电子的数目为 ;该电解池的阴极反应式为 。
。该电解池中,铜电极接直流电源的 极;每生成1molCu2O,电路中通过的电子的数目为 ;该电解池的阴极反应式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com