
科目: 来源: 题型:
对于易燃、易爆、有毒的化学物质,往往会在其包装上贴以下危险警告标签。下面所列物质中,贴错了标签的是( )
| A | B | C | D | ||
| 物质的 化学式 | 浓HNO3 | CCl4 | KCN | KClO3 | |
| 危险警 告标签 |
腐蚀性 |
易燃的 |
|
| |
查看答案和解析>>
科目: 来源: 题型:
下列实验叙述不正确的是( )
A.从试剂瓶中取出并切下使用的钠块后,剩余的钠不能放回原试剂瓶
B.过滤时,将烧杯尖嘴靠在玻璃棒上,将玻璃棒下端靠在三层滤纸上
C.蒸馏时,冷凝水应从冷凝管下端口进,上端口出
D.实验室制取乙酸乙酯时,导气管出口端不能插入到饱和Na2CO3溶液的液面以下
查看答案和解析>>
科目: 来源: 题型:
常用抗生素“先锋Ⅵ”为粉末状固体,每瓶含“先锋Ⅵ”0.5 g,注射时应配成质量分数不高于20%的溶液,则使用时每瓶至少需加入生理盐水(密度约为1 g/cm3)( )
A.1 mL B.2 mL C.3 mL D.4 mL
查看答案和解析>>
科目: 来源: 题型:
相对分子质量为92的某芳香烃X是一种重要的有机化工原料,研究部门以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去)。其中A是一氯代物,H是一种功能高分子,链节组成为C7H5NO。

已知:
Ⅰ ![]()
Ⅱ ![]() (苯胺,易被氧化)
(苯胺,易被氧化)
请根据所学知识与本题所给信息回答下列问题:
⑴x的化学式是 ;
⑵H的结构简式是___________________________;
⑶反应②的类型是 ;
⑷反应⑤的化学方程式是_________________________ _____;
⑸![]() 有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有 种;
有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有 种;
⑹请用合成反应流程图表示出由![]() 和其他无机物合成
和其他无机物合成 最合理的方案(不超过4步)。
最合理的方案(不超过4步)。
例:
![]()
![]()

查看答案和解析>>
科目: 来源: 题型:
 砷化镓(GaAs)属于第三代半导体,用它制造的灯泡寿命是普通灯泡的100倍,而耗能只有其10%。推广砷化镓等发光二极管(LED)照明,是节能减排的有效举措。砷化镓的晶胞结构如右图。
砷化镓(GaAs)属于第三代半导体,用它制造的灯泡寿命是普通灯泡的100倍,而耗能只有其10%。推广砷化镓等发光二极管(LED)照明,是节能减排的有效举措。砷化镓的晶胞结构如右图。
试回答:
(1)As的核外电子排布式为 。
(2)砷化镓晶胞中所包含的Ga原子个数为 。
(3)下列说法正确的是 (填字母)。
A.砷化镓晶胞结构与NaCl相同 B.第一电离能:As>Ga
C.电负性:As>Ga D.砷化镓晶体中含有配位键
E.半导体GaP与GaAs互为等电子体
(4)砷化镓是将(CH3)3Ga和AsH3用MOCVD方法在700℃时制备得到。
AsH3的空间形状为 ,(CH3)3Ga中镓原子的杂化方式为 。
(5)AsH3沸点比NH3低,其主要原因是 。
查看答案和解析>>
科目: 来源: 题型:
重铬酸钾是工业生产和实验室的重要氧化剂,工业上常用铬铁矿(主要成份为FeO·Cr2O3)为原料生产,实验室模拟工业法用铬铁矿制K2Cr2O7的主要工艺如下,涉及的主要反应是:6FeO·Cr2O3+24NaOH+7KClO3![]() 12Na2CrO4+3Fe2O3 +7KCl+12H2O,
12Na2CrO4+3Fe2O3 +7KCl+12H2O,
试回答下列问题:
⑴在反应器①中,有Na2CrO4生成,同时Fe2O3转变为NaFeO2,杂质SiO2、Al2O3与纯碱反应转变为可溶性盐,写出氧化铝与碳酸钠反应的化学方程式: 。
⑵NaFeO2能强烈水解,在操作②生成沉淀而除去,写出该反应的化学方程式: 。
⑶操作③的目的是什么,用简要的文字说明: 。
 |
⑷操作④中,酸化时,CrO42-转化为Cr2O72-,写出平衡转化的离子方程式: 。
⑸称取重铬酸钾试样2.5000g配成250mL溶液,取出25.00mL于碘量瓶中,加入10mL 2mol/LH2SO4和足量碘化钾(铬的还原产物为Cr3+),放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用0.1200mol/LNa2S2O3标准溶液滴定(I2+2S2O32-=2I-+S4O62-)。
①判断达到滴定终点的依据是: ;
②若实验中共用去Na2S2O3标准溶液40.00mL,则所得产品的中重铬酸钾的纯度(设整个过程中其它杂质不参与反应) 。
查看答案和解析>>
科目: 来源: 题型:
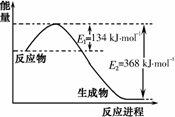 氮是地球上含量丰富的一种元素,氮元素的单质及其化合物在工农业生产、生活中有着重要作用。
氮是地球上含量丰富的一种元素,氮元素的单质及其化合物在工农业生产、生活中有着重要作用。
⑴右图是1mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式
⑵在固定体积的密闭容器中,进行如下化学反应:
N2(g)+3H2(g)![]() 2NH3(g) △H < 0 ,
2NH3(g) △H < 0 ,
其平衡常数K与温度T的关系如下表:
| T/K | 298 | 398 | 498 |
| 平衡常数K | 4.1×106 | K1 | K2 |
①该反应的平衡常数表达式:K=
②试判断K1 K2(填写 “>”“=”或“<”)
③下列各项能说明该反应已达到平衡状态的是 (填字母)
a.容器内N2、H2、NH3的浓度之比为1∶3∶2 b.v(N2)正 = 3v(H2)逆
c.容器内压强保持不变 d.混合气体的密度保持不变
⑶对反应N2O4(g)![]() 2NO2(g) △H > 0 ,在温度分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如右图所示,下列说法正确的是 。
2NO2(g) △H > 0 ,在温度分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如右图所示,下列说法正确的是 。
 a.A、C两点的反应速率:A>C
a.A、C两点的反应速率:A>C
b.A、C两点的化学平衡常数:A>C
c.A、C两点NO2的转化率:A<C
d.由状态B到状态A,可以用加热的方法
![]() ⑷一定温度下,在1L密闭容器中充入1molN2和3molH2并发生反应。若容器容积恒定,10min达到平衡时,气体的总物质的量为原来的 ,则N2的转化率a(N2)= , 以NH3表示该过程的反应速率v(NH3)= 。
⑷一定温度下,在1L密闭容器中充入1molN2和3molH2并发生反应。若容器容积恒定,10min达到平衡时,气体的总物质的量为原来的 ,则N2的转化率a(N2)= , 以NH3表示该过程的反应速率v(NH3)= 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com