
科目: 来源: 题型:
M、R都是生活中常见的金属单质,其中R是用量最多的金属。甲、乙是化合物,其中甲是黑色晶体,可由R在x中燃烧得到。

(1)M与甲在高温下反应的化学方程式是
(2)电解法制R的低价氢氧化物的装置如图I。a是4 mol·L— NaCl、1mol·L—NaOH的混合溶液。
①配制a时需要除去蒸馏水中溶解的O2,常采用 的方法。
②石墨电极应与电源的 (填“正”或“负”)极相连接,通电后,R电极附近的现象是 ,
R极的电极反应式是 。
③停止实验一段时间后,在R极上部有红褐色物质产生,反应的化学方程式是 。
(3)把R的某氧化物粉末与M粉末混合后分成两等份。一份在高温下恰好完全反应后,再与足量盐酸反应;另一份直接放入足量的烧碱溶液中充分反应。前后两种情况下生成的气体质量比是a:b,则R的氧化物的化学式是 。
(4)如图是一个化学过程的示意图。
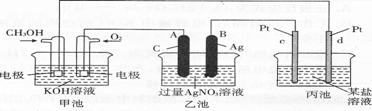
写出通入CH3OH的电极的电极反应式
(5)当乙池中B(Ag)极的质量增加5.40 g 时,甲池中理论上消耗O2 ml
(标准状况下);此时丙池某电极析出1.60 g某金属,则丙中的某盐溶液可能是 (填序号)。
A.MgSO4溶液 B.CuSO4溶液 C.NaCl溶液 D.AgN03溶液
查看答案和解析>>
科目: 来源: 题型:
如图表示由元素周期表中1~20号且不同主族元素组成的单质及化合物之间转化关系(产物中的水已略去)。其中A为单质;在实验室中.常用固体B和固体C加热制取气体F;F与G的组成元素相同.G与I分子所含电子数相同。请回答:

(1)写出B、G的化学式B 、G 。
(2)写出C的电子式 ;反应④的实验现象为 ;写出F的一种具体用途 。
(3)向具有漂白作用的D溶液加入I的稀溶液,写出反应的离子方程式: 。
向D的溶液加入I的浓溶液有A生成,其反应的离子方程式为: 。
(4)写出反应③的化学方程式 。
查看答案和解析>>
科目: 来源: 题型:
咖啡酸可用作化学原料和中间体,其结构如下图。下列关于咖啡酸的说法不正确的是
 A.能发生加聚反应
A.能发生加聚反应
B.能发生取代反应
C.1mol咖啡酸最多能与3mol NaOH反应
D.1mol咖啡酸最多能与3mol Br2反应
查看答案和解析>>
科目: 来源: 题型:
阿伏加德罗常数的值约为6.02×1023mol-1,下列叙述中不正确的是
①12.4g白磷晶体中含有的P-P键数约是0.6×6.02×1023
②电解精炼铜时转移了6.02×1023个电子,阳极溶解32 g铜
③7.8 g Na2S和Na2O2的混合物中含有的阴离子数大于0.1×6.02×1023
④2mol SO2和1 mol O2混合在V2O5存在的条件下于密闭容器中加热反应后,容器内物质分子数大于2×6.02×1023
⑤2.9g 2CaSO4·H2O含有的结晶水分子数为0.02×6.02×1023 (2CaSO4·H2O式量为290)
⑥含0.2 mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1 NA
A.①④⑥ B.①③④⑤⑥ C.②③⑤⑥ D.③④⑤⑥
查看答案和解析>>
科目: 来源: 题型:
已知:常温下醋酸铵溶液的PH=7现有常温下的4组混合溶液,分别由等体积0.1mol/l的2种溶液混合而成①NH4Cl与NaOH ②NH4Cl与 HCl ③NH4Cl 与NaCl ④NH4Cl与 NaHCO3 下列各项正确的是:
A.C(NH3·H2O)大小顺序:②>④>③>①
B.混合溶液④中存在C(NH3·H2O)+ C(CO32-)+ C(H+)= C(OH-)+ C(H2CO3)
C.混合溶液④中存在C(NH4+)< C(HCO3-)+ 2C(CO32-)
D.PH大小顺序①>④>③>②
查看答案和解析>>
科目: 来源: 题型:
水的电离平衡曲线如图所示,下列说法不正确的是:
 A.图中四点Kw间的关系: A=D<C<B
A.图中四点Kw间的关系: A=D<C<B
B.若从A点到D点,可采用:温度不变在水中加入少量酸
C.若从A点到C点,可采用:温度不变在水中加入少量NH4Cl固体
D.若处在B点,将pH=2的硫酸与pH=10的KOH的两种溶液等体积混合后,溶液显中性
查看答案和解析>>
科目: 来源: 题型:
下列反应的离子方程式正确的是
A.向Ba(OH)2溶液中滴加少量NaHSO4溶液,2H++SO42-+Ba2++2OH--=BaSO4+2H2O
B.向NH4HCO3溶液中加入足量的NaOH溶液并加热,NH4++OH—![]() NH3+H2O
NH3+H2O
C.将SO2气体通入NaClO溶液中,SO2+2ClO—+H2O=SO32—+2HClO
D. K2Cr2O7在水中存在平衡:其溶液颜色受酸碱性影响,碱性时为黄色
查看答案和解析>>
科目: 来源: 题型:
某无色溶液中含有①Na+②Ba2+③Cl-④Br-⑤SO32-⑥SO42-离子中的一种或几种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
| 步骤 | 操作 | 现象 |
| ① | 用PH试纸检验 | 溶液的PH大于7 |
| ② | 向溶液中滴入氯水,在加入CCl4振荡,静置 | CCl4层呈橙色 |
| ③ | 向②所得的溶液中加入Ba(NO3)2和稀HNO3 | 有白色沉淀产生 |
| ④ | 过滤,向滤液中加入AgNO3和稀HNO3 | 有白色沉淀产生 |
下列结论正确的是
A.肯定含有的离子是①④⑤ B. 肯定没有的离子是②⑤
C. 可能含有的离子是①③⑥ D.不能确定的离子是①③⑥
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是
A. 乙烯和聚乙烯都能使酸性KMnO4溶液褪色
B. 淀粉和纤维素水解的最终产物相同
C. 油脂的水解反应又称为皂化反应
D. 蔗糖属于高分子化合物,其水解产物能发生银镜反应
查看答案和解析>>
科目: 来源: 题型:
邻苯二甲酸丁基月桂酯是一种淡黄色透明油状液体,密度约0.97g/cm3,不溶于水,能溶于有机溶剂,常用作聚氯乙烯等树脂的增塑剂。工业上生产原理和工艺流程如下:
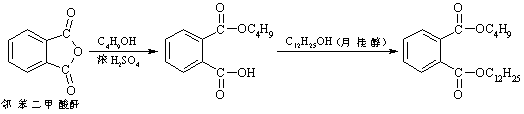
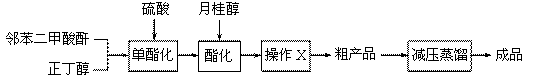
某实验小组的同学模拟工业生产的工艺流程,用右图所示装置制取少量邻苯二甲酸丁基月桂酯,图中夹持和加热装置已略去。主要操作步骤如下:
① 向三颈烧瓶内加入30 g 邻苯二甲酸酐、16 g 正丁醇以及少量浓硫酸。
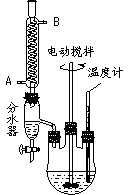 ② 搅拌,升温至105 ℃,持续搅拌反应1小时。
② 搅拌,升温至105 ℃,持续搅拌反应1小时。
③ 冷却至室温,加入40 g 月桂醇,升温至160 ℃,搅拌、保温至反应结束。
④ 冷却至室温,将反应混合物倒出。
⑤通过工艺流程中的操作X,得到粗产品。
请回答下列问题:
⑴反应物中加入浓硫酸的作用是 ▲ 。
⑵步骤③中搅拌下保温的目的是 ▲ ,判断反应已结束的方法是 ▲ 。
⑶步骤⑤中操作X包括 ▲ 。
⑷工艺流程中减压蒸馏的目的是 ▲ 。
⑸用测得相对分子质量的方法,可以检验所得产物是否纯净,测得相对分子质量通常采用的仪器是 ▲ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com