
科目: 来源: 题型:
下列实验设计能完成或实验结论合理的是
A.证明一瓶红棕色气体是溴蒸气还是二氧化氮,可用湿润的碘化钾-淀粉试纸检验,观察试纸颜色的变化
B.某溶液中加入碳酸钠溶液产生白色沉淀,再加盐酸沉淀消失,说明该溶液中有Ca2+
C.测氯水的pH,可用玻璃棒蘸取氯水点在pH试纸上,待其变色后和标准比色卡比较
D.用核磁共振氢谱图鉴别乙醇和乙酸
查看答案和解析>>
科目: 来源: 题型:
我国从澳大利亚进口的某高炉生铁(用A表示)的成分如下(其余是铁):
| C | Si | Mn | P | S |
| 4.070% | 2.900% | 0.495% | 0.165% | 0.010% |
(1)称取100.000g A经过一系列处理(最后一步是在空气中灼烧)后,锰全部转变为某种氧化物,其质量为0.687g,则其化学式为 。
(2)磷肥的肥效以相当含P2O5多少来表示。炼钢时,P元素形成炉渣Ca3(PO4)2,后者再与浓硫酸反应制得普通过磷酸钙[即普钙,成分是CaSO4、Ca(H2PO4)2和少量其它杂质]。若某普钙中Ca(H2PO4)2的质量分数为45.25%,则含P2O5的质量分数为 %。
(3)锰的质量分数为30%的高锰钢有很好的性能,可制作火车车轮。将A冶炼成含碳0.4%、含锰30%的高锰钢(设铁无损耗,其它杂质已除去,可补充锰),则100吨A可制得高锰钢
吨。
(4)某炼钢厂的烟尘成分和质量分数如下表:
| FeO | Fe2O3 | CaO | |
| 烟尘煅烧前(%) | 86.40 | 4.00 | 9.60 |
为了减少烟尘的排放,将烟尘与CO混合后在空气中煅烧,得到铁的氧化物和CaO的烧结物,其中CaO的质量分数为8.92%(金属元素无损耗),烧结物分离出CaO后,铁的氧化物的组成和物质的量之比如何 (若无确定值,请表示某组分物质的量分数的取值范围)?
查看答案和解析>>
科目: 来源: 题型:
钢铁生锈的过程十分复杂,已知某铁锈含有Fe2O3•nH2O(n≤1),还可能有Fe(OH)3和FeCO3。某学习小组做了以下实验:
①取12.574g铁锈隔绝空气加热至恒重,得到固体10.528g。
②另取6.287g铁锈,在205.00 mL 1.000mol/L的稀硝酸中恰好完全溶解,产生NO气体89.60 mL(标准状况)。
(1)根据实验①,铁锈中是否只含Fe2O3•nH2O?试通过计算回答。
(2)根据实验②,能否确定铁锈中含有FeCO3?理由是什么?
(3)若n=0.8,试通过计算确定6.287g铁锈的成分以及它们的物质的量。
查看答案和解析>>
科目: 来源: 题型:
水处理剂能使工业循环冷却系统保持良好状态。以下是两种新型水处理剂的合成方法。
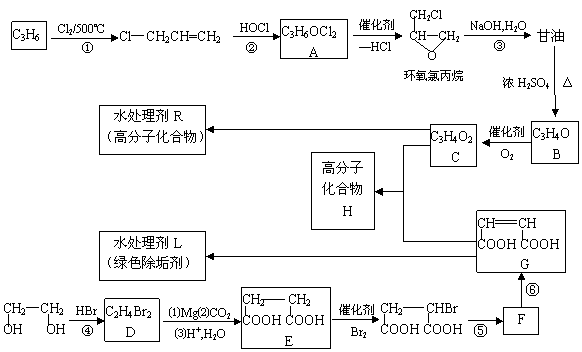 完成下列填空:
完成下列填空:
(1)写出反应类型。反应① 反应② 。
(2)反应④通常用一种盐和一种酸代替HBr参加反应,它们的名称是 和 。
(3)写出化学方程式。
B与新制氢氧化铜反应生成C ;
反应⑤ 。
(4)D转化为E的过程中,E分子中增加的碳原子来源于 ________(写物质的名称)。
(5)写出H的结构简式 。
 (6)E有多种同分异构体,其中能发生银镜反应、能发生缩聚反应,还能两分子生成六元环状化合物的物质的结构简式为 。
(6)E有多种同分异构体,其中能发生银镜反应、能发生缩聚反应,还能两分子生成六元环状化合物的物质的结构简式为 。
查看答案和解析>>
科目: 来源: 题型:
已知:苯环上连有的基团不同时,新的基团可能进入间位,也可能进入邻、对位。
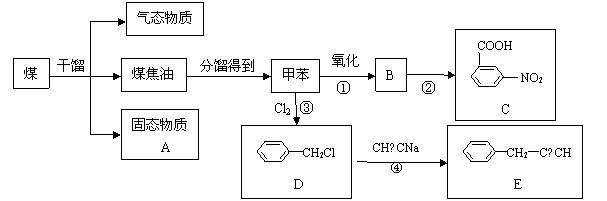
煤是非再生能源,我国煤炭储量占能源总储量约94%。下图是煤干馏得到的主要产物,以及产物之一甲苯的有关反应。回答下列问题:

(1) 煤的干馏是指 。固态物质A是
(写名称),它是冶金工业的重要原料,还用于 (再写一种用途)。
(2)由甲苯制备物质C时,若反应①和②的顺序交换,得到的物质不是C,而可能是 (写结构简式,一种即可)。
(3)反应③的反应条件是 ;反应④是 反应(填反应类型)。
(4)与E含相同基团(苯基和—C≡C—)的E的同分异构体(包括E)共 种。
查看答案和解析>>
科目: 来源: 题型:
某化工厂联合生产纯碱、镁、阻燃剂。以白云石(CaCO3·MgCO3)为原料冶炼镁:经高温煅烧生成的氧化物在还原炉中经1200℃用硅铁还原生成镁蒸汽(铁化合价不变),镁蒸汽经冷凝为粗镁;同时以海水为原料制碱和制阻燃剂。具体流程如下:

![]()
|
|
|
|
|
|
|
|
(1)分别写出A、B、C的化学式 、 、 ;沉淀池中反应的化学方程式是 。
(2)硅铁还原生成镁蒸汽时选择低压和1200℃,试分析选择这种反应条件的原因
。
(3)精制卤水中的MgCl2与适量石灰乳反应生成碱式氯化镁[Mg(OH)Cl]沉淀,此时溶液中主要溶质是(写化学式) 。
(4)描述流程中相关操作Ⅰ包括过滤、 、 。
(5)已知:Mg(OH)2(s)→MgO(s)+H2O(g)-81.5kJ;Al(OH)3(s)→0.5Al2O3(s)+1.5 H2O(g)-87.7kJ
①Mg(OH)2能起阻燃作用,其原因是 。
②等质量Mg(OH)2和Al(OH)3相比,阻燃效果较好的是 。
(6)某化工厂利用上图所示流程联合生产纯碱、镁、阻燃剂,试分析该生产的优点
。
查看答案和解析>>
科目: 来源: 题型:
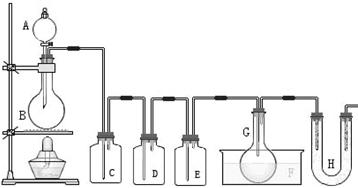
用图示装置制取PCl3,在E中放入足量白磷,将氯气不间断地通入E,氯气与白磷就会发生反应,并放出热量(温度高于75℃)。已知:PCl3和 PCl5遇水强烈反应,
 它们熔沸点数据如下:
它们熔沸点数据如下:
| 熔点 | 沸点 | |
| PCl3 | -112℃ | 75℃ |
| PCl5 | 148℃ | 200℃ |
|
| ||||||
| |||||||
请根据图中装置回答下列问题:
(1)检查该装置气密性的方法是 。
(2)为得到氯气,若B中加入MnO2,则A中应加入 ,反应的化学方程式为___________________________________ 。
(3)若发现C中气泡产生过猛,需要进行的操作或对装置进行的改进是 。
(4)在反应开始时主要生成PCl3,而后来主要生成PCl5,原因可能是 ;从PCl3和PCl5的混合物中分离出PCl3的方法是 (选填序号)。
a.蒸馏 b.过滤 c.分液 d.升华
(5)生成的PCl3在G中收集,则F中盛有 ,作用是___________________________。
(6)C、D、H所盛的试剂分别是(选填序号):C ; D ; H 。
a.饱和食盐水 b.浓硫酸 c.无水氯化钙 d.碱石灰
(7)如果E中反应放热较多,G处的导管可能发生堵塞,其原因是 。
查看答案和解析>>
科目: 来源: 题型:阅读理解
大气固氮(闪电时N2转化为NO)和工业固氮(合成氨)是固氮的重要形式。下表列举了不同温度下大气固氮和工业固氮的部分K值(K表示平衡常数):
| N2+O2 | N2+3H2 | |||
| 温度 | 25℃ | 2000℃ | 25℃ | 400℃ |
| K | 3.84×10-31 | 0.1 | 5×108 | 200 |
(1)固氮是指 的过程,自然界固氮的另一途径为 。
(2)根据表中的数据,并结合所学知识分析,下列说法正确的是 。
a.人类大规模模拟大气固氮实际意义很小
b.常温下,大气固氮与工业固氮完成程度相差很大
c.两种固氮都是放热反应 d.在常温下,大气固氮几乎不可能,而工业固氮很容易进行
(3)为研究反应条件的改变对化学平衡移动的影响,将N2和H2在一固定体积的密闭容器中进行反应,得到如下的图像。下列有关条件改变(每次只改变一个条件)的说法,正确的是 。
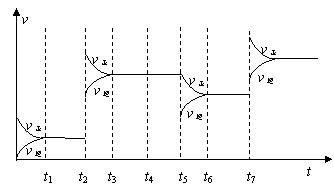 a.t2可能是增加了原料的物质的量
a.t2可能是增加了原料的物质的量
b.t4可能是充入了He气
c.t5是从反应体系中分离出氨气
d.t7时可能是升高温度,使平衡向
正反应方向移动
(4)目前工业固氮采用的是哈伯法,即在
20~50MPa的高压和500℃左右的高温下,并用铁触媒作为催化剂。俄勒冈大学的化学家使用了一种名为trans-Fe(DMeOPrPE)的新催化剂,在常温下合成氨,反应的化学方程式为:N2 +3H2![]() 2NH3 。有关说法正确的是 。
2NH3 。有关说法正确的是 。
a.新法不需要高温条件,可节约大量能源
b.新法能在常温下进行是因为不需要断裂化学键
c.在相同温度下不同的催化剂其催化活性不同
查看答案和解析>>
科目: 来源: 题型:
已知溶液中:还原性HSO3->I-,氧化性IO3-> I2 > SO42-。
在含3 molNaHSO3的溶液中逐滴加入KIO3溶液,加入的KIO3
 和析出的I2的物质的量的关系曲线如右图所示,试回答下列问题:
和析出的I2的物质的量的关系曲线如右图所示,试回答下列问题:
(1)写出a点反应的离子方程式 ;
反应中还原剂是 ;被还原的元素是 。
(2)写出b点到c点反应的离子方程式 。
(3)当溶液中的I-为0.4 mol时,加入的KIO3为 mol 。
(4)若往100 mL1mol/L的KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式为
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com