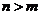+ n HOCH2CH2OH [ OC®D ®DCOOCH2CH2O ]n
+nH2O nHOOC®D ®DCOOH
‘œͫÈ
‘œͫÈ
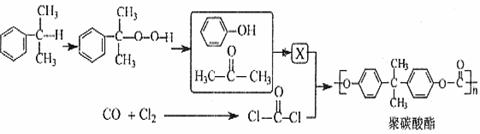
«Î–¥≥ˆ£∫ £®1£©XµƒΩ·ππºÚ Ω___________°£ ‘œͫÈ
£®2£©‘⁄“ª∂®Ãıº˛œ¬X”Î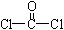 ∑¥”¶∫œ≥…æ€ÃºÀ·ı•µƒªØ—ß∑Ω≥Ã Ω£®≤ª±ÿ–¥∑¥”¶Ãıº˛£©£∫ ∑¥”¶∫œ≥…æ€ÃºÀ·ı•µƒªØ—ß∑Ω≥Ã Ω£®≤ª±ÿ–¥∑¥”¶Ãıº˛£©£∫ _________________________________________________°£ £®3£©X∫Õ≈®‰ÂÀÆ∑¥”¶ ±£¨1mol X◊Ó∂ýœ˚∫ƒBr2__________mol°£ ‘œͫÈ
£®4£© Ù”⁄±ΩµƒÕ¨œµŒÔ£¨”Î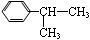 ª•Œ™Õ¨∑÷“Ïππõƒ”–ª˙ŒÔ”– ÷÷°£ ª•Œ™Õ¨∑÷“Ïππõƒ”–ª˙ŒÔ”– ÷÷°£ ∆þ£Æ£®±æÂ∞¸¿®2–°Ã‚£¨π≤18∑÷£© ‘œͫÈ
24£Æ£®6∑÷£©ƒ≥∑ºœ„◊ªØ∫œŒÔ”αΩ∑”ŒÞ¬€“‘∫Œ÷÷±»¿˝ªÏ∫œ£¨÷ª“™◊ÐŒÔ÷ µƒ¡ø“ª∂®£¨ÕÍ»´»º…’ ±À˘œ˚∫ƒµƒ—ı∆¯∫Õ…˙≥…ÀƵƒ÷ ¡ø º÷’“ª∂®°£ ‘ªÿ¥£∫ ¢≈’‚¿ýŒÔ÷ µƒœý∂‘∑÷◊”÷ ¡ø”αΩ∑”µƒœý∂‘∑÷◊”÷ ¡ø÷Æ≤ÓŒ™_________µƒ±∂ ˝£®ÃÓ ˝◊÷£©°£ ‘œͫÈ
¢∆œ÷”–’‚¿ýŒÔ÷ ÷–œý∂‘∑÷◊”÷ ¡ø◊Ó–°µƒŒÔ÷ A£¨“—÷™A»Ð“∫ƒÐ”ÎNaHCO3∑¥”¶∑≈≥ˆ∆¯Ã°£œ÷»°2.32g±Ω∑””ÎAµƒªÏ∫œŒÔ”Î50.0mL1.000mol/LµƒNaOH»Ð“∫≥‰∑÷∑¥”¶∫Û£¨º”ÀÆ÷¡100mL°£»°≥ˆ∆‰÷–µƒ10.0mL”√0.100mol/LµƒHCl»Ð“∫µŒ∂®π˝¡øµƒNaOH£¨œ˚∫ƒ20.0mL ±÷¡µŒ∂®÷’µ„°£«Û∏√ªÏ∫œŒÔ÷–±Ω∑”µƒ÷ ¡ø∑÷ ˝£®Ω·π˚±£¡Ù»˝Œª”––ß ˝◊÷£©°£ ‘œͫÈ
25£Æ£®12∑÷£©ÓÐ(Co)ªØ∫œŒÔ∂‘ªØ—ߺ¸µƒ—–æø∆◊≈÷ÿ“™µƒ◊˜”√°£Œ™≤‚∂®ƒ≥ÓЪØ∫œŒÔ£€Co(NH3)x
Cly£ðClzµƒ◊È≥…£¨Ω¯––»Áœ¬ µ—È£∫ ‘œͫÈ
¢Ÿ
≥∆»°—˘∆∑0.5010g £¨º”»Îπ˝¡øµƒNaOH»Ð“∫£¨÷Û∑–£¨’Ù≥ˆÀ˘”–µƒ∞±£¨¿‰»¥£¨µ√µΩA°£≤˙…˙µƒ∞±”√50.00mL 0.5000mol?L®D1 µƒ—ŒÀ·ÕÍ»´Œ¸ ’≤¢”√’Ù¡ÛÀÆ∂®»ðµΩ100mL,µ√»Ð“∫B£¨»°B»Ð“∫20.00mL , ”√0.1000mol?L®D1 NaOHµŒ∂®£¨œ˚∫ƒNaOH»Ð“∫30.00mL°£ ¢⁄
œÚA÷–º”»Îπ˝¡øµƒKIπÃ㨒ҵ¥£¨—ŒÀ·À·ªØ∫Û÷√”⁄∞µ¥¶£¨∑¢…˙∑¥”¶£∫ Com+ + I®D °˙ Co2+ + I2(Œ¥≈‰∆Ω) ‘œͫÈ
∑¥”¶ÕÍ≥…∫Û£¨’Ù¡ÛÀÆœ° Õ£¨”√Na2S2O3»Ð“∫µŒ∂®Œˆ≥ˆµƒI2£¨œ˚∫ƒ0.1000mol?L®D1Na2S2O3»Ð“∫20.00mL °£∑¥”¶∑Ω≥Ã ΩŒ™£∫I2 + 2Na2S2O3
= 2NaI + Na2S4O6 ‘œͫÈ
¢€
¡Ì≥∆»°∏√ŒÔ÷ —˘∆∑0.2505g£¨»Ð”⁄ÀÆ£¨“‘0.1000mol?L®D1AgNO3»Ð“∫µŒ∂®÷¡«°∫√∑¥”¶ÕÍ»´£¨œ˚∫ƒAgNO3»Ð“∫20.00mL°£œý”¶∑¥”¶ ΩŒ™£∫ £€Co(NH3)x Cly£ðClz +
zAgNO3=£€Co(NH3)x Cly£ð(NO3)z
+ zAgCl°˝ Õ®π˝º∆À„«Û£∫ ¢≈£€Co(NH3)x Cly£ðClz÷–µ™‘™Àÿµƒ÷ ¡ø∑÷ ˝°£ ¢∆∏√ÓЪØ∫œŒÔµƒªØ—ß Ω°£ 2009ΩÏΩ≠À’ °Ã©÷ð –∆⁄ƒ©¡™øº∏þ»˝ªØ—߃£ƒ‚ ‘ ‘œͫÈ
“ª°¢—°‘Ò£®√ø–°Ã‚4∑÷£¨π≤32∑÷£© Â∫≈ 1 2 3 4 5 6 7 8 ¥∞∏ A B C D D B C C ∂˛°¢—°‘Ò£®√ø–°Ã‚4∑÷£¨π≤32∑÷£© Â∫≈ 9 10 11 12 13 14 15 16 ¥∞∏ B BD AD B BD C AD AD »˝°¢£®±æÂ∞¸¿®2–°Ã‚£¨π≤22∑÷£© 17£Æ(√ø–°Ãı2∑÷)£®1£©150mL£¨∆¯ÃÂê˝Œ™110mL£¨¡øÕ≤µƒ¡ø≥Ã‘Ω–°£¨≤˙…˙µƒŒÛ≤Ó‘Ω–°£ª £®2£©À· ΩµŒ∂®πУ¨À·–‘KMnO4æþ”–«ø—ıªØ–‘£¨ƒÐ∏Ø ¥ºÓ ΩµŒ∂®πеƒ»ÈΩ∫πУª £®3£©B£¨∑¿÷π∆¯Ã¿‰»¥ ±∑¢…˙µπŒ¸œ÷œÛ£ª¥À ±∂¡ ˝”…”⁄¡øÕ≤÷–∆¯Ã—π«ø–°”⁄Õ‚ΩÁ¥Û∆¯—𣨠π∂¡µƒ∆¯ÃÂê˝∆´¥Û£¨Na2O2¥ø∂»∆´∏þ£ª”¶¬˝¬˝∞—¡øÕ≤Õ˘œ¬“∆£¨ π¡øÕ≤÷–“∫√Ê«°∫√”ÎÀÆ≤€÷–“∫√Êœý∆Ω£ª £®4£©»Ð“∫∏’∫√≥ˆœ÷«≥◊œ∫Ï…´£¨≤¢‘⁄∞Î∑÷÷”ƒ⁄≤ªÕ …´£ª £®5£©62.4%  18£Æ 18£Æ
Àƒ°¢£®±æÂ∞¸¿®2–°Ã‚£¨π≤18∑÷£© 19£Æ£®1£©S1£æS3£æS2£æS4£®2∑÷£©£®2£©¢Ÿb ¢⁄c £®∏˜1∑÷£¨π≤2∑÷£© £®3£©¢ŸHClO4£®1∑÷£©¢⁄¿Î◊”º¸°¢£®º´–‘£©π≤º€º¸£®1∑÷£© NaClO£®1∑÷£© ¢€SiO2+2C Si+2CO°¸£®1∑÷£© Si+2CO°¸£®1∑÷£© 20£Æ(1)DŒ™FeSO4£®2∑÷£©£¨EŒ™H2S
£®2∑÷£© (2)¿Î◊”∑Ω≥à Ω2Fe3++SO2+2H2O£Ω2Fe2++4H++SO42-£®2∑÷£© (3)¿Î◊”∑Ω≥à Ω2Cu2++2H2O 2Cu+4H++O2°¸£®2∑÷£© 2Cu+4H++O2°¸£®2∑÷£© (4)≥∆“ª∂®¡øµƒCu2S∫ÕCuS≥‰∑÷»º…’£¨‘Ÿ≥∆»º…’∫Ûµƒ≤˙ŒÔ£¨»Ù»º…’∫Ûµƒ÷ ¡ø∫Õ∑¥”¶ŒÔµƒ÷ ¡øœýµ»£¨‘Ú±ª»º…’µƒŒÔ÷ «Cu2S£¨»Ù»º…’∫Ûµƒ÷ ¡ø±»‘≠¿¥µƒ∑¥”¶ŒÔ÷ ¡ø…Ÿ£¨‘Ú±ª»º…’µƒŒÔ÷ «CuS°££®2∑÷£© ŒÂ°¢£®±æÂ∞¸¿®1–°Ã‚£¨π≤10∑÷£© 21£Æ(1)Œ¬∂»…˝∏þ£¨¥ŸΩ¯µÁ¿Î£¨À˘“‘K÷µ‘ˆ¥Û£®2∑÷£© (2)K÷µ‘Ω¥Û£¨µÁ¿Î≥ˆµƒ«‚¿Î◊”≈®∂»‘Ω¥Û£¨À˘“‘À·–‘‘Ω«ø£®2∑÷£© (3)H3PO4 HPO42®D£®2∑÷£© (4)K1£∫K2£∫K3°÷1£∫10®D5£∫10®D10 £®2∑÷£© …œ“ªº∂µÁ¿Î≤˙…˙µƒH+∂‘œ¬“ªº∂µÁ¿Î”–“÷÷∆◊˜”√ £®2∑÷£© ¡˘°¢£®±æÂ∞¸¿®2–°Ã‚£¨π≤18∑÷£©   22£Æ£®8∑÷£©£®I£©C2nH3nPn
°£ 22£Æ£®8∑÷£©£®I£©C2nH3nPn
°£
£®II£©C20H30O2£¨ 23£Æ£®10∑÷£© (1) (3∑÷)
(2)¬‘(3∑÷) (3)4(2∑÷)
(4)7(2∑÷) (3∑÷)
(2)¬‘(3∑÷) (3)4(2∑÷)
(4)7(2∑÷)
∆þ°¢£®±æÂ∞¸¿®2–°Ã‚£¨π≤18∑÷£© 24£Æ£®6∑÷£©(1)44 £®2∑÷£© (2)A∑÷◊”÷–∫¨“ª∏ˆÙ«ª˘∫Õ“ª∏ˆÙ»ª˘£¨1molAœ˚∫ƒ2molNaOH n(HCl)= 0.02 L°¡0.100mol/L= 0.002mol £®1∑÷£© °£±Ω∑””ÎAµƒªÏ∫œŒÔœ˚∫ƒµƒNaOHŒÔ÷ µƒ¡øŒ™£∫0.05L°¡1.000mol/L®D0.002mol°¡ =0.03mol £®1∑÷£© “¿Ã‚“‚ø…µ√£∫ =0.03mol £®1∑÷£© “¿Ã‚“‚ø…µ√£∫  n(C6H5OH)+2°¡n(A)=0.03mol n(C6H5OH)+2°¡n(A)=0.03mol
94 g/mol°¡n(C6H5OH)+138g/mol°¡n(A)=2.32 g n(C6H5OH)=0.01mol m(C6H5OH)=0.94g w (C6H5OH)= °¡100%=40.5%£®ªÚ0.405£© £®2∑÷£© °¡100%=40.5%£®ªÚ0.405£© £®2∑÷£© 25£Æ¢≈£®π≤4∑÷£©NaOH+HCl=NaCl+H2O NH3+HCl=NH4Cl 20.00mLB»Ð“∫œ˚∫ƒ0.1000mol?L-1NaOH 30.00mL°£ 20.00mLB»Ð“∫÷–π˝¡øµƒHCl£∫n(HCl)=0.003000mol°°, 100mL£¬»Ð“∫÷–π˝¡øµƒHCl£∫n(HCl)=0.01500molƒ«√¥”ÎNH3∑¥”¶µƒn(HCl)=0.01000mol π 0.5010g—˘∆∑÷–
n(NH3)=0.01000mol
n(N)=0.01000mol£®2∑÷£© £€Co(NH3)xCly£ðClz÷–µ™‘™Àÿµƒ÷ ¡ø∑÷ ˝  £®2∑÷£© £®2∑÷£©
¢∆£®π≤6∑÷£©I2+2Na2S2O3==2NaI+Na2S4O6 “Ú∑¥”¶”√»•0.1000mol?L-1Na2S2O3»Ð“∫20.00mL£¨Õ∆À„≥ˆ£∫n(I2)=0.001000mol£®1∑÷£© Co”Σ∆eÕ¨“ª◊£¨Com+æþ”–«ø—ıªØ–‘£¨π …Ëm=3 ‘Ú”–£∫2Co3++2I-==2Co2++I2 n(Co3+)=0.002000mol £®1∑÷£© 0.5010g—˘∆∑÷–Clµƒ◊Ð÷ ¡øŒ™£∫ m(Cl)=0.5010g-0.002000molx59g?mol -1-0.01000molx17g ?mol
-1=0.2130g n(Cl)=0.006000mol£®1∑÷£© ”÷”–£∫£€Co(NH3)xCly£ðClz+zAgNO3==£€Co(NH3)xCly£ð(NO3)z+zAgCl°˝ 0.2505g—˘∆∑¿©¥Û“ª±∂¿¥À„£®º¥”√0.5010g£©Õ∆À„≥ˆ£∫ ∑¥”¶œ˚∫ƒAgNO3£∫n£®AgNO3£©£Ω0.1000mol?L-1x40.00mL=0.004000mol º¥∑¢…˙…œ ˆ∑¥”¶µƒCl-Œ™£∫n(Cl-)
=0.004000mol£®1∑÷£© ‘Ú”– y:z=£®0.006000mol-0.004000
mol£©: 0.004000mol=1:2 Õ¨ ±ªπ”–£∫1£∫x:(y+z)= 0.002000: 0.01000:
0.006000=1:5:3 Ω‚µ√£∫x=5 y=1 z=2 ¥¯»Î£€Co(NH3)xCly£ðClz÷–£¨«Ûµ√CoªØ∫œº€Œ™£∫+3 ºŸ…Ë≥…¡¢ ∏√ÓЪØ∫œŒÔµƒªØ—ß ΩŒ™£∫£€Co(NH3)5Cl£ðCl2£®3∑÷£© ¥£∫¢≈£€Co(NH3)xCly£ðClz÷–µ™‘™Àÿµƒ÷ ¡ø∑÷ ˝Œ™27.94% ¢∆∏√ÓЪØ∫œŒÔµƒªØ—ß ΩŒ™£∫£€Co(NH3)5Cl£ðCl2
| 
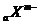 ∫Õ
∫Õ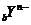 æþ”–œýÕ¨µƒµÁ◊”≤„Ω·π𣨻Ù
æþ”–œýÕ¨µƒµÁ◊”≤„Ω·π𣨻Ù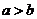 £¨‘Ú
£¨‘Ú