
浙江省温州中学
理科综合能力测试
本试卷分第I卷(选择题)和第II卷(非选择题)两部分,共300分。考试时间150分钟。
注意事项:
1.答第I卷前,考生务必将班级、姓名、学号填写在答题卷上。
2.每小题选出答案后,填写在答题卷上,不能答在试题卷上
可能用到的相对原子质量: H―1、C―12、Na―23、O―16、S―32、Fe―56、Ba―137
第I卷(本卷共21小题,共126分。)
一、选择题(本题包括13小题。每小题只有一个选项符合题意)
1.据报道,2004年4月,日本科学家依靠转基因技术使甲鼠的卵子带上“雄性遗传标记”,
再用这种“卵细胞”的“核”替代精子移植到乙鼠的卵子中,使其“受精”,结果成功繁育出没有父亲的老鼠――“辉夜姬”。则“辉夜姬”是
A.单倍体 B.性状与甲鼠几乎完全一样
C.只有一条性染色体 D.染色体数与正常鼠相同
2.某细菌多肽分子式C41H54O15N8,已知将它水解后只得到4种氨基酸:甘氨酸(C2H5O2N),丙氨酸(C3H7O2N),谷氨酸(C5H9O4N),苯丙氨酸(C9H11O2N)。已知谷氨酸中有2个羧基, 据氧原子数来推断,该多肽化合物中羧基数、氨基数、及合成该多肽的信使RNA中决定氨基酸的密码子数分别是
A.4、1、8 B.1、1、
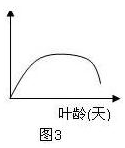 3.下图横坐标表示叶龄(用天数表示),根据此曲线表示的变化趋势,纵坐标可以表示
3.下图横坐标表示叶龄(用天数表示),根据此曲线表示的变化趋势,纵坐标可以表示
①光合作用速率 ②对二氧化硫的抗性 ③钙的总含量 ④叶绿素的总含量 ⑤镁的总含量
A.①②③④⑤ B.①②④⑤
C.①④⑤ D.①③⑤
4.下列叙述,有几项是正确的
①DNA的组成元素是C、H、O、N、P,有的含有S
②某细菌在缺Zn2+的培养基中不能生长,而加入Zn2+又能生长,则Zn2+是该细菌的生长因子
③质粒是环状单链DNA分子
④真核细胞基因中外显子的碱基数比内含子多1个
⑤人体不分裂的胰岛细胞和不分裂的口腔上皮细胞比较,核内DNA含量和细胞质中RNA含量均相同
⑥口腔上皮细胞与胰岛细胞中表达的基因全都不同
A.一项 B.二项 C.三项 D.都不正确
5.下列关于生态系统的叙述,正确的是
A.真正被植食性动物吃掉的那部分绿色植物大部分被初级消费者所同化
B.能量只能在食物链中流动
C.年龄组成只能通过影响出生率来影响种群数量
D.通过兔子的粪便流入到分解者体内的能量属于兔子同化作用所获得能量的一部分。
6.下列说法不正确的是
①一种元素只有一种原子,但可能有多种离子;②阴离子或阳离子有可能既有氧化性也有还原性;③由同种元素组成的物质属于单质;④有新单质生成的化学反应不一定是氧化还原反应;⑤具有相同质子数的粒子都属于同种元素。
A.①③⑤ B.①②③ C.③④⑤ D.①③④
7.以NA 表示阿伏加德罗常数,下列说法正确的是
A.某温度时,pH=6纯水中,含10-6NA个OH-
B.如果
C.常温常压下,
D.
8.A、B、C为第二、第三周期的元素A、B在同周期,A、C最低价离子分别为A2-和C-,B2+和C-具有相同的电子层结构。下列说法中,正确的是
 A.原子核外最外层电子数:A>C>B B.离子半径:A2->C->B2+
A.原子核外最外层电子数:A>C>B B.离子半径:A2->C->B2+
C.B和C形成化合物的电子式为B2+[:C:]2 D.稳定性:HC<H
9.下列各组离子能大量共存,当溶液中c(H+)=10-1 mol?L-1时,有气体产生;而当溶液中c(H+)=l0-13 mol?L-1时,又能生成沉淀。该组离子可能是
A.Na+、Cu2+、NO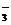 、CO
、CO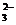 B.Ba2+、K+、Cl-、HCO
B.Ba2+、K+、Cl-、HCO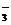
C.Fe3+、Na+、SO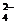 、I- D.Mg2+、NH
、I- D.Mg2+、NH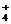 、SO
、SO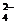 、Cl-
、Cl-
10.下列论述中,不正确的是
A.C2H5Br与NaOH溶液混合振荡后,先加入适量硫酸酸化再加入AgNO3溶液,以检验Br―离子
B.用标准盐酸滴定未知浓度 溶液,滴定前仰视读数,滴定后俯视读数,会使计算结果偏低
溶液,滴定前仰视读数,滴定后俯视读数,会使计算结果偏低
C.工业硫酸生产吸收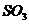 时,
时,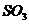 从吸收塔底部通入,98.3%的硫酸从塔顶喷下,剩余气体从塔上部放出
从吸收塔底部通入,98.3%的硫酸从塔顶喷下,剩余气体从塔上部放出
D.新型无机非金属材料继承了传统无机材料的许多优点,而且还克服了传统无机材料的某些缺点。
11.不久前,美国一个海军航空站安装了一台250kW的MCFC型燃料电池,该电池可同时供应电和水蒸气,其工作温度为
A.正极反应为: O2+2H2O+4e-==== 4OH-
 B.负极反应为:H2 + CO32--2e-====H2O + CO2
B.负极反应为:H2 + CO32--2e-====H2O + CO2
C.电池供应1 mol 水蒸气,转移的电子数2 mol
D.放电时CO32-向负极移动
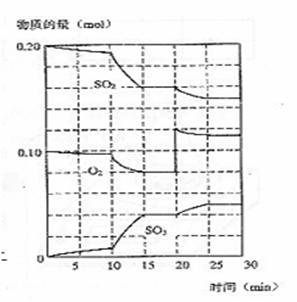
12.
①加了催化剂 ②缩小容器体积 ③降低温度 ④增加SO3的物质的量
A.②③ B. ①③ C.①② D.③④
13.
A.a可能等于1 B.a一定大于2
C.a一定等于2 D.a一定小于2
二、选择题(本题包括8小题。在每小题给出的四个选项中,有的小题只有一个正确选项正确,有的小题有多个选项正确。全部选对的得6分,选对但不全的给3分,有选错或者不答得0分)
14.
A.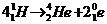 ;
B.
;
B.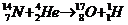 ;
;
C.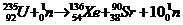 ; D.
; D.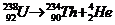 。
。
15.在防治“非典”期间,在机场、车站等交通出入口,使用了红外线热像仪.红外线热像仪通过红外线遥感,可检测出经过它时的发热病人,从而可以有效控制疫情的传播.关于红外线热像仪,下列说法正确的是
A.选择红外线进行检测,主要是因为红外线光子能量小,可以节约能量
B.红外线热像仪通过发射红外线照射人体来检测
C.红外线热像仪同时还具有杀菌作用
D.一切物体都能发射红外线,而且物体在不同温度下发射的红外线的频率和强度不同
16.下列叙述正确的是
A.物体温度升高,物体中分子热运动加剧,每个分子的热运动动能都会增大
B.对气体加热,气体的内能一定增大
C.物体的温度不变,其内能可能发生变化
D.布朗运动就是分子无规则的热运动
17.2004年,我国和欧盟合作正式启动伽利略卫星导航定位系统计划,这将结束美国全球卫星定位系统(GPS)一统天下的局面。据悉,“伽利略”卫星定位系统将由30颗轨道卫星组成,卫星的轨道高度为2.4×
A.替补卫星的周期大于工作卫星的周期,速度大于工作卫星的速度
B.替补卫星的周期大于工作卫星的周期,速度小于工作卫星的速度
C.替补卫星的周期小于工作卫星的周期,速度大于工作卫星的速度
D.替补卫星的周期小于工作卫星的周期,速度小于工作卫星的速度
 18.现在高速公路上的标志牌都用“回归反光膜”制成,夜间行车时,它能把车灯射出的光逆向返回,标志牌上的字特别醒目。这种“回归反光膜”是用球体反射原件制成的,如图所示,反光膜内均匀分布着直径为10µm的细玻璃珠,所用玻璃的折射率为
18.现在高速公路上的标志牌都用“回归反光膜”制成,夜间行车时,它能把车灯射出的光逆向返回,标志牌上的字特别醒目。这种“回归反光膜”是用球体反射原件制成的,如图所示,反光膜内均匀分布着直径为10µm的细玻璃珠,所用玻璃的折射率为 ,为使入射的车灯光线经玻璃珠折射→反射→再折射后恰好和入射光线平行,则第一次入射时的入射角应是
,为使入射的车灯光线经玻璃珠折射→反射→再折射后恰好和入射光线平行,则第一次入射时的入射角应是
A.15° B.30°
C.45° D.60°
 19.如图所示,在双人花样滑冰运动中,有时会看到被男运动员拉着的女运动员离开地面在空中做圆锥摆运动的精彩场面,目测体重为G的女运动员做圆锥摆运动时和水平冰面的夹角约为30°,重力加速度为g,估算该女运动员
19.如图所示,在双人花样滑冰运动中,有时会看到被男运动员拉着的女运动员离开地面在空中做圆锥摆运动的精彩场面,目测体重为G的女运动员做圆锥摆运动时和水平冰面的夹角约为30°,重力加速度为g,估算该女运动员
A.受到的拉力为 G
B.受到的拉力为
G
B.受到的拉力为
 C.向心加速度为
C.向心加速度为 g
D.向心加速度为
g
D.向心加速度为
20.如图所示为一列简谐横波t时刻的图象,已知波速为
A.经过0.5s,质点a、b、c通过的路程均为
B.从t时刻起质点a比质点b先回到平衡位置, 则波沿x轴正方向传播
C.图示时刻质点a、b、c所受的回复力大小之 比 为2∶1∶3
D.振源的振动频率为2.5Hz
 21.如图所示,在同时存在匀强磁场的空间中取正交坐标系Oxyz(z轴正
21.如图所示,在同时存在匀强磁场的空间中取正交坐标系Oxyz(z轴正
方向竖直向上),一质量为m、电荷量为q的带电正电粒子(重力不能
忽略)从原点O以速度 v沿x轴正方向出发。下列说法正确的是)
A.若电场、磁场分别沿z轴正方向和x轴正方向,粒子只能做曲线运动
B.若电场、磁场均沿z轴正方向, 粒子有可能做匀速圆周运动
C.若电场、磁场分别沿z轴正方向和y轴负方向,粒子有可能做匀速直线运动
D. 若电场、磁场分别沿y轴负方向和z轴正方向,粒子有可能做平抛运动
第Ⅱ卷(本卷共10小题,共174分)
22.(17分)
⑴(5分)“验证动量守恒定律”的实验装置原来的教科书采用图(甲)的方法,经过编者修改后,现行的教科书采用图(乙)的方法,两个实验装置 的区别在于①悬挂重垂线的位置不同;②图(甲)中设计有一个支柱(通过调整,可使用两球的球心在同一水平线上;上面的小球被碰离开后,支柱立即倒下),图(乙)中没有支柱。对于图(甲)入射小球和被碰小球做平抛运动的抛出点分别在通过O,O′点的竖直线上,重垂线只确定了O点的位置。
|