
2006-2007学年度潍坊市诸城九年级下学期
单元过关考(三)
可能用到的相对原子质量:H一1 C一12 O一16 Na一23 Cl一35.5 Fe一56 A1一27
Ca一40 Mg一24 Zn一65
一、选择题(本题包括5小题,每小题2分,共10分。每小题只有一个选项符合题意)
1.我国已启动“嫦娥工程”探月工程,拟于2007年前发射绕月飞行的探测卫星――“嫦娥一号”。人类探月的重要目的之一是勘察、获取地球上蕴藏量很小而月球上却极为丰富的核聚变燃料――“He一3”,解决地球能源危机。已知“C一13”是指原子核内含有6个质子、7个中子的碳原子,则“He一3”所指的氦原子核内 ( )
A.含有3个质子,没有中子 B.含有2个质子,l个中子
C.含有1个质子,2个中子 D.含有3个中子,没有质子
2.何洁同学学习化学后,对装修新房的爸爸说:“如果厨房不装抽油烟机家具将会沾满油渍。”何洁同学这样说的依据是 ( )
A.分子很大 B.分子之间有间隔
C.分子在不断运动 D.分子可以分成原子
3.下列变化中属于物理变化的是 ( )
A.将石油加热炼制,以得到多种石油化工产品
B.不小心将食醋洒落在大理石地面上,大理石地面被腐蚀
C.用铝制容器盛放酸性食物,铝制容器被腐蚀
D.把秸杆、杂草、人畜粪便放在密闭的沼气池中发酵制沼气
4.“群众利益无小事,食品安全是大事”。下列会导致食品对人体健康有害的做法是 ( )
A.用蔗糖做食品的甜味剂 B.用甲醛溶液浸泡水产品
C.用干冰保藏易腐败的食品 D.用袋装生石灰做饼干类食品的干燥剂
5。今年,我国世界水日的宣传主题为“转变用水观念,创新发展模式”。围绕这一主题采取的措施不合理的是 ( )
A.将工业用水重复使用
B.农田灌溉改大水漫灌为喷灌或滴灌
C.将对污水的处理再使用改为对地下水的大量开采
D.将不间断注水的洗衣机换成分段注水的洗衣机
二、选择题(本题包括l2小题,每小题3分,共36分。每小题只有一个选项符合题意)
6.白蚂蚁会蛀蚀木头,它分泌的蚁酸是一种酸,还能腐蚀很多建筑材料。下列建筑材料最不易被白蚂蚁腐蚀的是 ( )
A.铜塑像 B.钢筋
C.大理石 D.铝合金
7.粒度在 范围内的材料叫做纳米材料,它能实现意想不到的变化。如纳米铜颗粒一遇到空气就会剧烈燃烧,甚至发生爆炸。下列说法正确的是
( )
范围内的材料叫做纳米材料,它能实现意想不到的变化。如纳米铜颗粒一遇到空气就会剧烈燃烧,甚至发生爆炸。下列说法正确的是
( )
A.纳米铜与普通铜所含铜原子的种类不同
B.纳米铜属于化合物
C.纳米铜颗粒比普通铜更容易与氧气反应
D.纳米铜无需密封保存
8.化学实验中有一种加热方法叫“热水浴”(如图所示)。针对这种加热方式,下列说法错误的是 ( )
A.试管内试剂受热温度不超过100℃
B.试管内试剂受热比较均匀(与用酒精灯直接加热相比)
C.试管底部不能接触到烧杯底部
D.将烧杯内的水换成食盐水,试管内试剂受热温度仍然不会高于l00℃

9.下图是某固体物质的溶解度曲线图,对于该物质,下列说法不正确的是 ( ) 
A.A点的溶液是不饱和溶液
B.50℃时的溶解度大于20℃时的溶解度
C.将A点溶液降温至20℃时,将有晶体析出
D.A、B点比较,B点溶液的溶质质量分数较大
10.有M、N、X、Y四种物质,在一定条件下充分反应后,测得反应物和产物在反应前后的质量如下表所示:
物质
M
N
X
Y
反应前/g
2
20
34
0
反应后
2
38
0
16
对该反应下列说法错误的是 ( )
A.该反应生成N、Y的质量比为9:8 B.该反应属于化合反应
C.该反应中M可能作催化剂 D.该反应属于分解反应
11.已知甲烷( )与氧气反应的产物是
)与氧气反应的产物是 和
和 ,氯气(
,氯气( )和氧气一样,都是活泼的非金属单质。在一定条件下,甲烷和充足的氯气反应,推测其产物是
( )
)和氧气一样,都是活泼的非金属单质。在一定条件下,甲烷和充足的氯气反应,推测其产物是
( )
A. 和HCl
B.
和HCl
B. 和
和
C. D.C和HCl
D.C和HCl
12.在一定条件下,置于密闭容器中的下列各种物质,充分反应后,再冷却至室温,密闭容器中有气态物质且属于纯净物的是 ( )
A.质量比为1:4的 和
和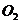 B.质量比为3:9的C和
B.质量比为3:9的C和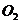 ,
,
C.质量比为1:8的 和
和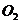 D.质量比为7:2的CO和
D.质量比为7:2的CO和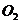
13.下表是小明制定的食物谱,为使营养均衡,在“你的补充”栏可以选填的食物是( )
主食
米饭、馒头
副食
烧鸡块、咸鸭蛋、红烧鱼、花生米
饮料
牛奶
你的补充
A.凉拌黄瓜 B.糖醋鱼 C.肉丝豆腐 D.蛋糕
14.类推是化学学习中常用的思维方法。现有以下类推结果:
①酸碱中和反应生成盐和水,所以生成盐和水的反应一定是中和反应;
②碱的水溶液显碱性,所以碱性溶液一定是碱溶液;
③氧化物都含有氧元素,所以含有氧元素的化合物一定是氧化物;
④有机物都含有碳元素,所以含有碳元素的化合物都是有机物,其中错误的是 ( )
A.只有① B.只有①②③
C.只有②③④ D.全部
15.一定条件下,在托盘天平的左右两盘上各放一只烧杯,均加入质量分数相同、体积相等的稀盐酸,调整天平呈平衡状态。下列实验操作,最终能使天平保持平衡的是 ( )
A.向左右两烧杯中分别加入5.6gFe和1.89A1,两种金属完全溶解
B.向左右两烧杯中分别加入质量相等的Al、Zn,两种金属完全溶解
C.向左右两烧杯中分别加入质量相等的Fe、CaO,反应后盐酸有剩余
D.向左右两烧杯中分别加入质量相等的Mg、Al,反应后两种金属均有剩余
16.小李家地处少雨的高寒山区,种的庄稼生长不茂盛,叶色偏黄,且籽粒不饱满,小李学了化学知识后,帮助父母科学种田,建议父母买化肥改善现状,以获得好的收成,他应向父母提出买的化肥是 ( )
A.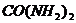 B.
B.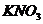
C.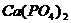 D.
D.
17.过氧化氢( )是一种无色液体,易分解为水和氧气,常用作氧化剂、漂白剂和消毒剂。为了贮存、运输、使用的方便,工业上将过氧化氢转化为固态的过碳酸钠晶体(
)是一种无色液体,易分解为水和氧气,常用作氧化剂、漂白剂和消毒剂。为了贮存、运输、使用的方便,工业上将过氧化氢转化为固态的过碳酸钠晶体( ),该晶体具有碳酸钠和过氧化氢的双重性质。接触下列物质不会使过碳酸钠失效的是
( )
),该晶体具有碳酸钠和过氧化氢的双重性质。接触下列物质不会使过碳酸钠失效的是
( )
A.二氧化锰 B.硫酸铜
C.盐酸 D.氯化钠
三、(本题包括4小题,每空2分,共26分)
18.(6分)春节燃放烟花爆竹是我国的传统习俗。2006年春节,不少城市开始解禁烟花爆竹的燃放,使今年烟花爆竹的燃放量明显增加。
(1)以氯酸钾为原料生产的劣质烟花爆竹极不安全,容易引起爆炸。在氯酸钾中氯元素的化合价为___;
(2)一种焰火药剂的组成中含有硝酸铜,当火药燃烧时,可以产生绿色火焰,反应的化学方程式为 ,试推断X的化学式为___;
,试推断X的化学式为___;
(3)燃放烟花爆竹给节日增添喜庆气氛的同时,也给我们的生活带来一些负面影响。请写出一条可能造成的负面影响________________________。
19.(6分)请分别用一种试剂,除去下列各组物质中的杂质:
(1)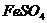 溶液中混有少量的
溶液中混有少量的 ___;
___;
(2) 中混有少量的
中混有少量的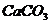 ;___;
;___;
(3)KCl溶液中混有少量的 ___。
___。
20.(6分)高致病禽流感病毒正威胁着人类的健康和安全,对抗禽流感病毒是人类的重大
课题。“达菲”是目前世界上对抗禽流感病毒的良药,生产“达菲”的主要原料是莽草酸,莽草酸的化学式是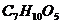 。请根据信息回答:
。请根据信息回答:
(1)莽草酸由___元素组成(填元素名称);
(2)莽草酸属于___(填“有机物”或“无机物”);
(3)莽草酸中氢、氧元素质量之比为___。
21.(8分)甲、乙、丙是初中化学中常见的物质,其转化关系如下图所示:

(1)若甲、乙组成元素相同,甲、乙、丙中有一种物质为水,则甲的化学式为___;实验室制丙的化学方程式为__________________
(2)若甲、乙、丙都含有三种元素,甲、乙、丙的相对分子质量依次增大,其中一种物质广泛应用于玻璃、造纸、纺织和洗涤剂的生产。由甲到乙反应的化学方程式为____________;乙也可以转化成甲,其反应的化学方程式为__________________。
四、(本题包括2小题,20分)
22.(10分)有一包粉末,可能由 ,
, ,NaCl、
,NaCl、 、
、 中的一种或几种组成。为测定其成分,一位同学进行如下实验:
中的一种或几种组成。为测定其成分,一位同学进行如下实验:
(1)取少量粉末加入足量水中,产生白色沉淀,过滤;
(2)往沉淀中加入足量盐酸,沉淀全部溶解且放出气泡;
(3)取(2)中溶解后的溶液加入足量NaOH溶液,产生白色沉淀。由上述实验可以确定这包粉末一定有____________,还不能确定的是____________。
根据你的推测,请帮助该同学继续实验,以确定这包粉末的组成:(按你的实际需要做实验,不一定填满,要求每一个实验确定一种物质)
实验操作
实验现象
实验结论
实验一
实验二
实验三
23.(10分)神舟六号载人飞船成功返航,标志着我国已跨入航天领域国际领先行列。某研究性学习小组查阅资料得知,宇宙飞船中可用超氧化钾( )作为氧气再生剂。超氧化钾是一种固体,它与人呼出的二氧化碳反应生成氧气
)作为氧气再生剂。超氧化钾是一种固体,它与人呼出的二氧化碳反应生成氧气 。为了验证这个反应能够产生氧气,该小组同学以大理石和盐酸反应生成的
。为了验证这个反应能够产生氧气,该小组同学以大理石和盐酸反应生成的 来与
来与 反应制取
反应制取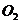 ,设计了如图所示的实验装置:
,设计了如图所示的实验装置:

(1)C处应从A、B两种装置中选择 作为 的发生装置。检查G中集气瓶内收集的气体是否为氧气,可以在取出集气瓶后,用_______________检验。
的发生装置。检查G中集气瓶内收集的气体是否为氧气,可以在取出集气瓶后,用_______________检验。
(2)已知 不溶于饱和碳酸氢钠溶液,D装置的作用是__________。
不溶于饱和碳酸氢钠溶液,D装置的作用是__________。
(3)为了除去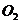 中可能混有的
中可能混有的 ,F中可盛放过量的_______溶液。
,F中可盛放过量的_______溶液。
(4)有同学提出,上述实验能生成氧气可能与 中混有的水蒸气有关。若要检验干燥的
中混有的水蒸气有关。若要检验干燥的 能否与超氧化钾反应生成氧气,你对上述实验装置的改进方法是_____________________________________________。
能否与超氧化钾反应生成氧气,你对上述实验装置的改进方法是_____________________________________________。
五、(本题包括l小题,共8分)
24.(7分)某课外活动小组为了测定铜铁合金中铁的质量分数,现取铜铁合金样品20.0g,将80.0g稀硫酸平均分成4份,分4次逐渐加入到样品中,每次充分反应测得剩余固体质量见下表:
次数
1
2
3
4
加入稀硫酸质量/9
20.0
20.0
20.0
20.0
剩余固体质量/g
17.2
14.4
13.0
13.0
试求:(1)20.0g铜铁合金中,铜的质量为___g。
(2)铜铁合金中,铁元素的质量分数___。
(3)20.0g稀硫酸中溶质的质量分数。
附加题(本题包括l小题,共l0分,计入总分,但整卷总分不抄过100分)
研究性学习:探究实验室中久置的NaOH的变质程度。[研究方案]先称取13.3gNaOH的样品(杂质为 ),配成溶液,然后向溶液中逐滴加入质量分数为14.6%的稀盐酸,根据生成的
),配成溶液,然后向溶液中逐滴加入质量分数为14.6%的稀盐酸,根据生成的 的质量测定
的质量测定 的质量。从而进一步确定样品中NaOH的变质程度。 [解决问题]实验测得加入稀盐酸的质量与产生
的质量。从而进一步确定样品中NaOH的变质程度。 [解决问题]实验测得加入稀盐酸的质量与产生 气体的质量关系如图所示。
气体的质量关系如图所示。

填写下表:(计算结果保留小数点后一位)
 的质量/g
的质量/g
变质NaOH的质量/g
NaOH的变质程度(用质量分数表示)
[继续探究]求实验过程中与NaOH反应所用盐酸的质量 。
[发现问题]根据“与NaOH反应所用盐酸的质量”,对照图像,你发现了什么问题?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com