|
试题详情
14.
以下说法不正确的是 ① 有单质和化合物生成的反应一定是置换反应 ② 通过化合、分解、置换和复分解反应均可制得水 ④ 棉花、羊毛、塑料和天然橡胶等均属于天然有机高分子材料 A. ①②
B. ③④
C. ①③④
D. ①②③④ 试题详情
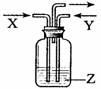
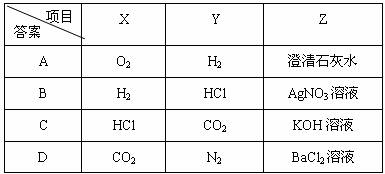
③ 凡均一、稳定、透明、澄清的液体一定是溶液 15. 向下表的甲物质中逐滴加入相应的乙溶液至过量,反应过程中生成气体或沉淀的质量与加入乙的质量关系,能用下图曲线表示的是 试题详情
试题详情
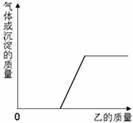
A. ②⑤ B.①③④ C.①②④ D. ①③⑤ 第Ⅱ卷(非选择题 共70分) 试题详情
二、(本题包括5小题,共22分) 16.(6分)生活处处有化学,现有以下常见的物质: A.生石灰 B.稀盐酸 C.天然气 D.聚乙烯 E.活性炭 F.维生素C 请按要求填空(填字母): (1)目前我市正在推广使用的清洁燃料是 ;(2)常用于防毒面具的是 ; (3)可作食品干燥剂的是________;
(4)可除铁锈的是 ; (5)可作食品包装材料的是 ;
(6)有抗坏血病功能的是 。 试题详情
试题详情
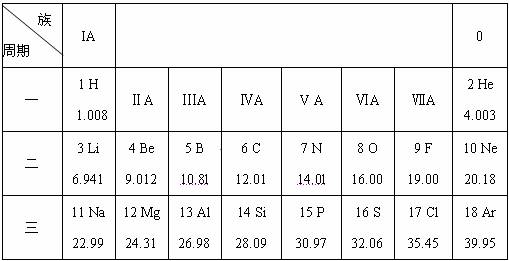
(1)12号元素的元素符号为 ;Be元素的相对原子质量为
。 试题详情
(2)相对原子质量为22.99的元素属 (填“金属”或“非金属”);Ne的化学性质_______;F元素最外层电子数为
。 (3)表中不同种元素最本质的区别是 (填字母)。 A.质子数不同 B.相对原子质量不同 C.中子数不同 试题详情
(4)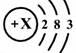 为某元素的原子结构示意图,该元素位于周期表中第
周期第ⅢA族。 为某元素的原子结构示意图,该元素位于周期表中第
周期第ⅢA族。 试题详情
试题详情
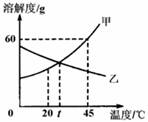
(1)t℃时,甲、乙的溶解度 (填“相等”或“不等”)。 (2) 45℃时,甲的饱和溶液中溶质和溶剂的质量比为______。 (3)45℃时,将乙的饱和溶液(无固体)降温至t℃,此过程是否有晶体析出?
(填“有”或“没有”)。 试题详情
19.(3分) 下图是一个具有刻度和活塞可滑动的玻璃容器,其中有空气和足量的白磷,将它放在盛有沸水的烧杯上方,进行实验。请完成实验报告: 试题详情
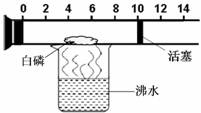
实验目的 实验现象 实验结论 测定空气中 的体积分数。 白磷着火燃烧,活塞先右移,后左移,最后停在刻度约为 (填整数)的位置上。 空气的成分按体积计算, 约占1/5。 试题详情
20.(3分) “安全重于泰山”,依据规定,凡易燃、易爆及具有腐蚀性的物品均不能携带上火车或公共汽车。浓硫酸、汽油、爆竹均不能携带上火车或公共汽车,是因为它们分别属于 、
、
物质。 试题详情
三、本题包括4小题,共21分) 21.(6分) 按要求完成以下化学方程式: (1)实验室制取二氧化碳:
。 (2)属于置换反应:
。 (3)工业制取硝酸的其中一步反应是NH3与O2在催化剂和加热条件下,反应生成NO和H2O:
。 试题详情
22.(5分) 制豆腐是中国古代的一项重要发明,现豆腐在全球已成为颇受欢迎的食品,其制作的主要工艺流程通常如下: 试题详情
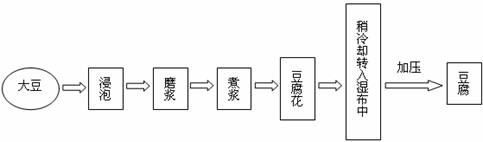
【资料】 下表是豆腐中主要成分的平均质量分数: 成 分 水 蛋白质 脂肪 糖类 钙 磷 铁 维生素B1 维生素B2 质量分数/
% 试题详情
试题详情
试题详情
试题详情
试题详情
试题详情
试题详情
试题详情
试题详情
0.00003 (1)上述工艺流程中,磨浆属于
变化,由豆腐花制豆腐的过程就是将豆腐与水分离,该设计利用的操作是
。 (2)除水、无机盐和维生素外,豆腐中还含的营养素有
,含人体所需的微量元素是
。 (3)除大豆外,很多食物也能提供丰富的蛋白质。下列能提供丰富蛋白质的食物有 (填字母)。 A.萝卜 B. 鱼 C. 大米 D. 奶制品 E. 花生油 F. 苹果 试题详情
23.(6分) 有A、B、C、D、E五种化合物,A为白色固体,B为无色无味的气体,E为不溶于稀硝酸的白色沉淀,它们的关系如下图: 试题详情
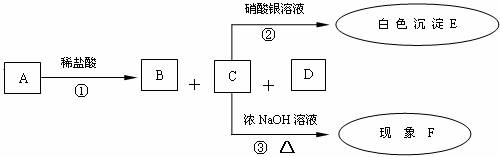
请填空: (1)白色沉淀E为
。 (2)若现象F为“无明显变化”,则A的化学式可能为
(填字母)。 a. Na2CO3
b. MgCO3 c.
KHCO3 (3)若现象F为“无色有刺激性气味的气体”,则A可能为
(填化学式),反应③的化学方程式为
。 试题详情
24.(4分) 盐的水溶液是否都呈中性呢?小松在老师的合作下进行了探究。 【实验试剂】10%的Na2CO3溶液、10%的Na2SO4溶液、10%的CuSO4溶液、蒸馏水、pH试纸 【信息资料】Na2CO3 、Na2SO4和CuSO4固体溶于水分别会解离出Na+ 与CO32-、Na+与 SO42-、Cu2+与SO42- 【实验记录】 10%的Na2CO3溶液 10%的Na2SO4溶液 10%的CuSO4溶液 蒸馏水 pH >7 =7 <7 =7 【结论】不同的盐溶于水形成的溶液,有呈中性、碱性或 性。 【推理】Na2CO3溶液呈碱性的原因除了与水有关外,还与该盐中的 (填离子符号,下同)有关,而CuSO4溶液呈酸性的原因除了与水有关外,还与该盐中的
有关。 【反思与评价】小松在上述实验探究中,采用了实验 的方法。 试题详情
四、(本题包括2小题,共17分) 25.(10分) 下图A与B是实验室常用来制取气体的装置,根据所学知识回答以下问题: 试题详情
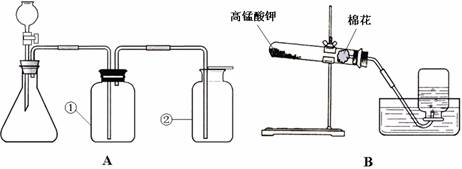
(1) 装置B表示正在用高锰酸钾制取氧气,其中还缺少的仪器是________(填名称),并将其画到相应的位置,图中棉花的作用是_________________________,该反应的化学方程式为__________________________________________,实验完毕,为防止水倒吸,应_______ ___________________________________。 (2)若想制取CO2,应选择图中的_______(填“A”或“B”)装置;若想用装置A来制取干燥的氧气,使用的药品是MnO2和___________(填化学式),并在瓶________(填“①”或“②”)中加浓硫酸。 (3)A装置气密性的检验:先关闭分液漏斗活塞,__________________________,用热毛巾捂住瓶①,若__________________________,则该装置漏气。 试题详情
26.(7分) 小亮对课本中C和CuO反应的产物进行了进一步的探究,以下是他进行实验的部分流程(装置气密性良好): 试题详情
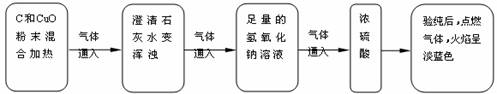
(1)通过以上实验,可知产物中有
气体。 (2)取出反应后的固体,观察呈红色。 【查阅资料】 ① C也能将CuO还原为红色固体Cu2O(氧化亚铜)
② Cu2O + H2SO4(稀)=
Cu + CuSO4 + H2O 【猜 想】 (a)红色固体只是Cu (b)
(c)红色固体是Cu和Cu2O的混合物 【实验探究】 实验操作 实验现象 实验结论 试题详情
取7.2g红色固体,置于烧杯中,向其中加入足量稀硫酸,充分搅拌,静置。 若无现象。 证明红色固体
。 若
。 证明红色固体肯定含有 ,可能含有 。 取上述反应液过滤、洗涤、干燥和称量,得固体 试题详情
6.8g 。 确认红色固体是
。 五、(本题包括2小题,共10分) 试题详情
27.(3分) 为使食品在较长的时间内保持色、香、味和口感,人们常在食品或食品包装中加入化学防腐剂。请根据下图回答: 试题详情

苯甲酸中C、H、O元素的原子个数比为 ,C、H元素的质量比为 , 相对分子质量为
。 试题详情
28.(7分) 小忻和小燕合作测定盐酸、硫酸组成的混合酸中溶质的质量分数,设计并进行了如下两个探究实验: 【实验1】 取20g该混合酸并分成4等份,然后分别加入一定量未知质量分数的BaCl2溶液,实验记录如下: 第1份 第2份 第3份 第4份 加入BaCl2溶液的质量 / g 15 20 25 30 反应得到的沉淀的质量 / g 试题详情
试题详情
试题详情
试题详情
2.330 【实验2】 将【实验1】中的第4份反应液过滤,再向滤液中逐滴加入10%的NaOH溶液,通过pH测定仪打印出加入NaOH溶液的质量与烧杯中溶液pH的关系如下图: 试题详情
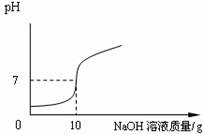
【数据处理】 小忻依据【实验1】沉淀的质量计算出混合酸中H2SO4的质量分数。 小燕依据【实验2】求混合酸中HCl的质量分数,过程如下: 【解】设混合酸中HCl的质量分数为ω。 HCl + NaOH = NaCl + H2O 试题详情
试题详情
试题详情
解得:ω=0.1825=18.25% 现请你参与探究并完成相关问题。(可能用到的相对分子质量:H2SO4―98
BaSO4―233 BaCl2―208
) (1)【实验1】中发生反应的化学方程式为
。 (2)小忻测出原混合酸中H2SO4的质量分数为
(保留三位有效数字)。 (3)小燕计算出混合酸中HCl的质量分数会
(填“偏高”、“偏低”或“无影响”),理由是
(如“无影响”,本空不作答)。 试题详情
| 
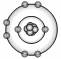 ,它的核电荷数和最外层电子数分别是
,它的核电荷数和最外层电子数分别是