
第五单元 测试A卷
测试时间:100分钟 总分:100分
一、选择题(每题3分,共36分)
1.判断下列事实,其中能用质量守恒定律解释的是 ( )
①蜡烛燃烧后质量变小了 ②镁带燃烧后质量变大了 ③湿衣服晾干后变轻了 ④ CuSO4溶液和NaOH溶液混合后总质量不变
A.①② B.③ C.①②④ D.都可以
2.化学反应前后,肯定没有变化的是 ( )
①原子的种类 ②分子的种类 ③元素的种类 ④参加化学反应各物质的质量总和
⑤原子的数目 ⑥物质的种类 ⑦物质的状态 ⑧原子的质量 ⑨分子的数目
A.①③④⑤⑧ B.①③④⑤⑦⑧⑨
C.①③⑤⑥⑦ D.①②③⑤⑥⑧
3.加热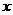 克氯酸钾和y克二氧化锰的混合物制取氧气至反应不再发生为止,剩余固体质量为z克,则生成的氧气的质量为 ( )
克氯酸钾和y克二氧化锰的混合物制取氧气至反应不再发生为止,剩余固体质量为z克,则生成的氧气的质量为 ( )
A.(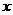 +y―z)克 B.(
+y―z)克 B.(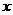 一z)克
一z)克
C.(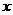 +y)克 D.(y―z)克
+y)克 D.(y―z)克
4.氧化汞受热时的变化可用下图表示(图中大圆圈表示汞原子,小圆圈表示氧原子)。据图得出的下列结论中错误的是 ( )
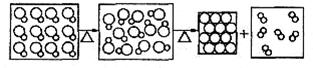
A.氧化汞受热时能分解成汞和氧气 B.原子是化学变化中的最小粒子
C.分子在化学变化中可以再分 D.所有的物质都是由分子构成的
5.相同质量的下列物质在氧气中燃烧,消耗氧气最少的是 ( )
A.H2 B.P C.C D.S
6.有反应2X+3Y2==2XY3,在一定条件下使62gX与足量的Y2反应,生成68gXY3,则X与Y两元素的相对原子质量之比为 ( )
A.2:3 B.31:
7.将
A.含有C、H、O三种元素 B.可能含有氧元素
C.一定含有氧元素 D.氢元素的质量分数为20%
8.镁在氧气中燃烧生成了氧化镁,在此反应中镁、氧气、氧化镁三者的质量比是 ( )
A.24:32:40 B.48:32:80
C.24:32:56 D.48:32:40
9.CO和O2的混合气体
A.2:1 B.3:
10.只含碳、氢或碳、氢、氧的物质充分燃烧后的产物均为CO2和H2O。相同分子数目的以下物质分别充分燃烧,所消耗O2的质量相等的是 ( )
①C2H5OH ②CH3OH ③CH4 ④C2H4
A.①③ B.②③ C.②④ D.①④
11.关于反应:X2+3Y2==2Z,可根据质量守恒定律推知下列说法一定错误的是( )
A.Z的化学式为XY3
B.若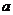 gX2和bgY2恰好完全反应,则生成(
gX2和bgY2恰好完全反应,则生成(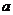 +b)gZ
+b)gZ
C.若X2的相对分子质量为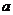 ,Y2的相对分子质量为b,则Z的相对分子质量为(
,Y2的相对分子质量为b,则Z的相对分子质量为(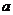 +3b)
+3b)
D.若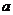 gX2完全反应生成bgZ,则同时消耗(b-
gX2完全反应生成bgZ,则同时消耗(b-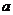 )gY2
)gY2
12.下图是铜粉和氧气反应生成氧化铜时,参加反应的铜粉的质量和产物氧化铜的质量的关系图像。氧化铜中,铜元素和氧元素的质量比值约为 ( )
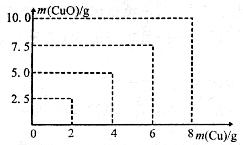
A.8
B.
二、填空题(每空2分,共32分)
13.有一位同学写出了下列化学方程式:
A.H2O H2↑+O2↑ B.S+O2
H2↑+O2↑ B.S+O2 SO2↑
SO2↑
C.Mg+O2 ↑ MgO2 D.P2+O2
MgO2 D.P2+O2 P2O5
P2O5
请将有关序号填入相应的横线上。
(1)化学式写错的是__________________________。
(2)未配平的是____________________________________。
(3)“↑”符号使用不当的是________________________。
(4)反应条件不对的是____________________________________。
14.写出下列反应的化学方程式。
(1)硫在氧气中燃烧
____________________________________________________________
(2)氢气燃烧
____________________________________________________________
(3)高锰酸钾加热
____________________________________________________________
(4)水通电分解
____________________________________________________________
(5)铁跟稀硫酸反应生成硫酸亚铁和氢气
____________________________________________________________
(6)钠放入水中生成氢氧化钠和氢气
____________________________________________________________
(7)在空气中能燃烧且生成白色固体的反应
____________________________________________________________
(8)产生使澄清石灰水变浑浊的气体的化合反应
____________________________________________________________
(9)有水生成的分解反应
____________________________________________________________
(10)在空气中不能燃烧,在氧气中能剧烈燃烧且生成黑色固体
________________________________________________
15.在使用体温计测量体温时,若不慎将体温计打破,散落出来的汞产生汞蒸气会对人体产生危害。此时可以撒一些硫粉在上面,使硫与汞发生化合反应生成固体硫化汞(HgS)。
(1)写出硫与汞反应的化学方程式____________________________________。
(2)用分子、原子的观点解释体温计测量体温时汞柱上升的现象____________________________________________________________。
16.已知“ ”:“
”:“  ”表示质子数不同的原子。
”表示质子数不同的原子。
(1)下列表示的气体物质中,属于化合物的是___________。
(2)下列表示的气体物质中,属于混合物的是___________。

三、实验探究题(每空2分,共18分)
17.某校化学探究性学习小组的同学用下图装置进行实验。

实验目的
(1)用高锰酸钾制取一瓶氧气,做铝箔燃烧的实验。
(2)粗略测定加热
反应原理(用化学方程式表示)
高锰酸钾制氧气:_________________________________;
铝箔在氧气中燃烧;_________________________________。
仪器认识
写出仪器①②的名称:①______________________;②______________________。
装置连接
为达到实验目的(2),各装置的正确连接顺序是(填接口的字母):
a→( )→( )→d
问题分析
(1)实验过程发现B瓶中的水变红了,原因是______________________。
(2)用收集到的氧气做铝箔燃烧的实验时,发现瓶底炸裂,发生失误的操作原因可能是________________________________。
(3)根据化学方程式可算出理论上
四、计算题(14分)
18.煤是重要的化工原料,用煤做燃料,不仅是极大的浪费,而且因煤中含有硫,燃烧后生成的二氧化硫会造成空气污染。某工厂用煤做燃料,每天燃烧含硫2%的煤4.8×
(1)试计算每天该厂排放到空气中的二氧化硫为多少千克。(计算结果保留一位小数,下同)
(2)该厂废气中二氧化硫的含量可根据下列反应测定:I2+SO2+2H2O==H2SO4+2HI。现取该厂废气样品500mL,用含碘4×10-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com