
2008-2009ѧÄê¶ÈÐË»¯ÊÐʵÑéÖÐѧµÚһѧÆÚ¾ÅÄ꼶ÖÊÁ¿³é²â
»¯Ñ§ÊÔ¾í
×¢ÒâÊÂÏ
1£®±¾ÊÔ¾í·ÖµÚ¢ñ¾í£¨Ñ¡ÔñÌ⣩ºÍµÚ¢ò¾í£¨·ÇÑ¡ÔñÌ⣩Á½²¿·Ö¡£±¾¾í¹²100·Ö¡£¿¼ÊÔʱ¼ä90·ÖÖÓ¡£
¿ÉÄÜÓõ½µÄÏà¶ÔÔ×ÓÖÊÁ¿£ºHÒ»
µÚ¢ñ¾í £¨Ñ¡ÔñÌâ ¹²40·Ö£©
Ò»¡¢Ñ¡ÔñÌ⣨±¾Ìâ¹²15СÌ⣬ÿСÌâÖ»ÓÐÒ»¸öÑ¡Ïî·ûºÏÌâÒ⡣ÿСÌâ2·Ö£¬¹²30·Ö£©
1£®ÏÂÁÐÔì³É¿ÕÆøÎÛȾµÄÎïÖÊÖ÷Òª²»ÊÇÓÉ»¯Ñ§·´Ó¦²úÉúµÄÊÇ
A£®·ÙÉÕÀ¬»ø²úÉúµÄ´óÁ¿Ñ̳¾ B£®½¨ÖþÊ©¹¤Ê±·ÉÑïÆðµÄ»Ò³¾
C£®È¼·ÅÑÌ»¨±¬Öñ²úÉúµÄÆøÌå D£®»ú¶¯³µÐÐʻʱÅŷŵÄβÆø
2£®ÏÂÁи÷×éÎïÖʶ¼ÊôÓÚ´¿¾»ÎïµÄÊÇ
A£®ÒºÑõ¡¢¸É±ù B£®Ãº¡¢Ê¯ÓÍ C£®ÕôÁóË®¡¢ÈíË® D£®´óÀíʯ¡¢ÌìÈ»Æø
3£®¿ÕÆøÊÇÒ»ÖÖ±¦¹ó×ÊÔ´¡£ÏÂÁÐÓйؿÕÆøµÄ˵·¨ÕýÈ·µÄÊÇ
A£®¿ÕÆøÖк¬Á¿×î¶àµÄÊÇÑõÔªËØ
B£®¿ÕÆøÓÉÑõÆøºÍµªÆø×é³É£¬ÆäÖÐÑõÆøµÄÖÊÁ¿Ô¼Õ¼¿ÕÆøÖÊÁ¿µÄ1£¯5
C£®¿ÕÆøÖзÖÀë³öµÄµªÆø»¯Ñ§ÐÔÖʲ»»îÆ㬿É×÷ʳƷ±£Ïʵı£»¤Æø
D£®¿ÕÆøÖÊÁ¿±¨¸æÖÐËùÁеĿÕÆøÖÊÁ¿¼¶±ðÊýÄ¿Ô½´ó£¬¿ÕÆøÖÊÁ¿Ô½ºÃ
4£®Í¨³£Çé¿öÏ£¬ÌúÖÆÆ·ÉúÐâµÄÌõ¼þÊÇ
A£®½öÐèÒªÑõÆø B£®½öÐèҪˮ
C£®Í¬Ê±ÐèÒªÑõÆøºÍË® D£®½öÐèҪϡÁòËᡢϡ´×Ëá»òʳÑÎË®
5£®ÏÂÁзûºÅÖУ¬¼ÈÄܱíʾһÖÖÔªËØ£¬ÓÖÄܱíʾһÖÖÎïÖÊ£¬»¹Äܱíʾһ¸öÔ×ÓµÄÊÇ
A£®Cl2 ¡¡¡¡¡¡¡¡B£®N ¡¡¡¡¡¡¡¡¡¡C£®Mg ¡¡¡¡¡¡¡¡D£®S2£
6£®ÏÂͼÊÇʵÑéÊÒÀï±êÇ©ÆÆËðµÄһƿÈÜÒº£¬Ö»ÄÜ¿´Çå¡°K¡±ºÍ¡°O
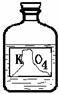
A£®¸ßÃÌËá¼ØÈÜÒº B£®ÃÌËá¼ØÈÜÒº
C£®ÁòËá¼ØÈÜÒº D£®Ì¼Ëá¼ØÈÜÒº
7£®ÑÌ»¨±¬ÖñרÔ˳µÁ¾ÒªÐü¹Ò»òÅçÍ¿Ïà¹ØΣÏÕ»õÎïÔËÊä±êÖ¾£¬¸Ã±êÖ¾Ó¦ÊÇÏÂÁÐÖеÄ
8£®ÏÂÁпα¾ÖÐÑо¿Î¢Á£ÌØÐԵĻ¯Ñ§ÊµÑéÓëÆäÖ÷ҪʵÑéÄ¿µÄ²»Ïà·ûµÄÊÇ
Ñ¡Ïî
ʵÑéÃû³Æ
Ö÷ҪʵÑéÄ¿µÄ
A
¸ßÃÌËá¼ØÈÜÓÚË®µÄʵÑé
Ö¤Ã÷ÎïÖÊÊÇ¿É·ÖµÄÇÒ¶¼ÓÉϸСµÄ΢Á£¹¹³É
B
°±Ë®»Ó·¢Ê¹ÎÞÉ«·Ó̪ÊÔÒº±äÉ«µÄʵÑé
Ö¤Ã÷΢Á£ÊDz»¶ÏÔ˶¯µÄ
C
Ë®ºÍ¿ÕÆøµÄѹËõʵÑé
Ö¤Ã÷΢Á£Ö®¼äÓпÕ϶
D
¾Æ¾«ÓëË®»ìºÏµÄÌå»ý±ä»¯µÄʵÑé
Ö¤Ã÷²»Í¬µÄ΢Á£»¯Ñ§ÐÔÖʲ»Í¬
9£®À¬»øÊÇ·Å´íÁ˵ط½µÄ¡°±¦²Ø¡±£¬ÎªÁ˽ÚÔ¼×ÊÔ´ºÍ±£»¤»·¾³£¬Ó¦ÊµÊ©À¬»ø·ÖÀà»ØÊÕ¡£Éú»îÖзÏÆúµÄÌú¹ø¡¢ÂÁÖÆÒ×À¹Þ¡¢ÍÏߵȿÉÒÔ¹éΪһÀà¼ÓÒÔ»ØÊÕ£¬ËüÃÇÊôÓÚ
A£®Ñõ»¯Îï B£®»¯ºÏÎï C£®½ðÊô»òºÏ½ð D£®·Ç½ðÊô
10£®ÏÂÁйØÓÚ·Ö×Ó¡¢Ô×Ó¡¢Àë×ÓµÄÐðÊö´íÎóµÄÊÇ
A£®·Ö×Ó¡¢Ô×Ó¡¢Àë×Ó¶¼¿ÉÒÔ¹¹³ÉÎïÖÊ ¡¡B£®·Ö×Ó¶¼ÊÇÓÉÀë×Ó¹¹³ÉµÄ
C£®Ô×ӳʵçÖÐÐÔ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡D£®Àë×Ó¿É·ÖΪÒõÀë×ÓÓëÑôÀë×Ó
11£®ÌúË¿ÔÚ¿ÕÆøÖÐ×ÆÈÈ·¢ºì£¬µ«²»ÄÜȼÉÕ£¬¶øÔÚ´¿ÑõÖÐÈ´ÄÜȼÉÕ£¬ÕâÒ»ÊÂʵÓëÏÂÁÐÄÄÒ»ÒòËعØϵ×îÃÜÇÐ
A£®ÌúË¿µÄ±íÃæ»ý B£®ÑõÆøµÄº¬Á¿
C£®È¼ÉÕÇøÓòµÄÎÂ¶È D£®ÌúµÄ×Å»ðµã
12£®ôä´äÊÇÈËÃÇϲ°®µÄÒ»ÖÖ×°ÊÎÆ·£¬ôä´äµÄÖ÷Òª³É·ÝÊÇÓ²Óñ£Û»¯Ñ§Ê½ÎªNaAlSi2O6£Ý¡£ÏÂÁÐÓйØ˵·¨ÕýÈ·µÄÊÇ
A£®ôä´äÊÇÒ»ÖÖ´¿¾»Îï B£®Ó²ÓñÖУ¬¹èÔªËصĻ¯ºÏ¼ÛΪ+4¼Û
C£®Ó²Óñº¬ÓÐ10¸öÔ×Ó D£®ôä´ä½öÓÉÄÆ¡¢ÂÁ¡¢¹è¡¢ÑõËÄÖÖÔªËع¹³É
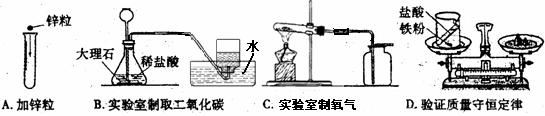
13£®ÏÂÁÐͼʾʵÑé·½·¨»ò²Ù×÷ÕýÈ·µÄ
14£®ÄêÇáÈËϲ»¶È¾·¢,Ⱦ·¢Ê±»áÓõ½Ò»ÖÖ×ÅÉ«¼Á¨D¶Ô±½¶þ°·,ËüÊÇÒ»ÖÖÓж¾µÄ»¯Ñ§Ò©Æ·,ÓÐÖ°©ÐÔ,»á¶ÔȾ·¢ÕßµÄÉíÌå´øÀ´É˺¦,ÏÂÁйØÓÚ¶Ô±½¶þ°·£¨C6H8N2£©ÐðÊö²»ÕýÈ·µÄÊÇ
A£®ËüÊÇÓÉ̼¡¢Çâ¡¢µªÈýÖÖÔªËØ×é³ÉµÄ»¯ºÏÎï
B£®ËüµÄ·Ö×ÓÖÐ̼¡¢Çâ¡¢µªµÄÔ×Ó¸öÊý±ÈΪ6:8:2
C£®ËüµÄÏà¶Ô·Ö×ÓÖÊÁ¿Îª108
D£®ËüµÄ·Ö×ÓÖÐ̼¡¢Çâ¡¢µªÈýÖÖÔªËصÄÖÊÁ¿±ÈÊÇ3:4:1
15£®±È½Ï¡¢ÍÆÀíÊÇ»¯Ñ§Ñ§Ï°³£Óõķ½·¨£¬ÒÔÏÂÊǸù¾ÝһЩ·´Ó¦ÊÂʵÍƵ¼³öµÄÓ°Ï컯ѧ·´Ó¦µÄÒòËØ£¬ÆäÖÐÍÆÀí²»ºÏÀíµÄÊÇ
ÐòºÅ
»¯Ñ§·´Ó¦ÊÂʵ
Ó°Ïì·´Ó¦µÄÒòËØ
A
ÌúË¿ÔÚ¿ÕÆøÖкÜÄÑȼÉÕ£¬¶øÔÚÑõÆøÖÐÄܾçÁÒȼÉÕ
·´Ó¦ÎïŨ¶È
B
̼³£ÎÂϲ»ÓëÑõÆø·¢Éú·´Ó¦£¬¶øÔÚµãȼʱÄÜÓëÑõÆø·´Ó¦
·´Ó¦Î¶È
C
Ë«ÑõË®ÔÚ³£ÎÂϽÏÄѷֽ⣬¶ø¼ÓÈë¶þÑõ»¯Ã̺óѸËÙ·Ö½â
´ß»¯¼Á
D
ÍƬÔÚ¿ÕÆøÖкÜÄÑȼÉÕ£¬Í·ÛÔÚ¿ÕÆøÖнÏÒ×ȼÉÕ
·´Ó¦ÎïµÄÖÖÀà
¶þ¡¢Ñ¡ÔñÌ⣨±¾Ìâ¹²5СÌ⣬ÿСÌâÓÐÒ»¸ö»ò¶þ¸öÑ¡Ïî·ûºÏÌâÒâ¡£´íÑ¡¡¢¶àÑ¡²»¸ø·Ö¡£Óжþ¸ö´ð°¸µÄ£¬Ö»Ñ¡Ò»¸öÇÒÕýÈ·£¬¸ø1·Ö¡£Ã¿Ð¡Ìâ2·Ö£¬¹²10·Ö£©
16£®Ä³Á½ÖÖÎïÖÊÔÚÒ»¶¨Ìõ¼þÏ·¢Éú»¯Ñ§·´Ó¦µÄ΢¹ÛʾÒâÈçͼ£¨ÆäÖС° ¡±¡°
¡±¡°  ¡± ·Ö±ð±íʾÁ½ÖÖ²»Í¬µÄÔ×Ó£©¡£¶ÔÉÏÊö·´Ó¦£¬ÏÂÁÐ˵·¨ÕýÈ·µÄÊÇ
¡± ·Ö±ð±íʾÁ½ÖÖ²»Í¬µÄÔ×Ó£©¡£¶ÔÉÏÊö·´Ó¦£¬ÏÂÁÐ˵·¨ÕýÈ·µÄÊÇ
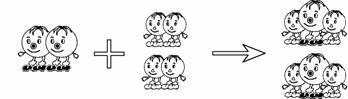
A£®·´Ó¦ÎﶼÊÇ»¯ºÏÎï B£®·´Ó¦ÊôÓÚ»¯ºÏ·´Ó¦
C£®Éú³ÉÎï¿ÉÄÜÊÇÑõ»¯Îï D£®·´Ó¦Ç°ºó·Ö×ÓÖÖÀ಻±ä
17£®Òâ´óÀû¿Æѧ¼Ò×î½üºÏ³ÉÁËÒ»ÖÖÐÂÐ͵ÄÑõ·Ö×Ó£¬Æ仯ѧʽΪO4¡£ÏÂÁжÔÕâÖÖÎïÖʵķÖÎöÓëÈÏʶÖÐÕýÈ·µÄÊÇ
A£®O4ÊÇÒ»ÖÖ»¯ºÏÎï B£®O4ÊÇÓÉO2×é³ÉµÄ»ìºÏÎï
C£®O4ÊÇÒ»ÖÖÑõ»¯Îï D£®O4ºÍO2µÄ×é³ÉÔªËØÏàͬ
18£®ÔÚÒ»¸öÃܱÕÈÝÆ÷ÖУ¬Óмס¢ÒÒ¡¢±û¡¢¶¡ËÄÖÖÎïÖÊÔÚÒ»¶¨Ìõ¼þϳä·Ö·´Ó¦ºó£¬²âµÃ·´Ó¦Ç°ºó¸÷ÎïÖʵÄÖÊÁ¿ÈçÏÂ±í£º
ÎïÖÊ
¼×
ÒÒ
±û
¶¡
·´Ó¦Ç°ÖÊÁ¿£¯g
5
2
20
22
·´Ó¦ºóÖÊÁ¿£¯g
´ý²â
11
28
5
ÏÂÁÐ˵·¨´íÎóµÄÊÇ
A£®¸Ã·´Ó¦ÊǷֽⷴӦ B£®¼×¿ÉÄÜÊǸ÷´Ó¦µÄ´ß»¯¼Á
C£®ÒÒ¡¢±û±ä»¯µÄÖÊÁ¿±ÈΪ9£º8 D£®·´Ó¦ºó¼×µÄÖÊÁ¿Îª
19£®Á½Í¬Ñ§Î§ÈÆ·äÎÑúȼÉÕ½øÐÐÁËÈçÏÂ̽¾¿£¬ÆäÖÐÒÀ¾ÝÖÊÁ¿Êغ㶨ÂɽâÊ͵ÄÊÇ
A£®µ±ÃºÈ¼ÉÕÕýÍúʱ½«Â¯ÃŹØÉÏ£¬Ãº²ãÉÏ·½·¢ÏÖÀ¶É«»ðÑæ¡£½âÊÍ£º´ËʱÑõÆø²»×ã¶ø²úÉúµÄCOÔÚȼÉÕ
B£®ÃºÈ¼ÉÕÍêºóú»ÒÖÊÁ¿±ÈúµÄÖÊÁ¿Çá¡£½âÊÍ£ºÃºÈ¼ÉÕºó²úÉúµÄ¶þÑõ»¯Ì¼µÈÆøÌåÒݳö
C£®ÔÚú¯ÉÏ·½·ÅÒ»ºøË®²»ÄÜ·ÀÖ¹COÖж¾¡£½âÊÍ£ºCOÄÑÈÜÓÚË®
D£®½«Ãº×ö³É·äÎÑ×´¾Í¸üÒ×ȼÉÕ¡£½âÊÍ£º·äÎÑ×´µÄúÓë¿ÕÆø½Ó´¥Ãæ»ýÔö´ó
20£®»îÐÔÌ¿ÊÇÒ»ÖÖÓÅÁ¼µÄÆøÌåÎü¸½¼Á£¬¿ÉÓÃÓÚ±ùÏä³ý³ô¡£Ï±íÁгöÁ˲»Í¬Î¶ÈÏÂÿÁ¢·½ÀåÃ×»îÐÔÌ¿ËùÄÜÎü¸½µÄ³£¼ûÆøÌåµÄÌå»ý£®·ÖÎö±íÖÐÊý¾ÝÓëÆøÌå×é³É¡¢ÐÔÖʵȵĹØϵ£¬ÄãÈÏΪÏÂÁнáÂÛÕýÈ·µÄÊÇ
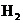
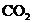
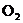
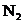
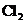
ÆøÌåµÄ·Ðµã£¨¡æ£©
-252
-78
-183
-196
-34
±»Îü¸½µÄÌå»ý£¨mL£©
4.5
97
35
11
494
A£®ÆøÌå·Ö×ÓËùº¬Ô×Ó¸öÊý¶àʱ£¬ÆøÌåÒ×±»Îü¸½
B£®·ÐµãÔ½¸ßµÄÆøÌ壬ԽÒ×±»Îü¸½
C£®ÆøÌåÊÇ»¯ºÏÎïʱ£¬Ò×±»Îü¸½
D£®ÆøÌåµÄÏà¶Ô·Ö×ÓÖÊÁ¿Ô½´ó£¬Ô½Ò×±»Îü¸½
µÚ¢ò¾í£¨·ÇÑ¡ÔñÌâ ¹²60·Ö£©
Èý¡¢Ìî¿ÕÌ⣨±¾Ìâ°üÀ¨7СÌ⣬¹²33·Ö£©
21£®£¨4·Ö£©Óû¯Ñ§ÓÃÓïÌî¿Õ:
2¸öÑõÔ×Ó £»3¸öµª·Ö×Ó £»ï§¸ùÀë×Ó £»±ê³öÁòËáÌúÖÐÌúµÄ»¯ºÏ¼Û £»
22£®£¨4·Ö£©Ð´³öÏÂÁз´Ó¦µÄ»¯Ñ§·½³Ìʽ²¢×¢Ã÷·´Ó¦ÀàÐÍ£º
£¨1£©Á×ÔÚÑõÆøÖÐȼÉÕ £¨ ·´Ó¦£©£»
£¨2£©Ð¿ºÍÏ¡ÁòËá·´Ó¦ £¨ ·´Ó¦£©¡£
23£®£¨6·Ö£©»¯Ñ§¾ÍÔÚÎÒÃÇÉí±ß£¬ËüÄܸÄÉÆÎÒÃǵÄÉú»î¡£Çë´Ó¡°A£®¸É±ù¡¢B£®µªÆø¡¢C£®Çâ
Æø¡¢D£®Ê¯ÓÍ¡¢E£®Ì¼ËáÄÆ¡¢F£®ÇâÑõ»¯ÄÆ¡¢G£®Ñõ»¯Ìú¡±ÖÐÑ¡ÔñÊʵ±µÄÎïÖÊÌî¿Õ£¨Ìî×Öĸ£©¡£
£¨1£©±»³ÆΪÀíÏëµÄ¡°ÂÌÉ«ÄÜÔ´¡±ÊÇ £»£¨2£©¿ÉÓÃÓÚÈ˹¤½µÓêµÄÎïÖÊÊÇ £»
£¨3£©³£ÓõĴ¿¼îÊÇÖ¸ £»£¨4£©±»ÓþΪ¡°¹¤ÒµµÄѪҺ¡±µÄÊÇ £»
£¨5£©¿ÕÆøÖÐÌå»ý·ÖÊý×î´óµÄÊÇ £»£¨6£©ÌúÐâµÄÖ÷Òª³É·ÖÊÇ ¡£
24£®£¨4·Ö£©Çë´ÓÍ¡¢Ð¿¡¢îÑ¡¢Ìú¡¢Òø¡¢ÂÁ¡¢¹¯µÈ½ðÊôÖÐÑ¡È¡ºÏÊʵĴð°¸ÌîÈëÏÂÃæ¿Õ¸ñÖУº
£¨1£©µ¼µçÐÔÄܽö´ÎÓÚÒø£¬¹ã·ºµØÓ¦ÓÃÓÚÖÆÔìµçÏß¡¢µçÀµÄÊÇ £»
£¨2£©¹ã·ºÓÃÓÚº½¿Õ¹¤Òµ¡¢Ôì´¬¹¤ÒµºÍ»¯Ñ§¹¤Òµ¡¢Ò½Ñ§²ÄÁÏ£¨ÈËÔì¹Ç¹Ø½ÚµÈ£©µÄÊÇ £»
£¨3£©ÌúÀ¸¸ËÍâ²ãÍ¿Áϵġ°Òø·Û¡±´ó¶àÊÇ £»
£¨4£©ÈÈˮƿÄÚµ¨±Ú³£¶ÆÒ»²ãÒø°×É«ÎïÖÊÖÐÓÐ ¡£
25£®£¨5·Ö£©×ÔÀ´Ë®Ïû¶¾¹ý³ÌÖÐͨ³£»á·¢ÉúÈçÏ»¯Ñ§·´Ó¦£¬Æä·´Ó¦µÄ΢¹Û¹ý³Ì¿ÉÓÃÏÂͼ±íʾ£º
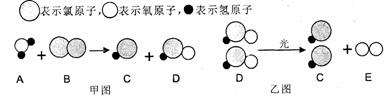
£¨1£©Çëд³öÈçͼËùʾ·´Ó¦µÄ»¯Ñ§·½³Ìʽ
¼×ͼ
ÒÒͼ
£¨2£©ÒÒͼËùʾ·´Ó¦µÄ»ù±¾·´Ó¦ÀàÐÍΪ £»
£¨3£©ÉÏÊöÎïÖÊÖУ¬ÊôÓÚµ¥ÖʵÄÓÐ £¨Ìѧʽ£©£»
£¨4£©DÎïÖÊÖÐÂÈÔªËصĻ¯ºÏ¼ÛΪ £»
26£®£¨5·Ö£©ÀûÓû¯Ñ§ÖªÊ¶£¬¿ÉÒÔ½âÊÍÓë½â¾öÉú»îÖÐһЩ³£¼ûµÄÎÊÌ⣬ÇëÄã³¢ÊÔÍê³ÉÏÂÁÐÌî¿Õ¡£
£¨1£©ÒªÇø·ÖӲˮÓëÈíË®£¬¿ÉÒÔʹÓõÄÎïÖÊÊÇ £»
£¨2£©Òª³ýÈ¥ÎÛË®ÖеÄÄÑÈÜÐÔÔÓÖÊ£¬¿ÉÒÔ²ÉÓõĻù±¾²Ù×÷ÊÇ________________£»
£¨3£©Òª·ÀÖ¹¼ÒÀï³£ÓõIJ˵¶ÉúÐ⣬ͨ³£²ÉÓõķ½·¨ÊÇ________________£»
£¨4£©Îª±£Ö¤ÈËÉí°²È«£¬½øÈë¾Ã먦ÆôµÄ²Ë½ÑÇ°£¬Ðë×ö________________ÊÔÑ飻
£¨5£©µãȼ¿ÉȼÐÔÆøÌåÇ°Ó¦½øÐÐ________________¡£
27£®£¨5·Ö£©»¯Ñ§·´Ó¦×ñÑÖÊÁ¿Êغ㶨ÂÉ¡£
£¨1£©Ã¾´øÔÚ¿ÕÆøÖÐÍêȫȼÉÕºóÉú³ÉÑõ»¯Ã¾£¬Æä¹ÌÌåÖÊÁ¿±ä»¯¿ÉÓÃͼһ±íʾ£¬Ôò£ºM2ÓëM1ÖÊÁ¿²î±íʾµÄÖÊÁ¿ÊÇ £¨ÌîÐòºÅ£©£º
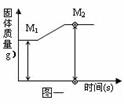
A£®Éú³ÉMgOµÄÖÊÁ¿£» B£®MgµÄÖÊÁ¿£»
C£®²Î¼Ó·´Ó¦µÄO2µÄÖÊÁ¿£» D£®¶àÓàµÄO2µÄÖÊÁ¿¡£
£¨2£©Ð¡·ïͬѧÓÿÕÆøÖÐȼÉÕþ´øµÄʵÑéÀ´Ì½¾¿ÖÊÁ¿Êغ㶨ÂÉ¡£Ã¾µãȼºóµÄʵÑéÏÖÏóÈçͼ¶þ£¬Ã¾ÍêȫȼÉպ󣬳ÆÁ¿Ê¯ÃÞÍøÉÏÁôϹÌÌåµÄÖÊÁ¿±È·´Ó¦Ç°Ã¾´øÖÊÁ¿»¹Çᣨֻ¿¼ÂÇÑõÆø²Î¼Ó·´Ó¦£©£¬ÁªÏµÊµÑé¹ý³Ì£¬·ÖÎöÆäÔÒò µÈ¡£

£¨3£©Ð¡·ïÓÖÔÚÒ»±¾²Î¿¼ÊéÉÏ·¢ÏÖ£¬Ã¾Ò²ÄÜÔÚ¶þÑõ»¯Ì¼ÖÐȼÉÕ£¡ÓÚÊÇËý×öÁËÕâ¸öʵÑ飨ÈçͼÈý£©£¬½«Ã¾ÌõµãȼºóѸËÙÉìÈëÊ¢ÓжþÑõ»¯Ì¼µÄ¼¯ÆøÆ¿ÖУ¬·¢ÏÖþÌõ¾çÁÒȼÉÕ£¬·¢³ö°×¹â£¬·ÅÈÈ£¬²úÉúÒ»ÖÖ°×É«·ÛÄ©ºÍÒ»ÖÖºÚÉ«·ÛÄ©¡£¸ù¾ÝÉÏÊöÏÖÏó£¬Ð´³ö¸Ã·´Ó¦µÄ»¯Ñ§·½³Ìʽ£º
£»
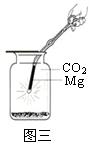
Õâ¸öʵÑ黹Òý·¢ÁËÎÒÃǶԹýȥijЩ֪ʶµÄ·´Ë¼£¬´Ó¶øÓÐÁËеķ¢ÏÖ£¬ÄãÈÏΪеķ¢ÏÖÊÇ £¨ÌîÐòºÅ£©£º
A£®ÔÚÒ»¶¨µÄÌõ¼þÏ£¬¶þÑõ»¯Ì¼Ò²ÄÜÖ§³ÖȼÉÕ£»
B£®»îÆýðÊô×Å»ðʱ²»ÄÜÓöþÑõ»¯Ì¼Ãð»ð£»
C£®È¼ÉÕ²»Ò»¶¨ÐèÒªÓÐÑõÆø¡£
ËÄ£®ÊµÑéÌ⣨±¾Ìâ°üÀ¨3СÌ⣬¹²20 ·Ö£©
28£®£¨5·Ö£©¸ÖÌúµÄÉú²úºÍʹÓÃÊÇÈËÀàÎÄÃ÷ºÍÉç»á½ø²½µÄÒ»¸öÖØÒª±êÖ¾£¬µ«¸ÖÌúµÄÐâÊ´Ò²¸øÈËÀà´øÀ´Á˾޴óµÄËðʧ¡£
£¨1£©Ä³Ñ§ÉúÏë̽¾¿ÌúÉúÐâµÄÌõ¼þ£¬Ëû½«¸ÉÔï¡¢ÎÞÐâµÄÌú¶¤·Ö±ðͬʱ·ÅÈëA¡¢B¡¢CÈýÖ§ÊÔ¹ÜÖнøÐÐÑо¿¡£ÇëÄã°ïÖú¸ÃѧÉúÍê³ÉÏÂÁÐʵÑéÉè¼ÆµÄÄÚÈÝ£º
񅧏
²Ù×÷·½·¨
ʵÑéÄ¿µÄ
A
̽¾¿ÌúÔÚ¸ÉÔï¿ÕÆøÖеÄÉúÐâÇé¿ö
B
·ÅÈëÌú¶¤£¬×¢ÈëÕôÁóË®½þûÌú¶¤£¬²¢ÓÃÖ²ÎïÓÍÒº·â
C
̽¾¿ÌúÔÚÓпÕÆøºÍˮʱµÄÉúÐâÇé¿ö
£¨2£©×ÔÐгµµÄÖ÷Òª²ÄÁϸÖÌúÒ×ÉúÐ⣬ÇëÄãÑ¡ÔñÏÂÁÐÑ¡ÏîΪÏÂͼ±êʾµÄ×ÔÐгµ²¿¼þ¸÷Éè¼ÆÒ»ÖÖ²»Í¬µÄ¡¢ºÏÀíµÄ·ÀÐâ·½·¨£º
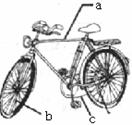
a.Èý½Å¼Ü ¡¢c.Á´Ìõ £¨ÌîÐòºÅ£©£º
A£®¶ÆÆäËü½ðÊô B£®Í¿Æá C£®ÐγÉÖÂÃÜÑõ»¯Ä¤
D£®Ðγɲ»Ðâ¸ÖµÈºÏ½ð E£®Í¿ÓÍ
29£®£¨9·Ö£©ÏÂͼ1ÊÇʵÑéÊÒÄ£ÄâÁ¶ÌúµÄ×°ÖÃͼ£¬ÊԻشð£º
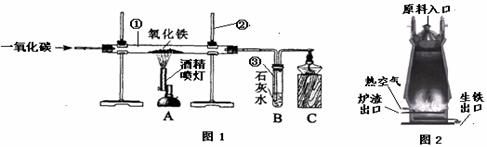
£¨1£©ÒÇÆ÷¢ÚµÄÃû³ÆÊÇ £»ÒÇÆ÷¢ÛµÄÃû³ÆÊÇ ¡£
£¨2£©°´ÉÏͼÁ¬½ÓʵÑé×°Öᢼì²é×°ÖõÄÆøÃÜÐÔ¡¢×°Ò©Æ·¡¢¹Ì¶¨ÊµÑé×°Öúó£¬Ö÷ҪʵÑé²½ÖèÓУº¢ÙͨÈëÒ»Ñõ»¯Ì¼£»¢ÚֹͣͨÈëÒ»Ñõ»¯Ì¼£»¢Ûµãȼ¾Æ¾«µÆ£»¢ÜϨÃð¾Æ¾«µÆ£»¢Ýµãȼ¾Æ¾«ÅçµÆ£»¢ÞϨÃð¾Æ¾«ÅçµÆ¡£ÕýÈ·µÄ²Ù×÷˳ÐòÊÇ£¨ÌîÐòºÅ£© ¡£
£¨3£©ÊµÑé¹ý³ÌÒÇÆ÷¢ÙÖз¢Éú·´Ó¦µÄ»¯Ñ§·½³ÌʽÊÇ £¬ÒÇÆ÷¢ÛÖеÄÏÖÏóÊÇ ¡£
£¨4£©Çëд³öÒ»ÖÖÖ¤Ã÷²úÎïÖк¬Ìú·ÛµÄ·½·¨£º ¡£
£¨5£©ÊµÑé¹ý³ÌÖвúÉúµÄβÆø²»ÄÜÖ±½ÓÅŷŵÄÔÒòÊÇ ¡£
£¨6£©Í¼2Êǹ¤ÒµÉú²úÖÐÁ¶Ìú¸ß¯µÄ½á¹¹Í¼¡£Êµ¼ÊÉú²úÖÐÁ¶ÌúµÄÔÁÏÌú¿óʯ¡¢½¹Ì¿¡¢Ê¯»ÒʯÊÇ´ÓÔÁÏÈë¿Ú¼ÓÈ룬ÆäÖн¹Ì¿Ôڸ߯Á¶ÌúʱµÄ×÷ÓÃÖ®Ò»ÊDzúÉú¸ßÎÂ,ÁíÒ»×÷ÓÃΪ £»ÉúÌú³ö¿ÚµÍÓÚ¯Ôü³ö¿ÚµÄÔÒòÊÇ ¡£
30£®£¨6·Ö£©Ð¡Ã÷ͬѧÔÚʳƷ°ü×°´üÄÚ£¬·¢ÏÖÓÐÒ»¸öСֽ´ü£¬ÉÏÃæд×Å¡°Éúʯ»Ò¸ÉÔï¼Á£¬ÇëÎðʳÓᱡ£ËûËæÊÖ½«Ð¡Ö½´üÄóöÀ´·ÅÔÚ×ÀÃæÉÏ£¬¾¹ýÒ»¶Î½Ï³¤Ê±¼äºó·¢ÏÖÖ½´üÄڵİ×É«¿ÅÁ£Õ³ÔÚÒ»Æð³ÉΪ¿é×´¹ÌÌåM¡£ÇëÄãÓëËûÒ»Æð¶Ô¿é×´¹ÌÌåM½øÐÐ̽¾¿¡£
¡¾Ì½¾¿ÈÎÎñ¡¿
£¨1£©Ì½¾¿¹ÌÌåMÊÇ·ñʧЧ£»
£¨2£©Ì½¾¿¹ÌÌåMÖÐÊÇ·ñº¬ÓÐÇâÑõ»¯¸Æ¡£
¡¾Ì½¾¿·½°¸¡¿
ÎÊÌâÓë²ÂÏë
ʵÑé²½Öè
ʵÑéÏÖÏó
ʵÑé½áÂÛ
̽¾¿Ò»£º¹ÌÌåMÊÇ·ñʧЧ
È¡ÊÊÁ¿¹ÌÌåM£¬¼ÓÈëÊ¢ÓÐË®µÄÉÕ±ÖУ¬ÓÃζȼƲâÁ¿¼ÓÈëÇ°ºóµÄζÈ
ζÈûÓÐÃ÷ÏԱ仯
̽¾¿¶þ£º¹ÌÌåMÖÐÊÇ·ñº¬ÓÐÇâÑõ»¯¸Æ
½«ÉÏÊöÉÕ±ÄÚµÄÒºÌå³ä·Ö½Á°è¡¢¾²Öã¬È¡ÉϲãÇåÒº£¬¼ÓÈëÎÞÉ«·Ó̪ÊÔÒº
ÓÐÇâÑõ»¯¸Æ
¡¾·´Ë¼ÍØÕ¹¡¿
£¨1£©ÄãÈÏΪ¡°Ì½¾¿¶þ¡±ÊÇ·ñÑÏÃÜ £¬ÆäÔÒòÊÇ £»
£¨2£©ÄãÈÏΪ¹ÌÌåMÖгýº¬ÓÐÇâÑõ»¯¸ÆÍ⣬»¹¿ÉÄܺ¬ÓÐ £¬ÇëÄãÉè¼ÆʵÑéÊÇ·ñº¬ÓиÃÎïÖÊ ¡£
Îå¡¢¼ÆËãÌâ
31£®£¨7·Ö£©Ä³»¯Ñ§ÐËȤС×éΪÁ˲ⶨһÅúʯ»ÒʯÑùÆ·ÖÐ̼Ëá¸ÆµÄÖÊÁ¿·ÖÊý£¬È¡ÓÃ
ʵÑé´ÎÊý
µÚ1´Î
µÚ2´Î
µÚ3´Î
µÚ4´Î
¼ÓÈëÏ¡ÑÎËáµÄÖÊÁ¿£¯g
20
20
20
20
Ê£Óà¹ÌÌåµÄÖÊÁ¿£¯g
11
6
3.2
n
£¨1£©ÉϱíÖÐnµÄÊýֵΪ__________¡£ÓÉÉϱíÊý¾Ý¿ÉÖªÕâËÄ´ÎʵÑéÖУ¬µÚ ´ÎËù¼ÓµÄÑÎËáû·´Ó¦Íê¡£
£¨2£©Ê¯»ÒʯÑùÆ·ÖÐ̼Ëá¸ÆµÄÖÊÁ¿·ÖÊýÊÇ____________¡£
£¨3£©Èç¹û¸Ãʯ»Ò³§ìÑÉÕ50tÕâÖÖʯ»Òʯ£¬×î¶à¿ÉµÃµ½¶þÑõ»¯Ì¼ÆøÌå¶àÉÙ¶Ö£¿£¨±¾Ð¡ÌâÒªÇóд³öÍêÕûµÄ¼ÆËã¹ý³Ì£¬½á¹û±£ÁôСÊýµãºó1룩
¹ú¼ÊѧУÓÅÑ¡ - Á·Ï°²áÁбí - ÊÔÌâÁбí
ºþ±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨Æ½Ì¨ | ÍøÉÏÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | µçÐÅթƾٱ¨×¨Çø | ÉæÀúÊ·ÐéÎÞÖ÷ÒåÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com