
2009年广东省茂名市初中毕业生学业考试与高中阶段学校招生考试
化学试卷
可能用到的相对原子质量:H-l C-12 O-16 Cl - 35.5 Na-23 Mg-24
第一卷(选择题,共30分)
一、选择题(本题有10小题,每小题3分,共30分。每小题只有一个选项符合题意)
1.下列做法会加剧温室效应的是
A.大力植树造林 B.鼓励私人使用小汽车代替公交车
C.骑自行车上下班 D.大量利用太阳能、风能和氢能等新能源
2.下列说法正确的是
A.空气是混合物,其中氧气质量约占空气质量的五分之一
B.O2能跟所有物质发生氧化反应
C.CO和C都具有还原性,可用于冶金工业
D.香烟的烟气中含有二氧化碳等多种有毒物质
3.下列变化属于化学变化的是
A.干冰升华 B.电解水制氢气和氧气
C.汽油挥发 D.海水通过高分子分离膜制淡水
4.下列说法正确的是
A.木柴温度达到着火点就燃烧 B.化学反应中,原子都失去最外层电子
C.化学反应都伴有能量变化 D.催化剂在反应后质量会减少
5.下列有关水的说法正确的是
A.蒸馏水属于硬水 B.净化水时,可用活性炭作杀菌剂
C.水变成水蒸气,水分子变大 D.湿衣服晾干说明分子作不断运动
6.下列说法正确的是
A.棉花属于天然有机高分子材料
B.缺铁会引起贫血,故人体补铁越多越好
C.多吃水果和蔬菜能给人体补充油脂
D.霉变的大米用清水洗干净后继续食用
7.下列选项中代表离子的是(说明:数字代表质子数,“+”表示原子核所带的电荷,黑点代表核外电子)
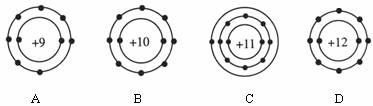
8.下列说法正确的是:
A.碳酸氢钠可用于治疗胃酸过多症 B.用酚酞区分氢氧化钾和氢氧化钠溶液
C.浓硫酸溶于水时吸收热量 D.不能用食盐作原料制氢氧化钠
9.据报道,用750mL/L的乙醇处理5分钟,即可杀灭活甲型H1N1流感病毒。以下关于乙醇(化学式:C2H6O)说法不正确的是:
A.乙醇可用作消毒剂
B.乙醇中碳、氢、氧三种元素的质量比为2:6:1
C.乙醇由碳、氢、氧三种元素组成
D.乙醇是一种可再生能源
10.物质M的溶解度曲线如下图所示。下列说法正确的是

A.M的溶解度随温度升高而增大
B.使用降温法可使M从饱和的水溶液中析出
C.在
D.在
第二卷(非选择题,共70分)
二、填空题(本题有3小题,共16分)
11.(2分)用正确的数字和符号填空:
(1)2个氯原子____; (2)保持氧气化学性质的微粒______
12.(6分回答下列有关军事上的问题:
(1)火药:火药爆炸时反应的化学方程式为:2KNO3+S+
(2)烟雾弹:将装有白磷(P)的烟雾弹引爆后,白磷在空气中燃烧,再发生一系列反应,产生大量烟雾将目标隐蔽。写出白磷燃烧的化学方程式_________________,该反应的基本类型是_______。
13.(8分)根据一定的标准对物质进行整理和分类,是学习化学有效的方法。回答问题:
(1)盐酸、硫酸属于酸,其分类标准是:它们在水溶液中离解出的阳离子都是________。
(2)根据“组成元素种类的异同”,可将纯净物分为__________和__________。
(3)某同学将含碳元素的不同物质按一定的分类标准进行整理,得到如下的物质关系:
C→CO2→H2CO3→Na2CO3。请你参照他的分类标准,完成含钙元素的不同物质关系:
___ ____ _→_ ____ ___→____________→__________。
三、简答题(本题有3小题,共21分)
14.(2分)物质的结构决定物质的性质,性质决定用途。回答下列问题:
(1)石墨与金刚石性质不同是由于它们的____________________不同。
(2)CO2不燃烧、也不支持燃烧,故CO2能用来____________________。
15.(8分)铬(Cr)为不锈钢主要的添加元素,含量一般在12%以上。铬的表面生成一薄层致密的钝态氧化物保护膜是不锈钢具有耐蚀性主要原因。请回答下列问题:
(1)铁生锈的主要条件是铁与________和________直接接触。
(2)不锈钢是一种____________(填“合金”或“金属”)。
(3)相同温度下,取大小相同、表面光亮的Cr、Mg、Cu三种金属薄片,分别投入等体积等溶质质量分数的足量稀盐酸中(反应中Cr显+2价),现象如下:
金属
Cr
Mg
Cu
与盐酸反应现象
放出气泡速率缓慢
放出气泡速率较快
无明显现象
①上述三种金属的活动性由强到弱的顺序是__________________。
②从上述探究实验可知,Cr(填“能”或“不能”)跟CuSO4溶液反应。若反应,请写出反应的化学方程式______________________________。
16.(11分)废干电池内的黑色固体含有MnO2、ZnCl2、NH4Cl、C(少量)等物质。化学小组欲通过以下流程,分离并回收部分物质。回答相关问题;

(1)玻璃棒在操作I中的作用:____________________。
(2)过滤后,滤液C仍然浑浊,则造成浑浊的原因可能是____________(填编号)。
A.滤纸破损 B.过滤过程中滤液的液面超过了滤纸的边缘
C.烧杯不干净 D.滤波C中的物质相互反应
(3)固体B常用作催化剂,则B是 __ (填化学式),写出在空气中灼烧A时发生反应的化学方程式:_______________。
(4)仅用硝酸银溶液 (填“能”或“不能”)区分E和F。某同学认为固体E是NH4Cl,则检验方法是: ______________________ 。
(5) NH4Cl属于化学肥料中的 肥。
四、实验与探究题(本题有2小题,共21分)
17. (12分)结合下列实验装置回答相关问题:
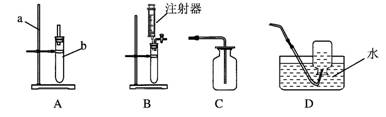
(1)写出A装置中a、b仪器的名称:____________、 __ 。
(2)用石灰石与盐酸反应制CO2的化学方程式为 ,收集装应选________(填编号);用双氧水制O2的化学方程式为 。
(3)若用B作制气装置,与A相比,其优点是 ______________ 。(写一点)
(4)用KClO3和MnO2制O2 ,若选用A作发生装置,则还要增加____________(填仪器名称),并把A作如下改动:________________________________。
18.(9分)小青探究铜与稀硫酸在加热的条件下能否发生反应的实验时,发现加热沸腾一段时间后,溶液开始变色,同时产生较多的气泡。生成的是什么气体呢?
[提出猜想]①可能是H2 ;②可能是O2 ;③可能是SO2
任何的猜想都要有依据,则小青提出猜想的依据是: ____ 。
[查阅资料]①铜与热的浓硫酸反应产生SO2;②SO2与Ca(OH)2反应生成难溶的CaSO3。
[实验验证]请你根据以下实验条件,设计实验验证小青的猜想,并将相关内容填在下表。
仅限选择的用品和试剂:试管;带火星的木条、澄清石灰水。
实验步骤
实验操作
预期现象和结论
第一步
第二步
[交流与讨论]经验证,猜想③正确,为此,小青作了如下解释:加热使溶液中的水不断蒸发,硫酸浓度逐渐增大,当达到一定浓度时,硫酸跟铜反应产生SO2气体。你觉得小青的解释_______(填“合理”或“不合理”)。
五、计算题(本题有1小题,共1 2分)
19.(12分)甲、乙、丙三位同学对氯化镁样品(仅含氯化钠杂质)进行如下检测:各取
甲
乙
丙
加入氢氧化钠溶液质量 (g)
35.0
40.0
45.0
反应得到沉淀的质量 (g)
2.5
2.9
2.9
试回答下列问题:
(1)上述实验中,__________同学所用的氢氧化钠溶液一定过量。
(2)求样品中氯化镁的含量(写出计算过程,结果精确到0.1%,下同)。
(3)计算乙同学实验后所得溶液中的氯化钠的质量分数。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com