
题目列表(包括答案和解析)

| ||
| ||

t(min) 浓度(mol/L) |
0 | 1 | 2 | 3 | 4 | 5 | 6 |
| c(C) | 0.054 | 0.034 | 0.018 | 0.012 | 0.008 | 0.006 | 0.006 |
| c(O2) | 0.032 | 0.022 | 0.014 | 0.011 | 0.009 | 0.008 | 0.008 |
t(min) 浓度(mol/L) | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| c(C) | 0.054 | 0.034 | 0.018 | 0.012 | 0.008 | 0.006 | 0.006 |
| c(O2) | 0.032 | 0.022 | 0.014 | 0.011 | 0.009 | 0.008 | 0.008 |
t(min) 浓度(mol/L) |
0 | 1 | 2 | 3 | 4 | 5 | 6 |
| c(C) | 0.054 | 0.034 | 0.018 | 0.012 | 0.008 | 0.006 | 0.006 |
| c(O2) | 0.032 | 0.022 | 0.014 | 0.011 | 0.009 | 0.008 | 0.008 |
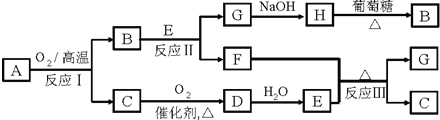
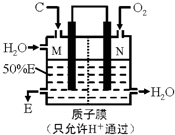
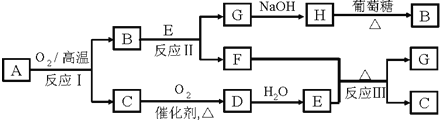
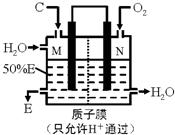
固态化合物A由两种短周期元素组成,可与水发生复分解反应,甲组同学用下图装置(夹持装置略)对其进行探究实验.

(1)仪器B的名称是________.
(2)实验中,Ⅱ中的试纸变蓝,Ⅳ中黑色粉末逐渐变为红色并有气体M生成,则Ⅳ发生反应的化学方程式为________;Ⅲ中的试剂为________.
(3)乙组同学进行同样实验,但装置连接顺序为Ⅰ——Ⅲ——Ⅳ——Ⅱ——Ⅴ,此时Ⅱ中现象为________,原因是________.
(4)经上述反应,2.5 g化合物A理论上可得0.56 L(标准状况)M;则A的化学式为________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com