
题目列表(包括答案和解析)
A.MgCl2+Ca(OH)2![]() CaCl2+Mg(OH)2↓ B.Mg(OH)2+2HCl
CaCl2+Mg(OH)2↓ B.Mg(OH)2+2HCl![]() MgCl2+2H2O
MgCl2+2H2O
C.Mg(OH)2+H2SO4![]() MgSO4+2H2O D.MgCl2
MgSO4+2H2O D.MgCl2![]() Mg+Cl2↑
Mg+Cl2↑
从海水中提取镁时,用不到的化学反应是( )
A.MgCl2+Ca(OH)2══CaCl2+Mg(OH)2↓ B.Mg(OH)2+2HCl══MgCl2+2H2O
C.Mg(OH)2+H2SO4══MgSO4+2H2O D.MgCl2![]() Mg+Cl2↑
Mg+Cl2↑
A.MgCl2+Ca(OH)2══CaCl2+Mg(OH)2↓ B.Mg(OH)2+2HCl══MgCl2+2H2O
C.Mg(OH)2+H2SO4══MgSO4+2H2O D.MgCl2![]() Mg+Cl2↑
Mg+Cl2↑
从海水中提取镁是世界各国获得镁的主要来源,下表是制镁过程中涉及的几种物质的溶度积,根据你所学的知识回答下列问题:
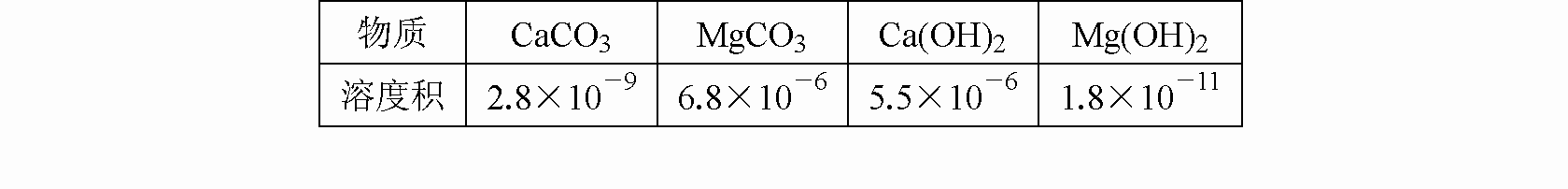
(1)从海水中提到镁时,往往会用到贝壳(主要成分是碳酸钙),你认为能否将贝壳研磨成粉末后直接投入海水中去获得含有镁元素的化合物?________(填“能”或“否”),其理由是________;如果不能直接投入,应将贝壳如何处理才能投入海水中,试写出有关贝壳处理过程中涉及的反应的化学方程式:________.
(2)某同学在实验室条件下模拟该生产过程,但实验室无石灰,他打算用纯碱代替,你认为可否得到Mg(OH)2沉淀?________(填“能”或“否”).在加试剂时,误将纯碱溶液加入海水中,他思考了一下,又在得到的混合体系中加入过量的烧碱溶液,你觉得他能否将Mg2+转化为Mg(OH)2沉淀?________(填“能”或“否”),理由是________.
(3)常温下,已知某地海水中镁离子的浓度为1.8×10-3 mol/L,要使镁离子产生沉淀,溶液的pH值最低应为________.
海水中提取镁的工业流程如下图所示:

回答下列问题。
⑴用贝壳而不从异地山中开凿石灰石的原因是______________________________。
⑵母液中含有MgCl2,写出反应池1的离子方程式_________________________。
⑶反应池1中,加入Ca(OH)2,使溶液的pH为11时,认为Mg2+沉淀完全[c(Mg2+)<1×10-5mol·L-1],则Mg(OH)2的溶度积约为_______________________。
⑷干燥塔中,在干燥的HCl气流中加热MgCl2·6H2O时,能得到无水MgCl2,其原因是_______________________________________________________________。
⑸电解槽中先得到的是镁的蒸气,镁蒸气可以在下列_____(填编号)气体氛围中冷却。
A.空气 B.氧气 C.水蒸气 D.氢气
⑹镁可用于生产金属钛,主要步骤有:①在高温下,向金红石(主要成分TiO2)与焦炭的混合物中通入Cl2,得到TiCl4和一种可燃性气体;②在稀有气体(如氩)氛围和加热条件下,用镁与TiCl4反应可得到钛。写出上述两步反应的化学方程式。
反应①:____________________________________________________________;
反应②:____________________________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com