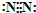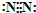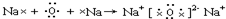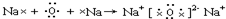¶̀ÖÜÆÚÖ÷×åÔªËØA¡¢B¡¢C¡¢D¡¢EµÄÔ×ÓĐ̣ÊửÀ´ÎÔö´ó£®̉ÑÖª£ºAÓëBÄÜĐγÉ̉»ÖÖ¼îĐÔÆø̀壬DÊǶ̀ÖÜÆÚÔªËØÖĐÔ×Ӱ뾶×î´óµÄÖ÷×åÔªËØ£¬C¡¢EµÄ×îÍâ²ăµç×ÓÊưÏàµÈ£¬Ç̉C¡¢EµÄÔ×ÓĐ̣ÊưÖ®ºÍΪA¡¢DµÄÔ×ÓĐ̣ÊưÖ®ºÍµÄ2±¶£®
ÊԻشđÏÂÁĐÎỀ⣺
£¨1£©Đ´³öÁ½ÖÖÓÉÉÏÊöÔªËØĐγɵľßÓĐƯ°××÷ÓõÄÎïÖʵĻ¯Ñ§Ê½£º
H2O2¡¢Na2O2
H2O2¡¢Na2O2
£®
£¨2£©Đ´³öÓÉBĐγɵĵ¥Öʵĵç×Óʽ£º
£»ÉÏÊö¼îĐÔÆø̀åÊÇ
¼«ĐÔ
¼«ĐÔ
£῭î¡°¼«ĐÔ¡±»̣¡°·Ç¼«ĐÔ¡±£©·Ö×Ó£®
£¨3£©ÓÉA¡¢C¡¢EÈưÖÖÔªËØÖеÄ̉»ÖÖ»̣Á½ÖÖ¿É·Ö±đĐγɼס¢̉̉Á½ÖÖÁ£×Ó£¬ËüĂǾùÊÇ-2¼ÛµÄ̉ơÀë×Ó£¬Ç̉¼×ΪËĺË42µç×ÓµÄ΢Á££¬̉̉Ϊµ¥ºË18µç×ÓµÄ΢Á££¬Ộ¼×Óë̉̉ÔÚËáĐỒơ¼₫Ï·´Ó¦µÄÀë×Ó·½³̀ʽΪ£º
SO32-+2S2-+6H+¨T3S¡ư+3H2O
SO32-+2S2-+6H+¨T3S¡ư+3H2O
£®
£¨4£©Óõç×Óʽ±íʾC¡¢DÁ½ÖÖÔªËØĐγɻ¯ºÏÎïD
2CµÄ¹ư³̀
£®