下面几位同学是测量空气中氧气体积含量的四个实验,请你参与他们的实验探究:
[实验一]小强采用A图所示的装置进行实验:在由两个注射器组成的密闭系统中留有25mL空气,给装有细铜丝的玻璃管加热,同时缓慢推拉两个注射器活塞,至玻璃管内的铜丝在较长时间内无进一步变化时停止加热,待冷却至室温,将气体全部推至一个注射器内,观察密闭系统内空气体积变化.
(1)在实验加热过程中,交替缓慢推动两个注射器活塞的目的是________.
(2)该反应的化学反应表达式________,铜丝表面的变化是________.
(3)小强测得实验结果如下:
| 反应前注射器内气体总体积 | 反应后注射器内气体总体积 |
| 25mL | 22mL |
由此数据可以推算出他测定的空气中氧气的体积分数________2l%(填“>”、“=”、“<”).造成该实验出现误差的原因可能是________.(填序号,)
①没有交替缓缓推动两个注射器活塞;
②读数时没有冷却至室温;
③加入铜丝量太少;
[实验二]:小红采用B图所示的装置进行实验:实验过程如下:
第一步:将集气瓶容积划分为五等份,并做好标记.
第二步:用放大镜点燃燃烧匙内的红磷.
第三步:待红磷熄灭并冷却后,打开弹簧夹,发现水被吸入集气瓶中,进入集气瓶中水的体积约为集气瓶总容积的1/5.
请回答下列问题:
(1)集气瓶中剩余的气体主要是________,根据实验推断它的性质有________.
(2)实验完毕,若进入集气瓶中水的体积小于总容积的
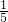
,其原因可能是________,若进入集气瓶中水的体积大于总容积的
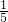
,其原因可能是________.
(3)红磷燃烧的现象是________,化学反应表达式为________.
[实验三]小华同学打算采用C图所示的装置进行实验:设计如下方案:选用实际容积为25mL的试管作为反应容器,将过量的白磷放入试管,用橡皮塞塞紧试管,通过导管与注射器(注射器的容积为40ml,且润滑性很好)相连,注射器的前沿停在20ml刻度处.(假设此实验能够按照小华的设想正常进行,白磷所占体积与导管内的气体体积忽略不计,且两个容器间的导管足够粗,保持空气正常流动.)请回答下列问题:
(1)实验前,打开弹簧夹,将注射器活塞前沿从20mL刻度处推至15mL刻度处,然后松开手,若活塞仍能返回至20mL刻度处,则说明________;
(2)若先夹紧弹簧夹,用酒精灯加热白磷,燃烧结束,试管冷却后,再松开弹簧夹.可观察到的现象为:________;
(3)若不使用弹簧夹,用酒精灯加热白磷,燃烧结束,试管冷却.在实验的过程中观察到的现象为________,________,________.
(4)若按小华的设想进行实验,实际可能遇到诸多问题而发生危险,造成实验失败.例如:________.
[实验四]小明用图D装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.
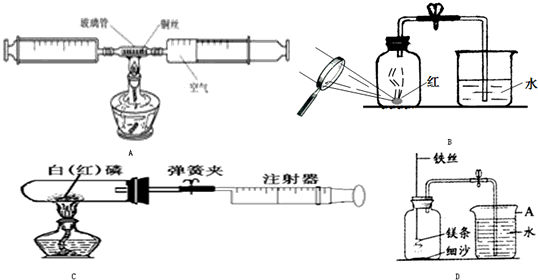
(1)如图A仪器的名称是________,
镁带燃烧的反应表达式为________、冷却后打开止水夹,水能进入集气瓶的原因是________.
(2)如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的________%.现进入集气瓶中水的体积约为其容积的70%,根据空气的组成可推出减少的气体中有________.

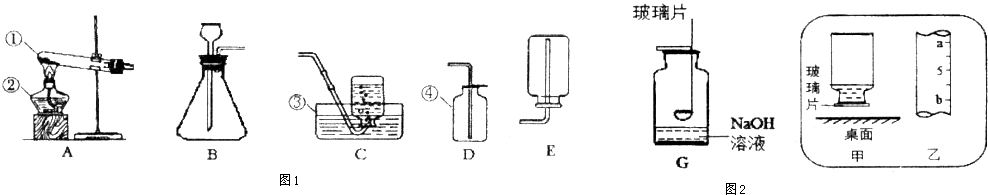
 17、人的胃液里含有适量的盐酸,可以帮助消化,但如果胃酸分泌过多,人会感到胃痛.小军拿来了一种抗酸药(治疗胃酸过多的药物),该药物说明书的部分内容如图所示.当小军看到药物说明书上的服用方法后,对此产生了探究的兴趣,请你和他一起完成探究活动.
17、人的胃液里含有适量的盐酸,可以帮助消化,但如果胃酸分泌过多,人会感到胃痛.小军拿来了一种抗酸药(治疗胃酸过多的药物),该药物说明书的部分内容如图所示.当小军看到药物说明书上的服用方法后,对此产生了探究的兴趣,请你和他一起完成探究活动.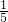 ,其原因可能是________,若进入集气瓶中水的体积大于总容积的
,其原因可能是________,若进入集气瓶中水的体积大于总容积的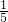 ,其原因可能是________.
,其原因可能是________.
