
题目列表(包括答案和解析)
a、b、c、d、e、f是原子序数依次增大的6种短周期元素,a、d同主族,a是子半径最小的元素,b的最高正价与最低负价的代数和为零,a与c、d与c均可形成原子个数比为2:1和1:1的化合物,d、e的最外层电子数之和等于b的最外层电子数,f是同周期中得电子能力最强的元素。
(1)画出f元素的原子结构示意图 。在a、c、d三种元素形成的化合物中存在的化学键类型是 。
(2)写出d、e两元素的最高价氧化的水化物之间反应的离子方程式 。
(3)写出下列反应的化学方程式(有机物用结构简式表示):
①将化合物a6b6与浓硫酸和浓硝酸的混合液共热并保持(55~60)℃反应 ;
②将a6b2c和氧气的混合气体通过加热的铜网反应 。
 (4)甲、乙、丙、丁四种无机物具有如图所示的转化关系,甲是f的单质,且甲、乙、丙中均含有同一种元素,丁为金属单质,请写出检验乙中阳离子的一种方法:
(4)甲、乙、丙、丁四种无机物具有如图所示的转化关系,甲是f的单质,且甲、乙、丙中均含有同一种元素,丁为金属单质,请写出检验乙中阳离子的一种方法:
。
 )常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精.
)常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精.
【化学——有机化学】
肉桂酸甲酯(![]() ),常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精。
),常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精。
(1)有关肉桂酸甲酯的叙述中,正确的是 (填标号)。
A.能与溴的四氯化碳溶液发生加成反应 B.无法使酸性高锰酸钾溶液褪色
C.在碱性条件下能发生水解反应 D.不可能发生加聚反应
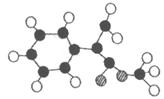 (2)G为肉桂酸甲酯的一种同分异构体,其分子结构模型如右图所示(图中球与球之间连线表示单键或双键)。
(2)G为肉桂酸甲酯的一种同分异构体,其分子结构模型如右图所示(图中球与球之间连线表示单键或双键)。
G的结构简式为 。
(3)用芳香烃A为原料合成G的路线如下:
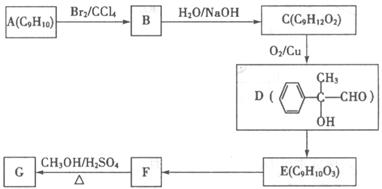 |
②B→C该反应的化学方程式为: 。
③E→F的反应类型是 。
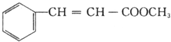 ),常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精.
),常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精.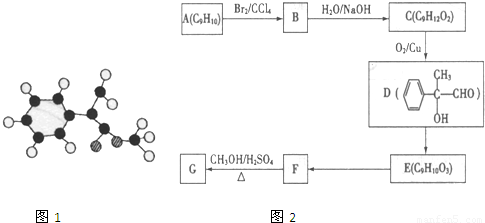
 已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E<F.其中A原子核外有三个未成对电子;化合物B2E的晶体为离子晶体,E原子核外M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的晶体类型在同周期的单质中没有相同的;F原子核外最外层电子数与B相同,其余各层电子均充满.请根据以上信息,回答下列问题:(答题时,A、B、C、D、E、F用所对应的元素符号表示)
已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E<F.其中A原子核外有三个未成对电子;化合物B2E的晶体为离子晶体,E原子核外M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的晶体类型在同周期的单质中没有相同的;F原子核外最外层电子数与B相同,其余各层电子均充满.请根据以上信息,回答下列问题:(答题时,A、B、C、D、E、F用所对应的元素符号表示)湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com